4.2 Atommasse
Die Masse eines einzelnen Atoms ist unvorstellbar klein.
Die geringste Masse besitzt ein Wasserstoffatom (H-Atom):
m(Wasserstoffatom) = 0, (23 Nullen) 1 67 g
m(H-Atom) = 0,000 000 000 000 000 000 000 001 67 g = 1,67 • 10-24 g = 1 u
Zur Erinnerung: 1 t = 1 000 kg = 10 • 10 • 10 kg = 10³ kg = 106 g = 109 mg
Eine Angabe der Atommasse in Gramm ist somit nicht sinnvoll. Man hat deshalb für die Atommasse eine eigene Einheit eingeführt:
die atomare Masseneinheit u (engl. unit = Einheit)
1 u entspricht etwa der Masse des Wasserstoff-Atoms.
Im PSE steht die Atommasse links über dem Elementsymbol. 1H
Zwischen der Einheit 1 g und 1 u besteht folgender Zusammenhang:
1 g = 602 200 000 000 000 000 000 000 u = 6,022 • 1023 u
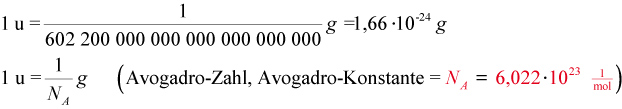
Veranschaulichung der Avogadro-Konstante:
- Länge Erdumfang: ~ 4 · 1010 mm
- Entfernung Erde-Mond: ~ 4 · 105 km ~ 4 · 1011 mm
- Fläche Erdoberfläche: ~ 5 · 108 km² ~ 5 · 1020 mm²
- Volumen Erdinhalt: ~ 1 · 1030 mm³
- Zeit seit Christi Geburt: ~ 6 · 1010 s
- 1 mol Ethanolmoleküle (C2H5OH) werden gleichmäßig in den Weltmeeren verrührt. Jetzt enthält jedes Liter Meerwasser (1,37 Milliarden km³) immer noch 460 Ethanolmoleküle.
Wie viel H-Atome wiegen genau ein Gramm?
1 g = 6,022·1023
Beispiele einiger Atommassen (gerundet)
| 1 H-Atom | hat die Masse | 1 u | 6,022 • 1023 H-Atome haben die Masse | 1g | 1 mol H-Atome haben die Masse | 1 g |
| 1 C-Atom | hat die Masse | 12 u | 6,022 • 1023 C-Atome haben die Masse | 12 g | 1 mol C-Atome haben die Masse | 12 g |
| 1 N-Atom | hat die Masse | 14 u | 6,022 • 1023 H-Atome haben die Masse | 14 g | 1 mol H-Atome haben die Masse | 14 g |
| 1 O-Atom | hat die Masse | 16 u | 6,022 • 1023 H-Atome haben die Masse | 16 g | 1 mol H-Atome haben die Masse | 16 g |
| 1 Mg-Atom | hat die Masse | 24 u | 6,022 • 1023 H-Atome haben die Masse | 24 g | 1 mol H-Atome haben die Masse | 24 g |
1 mol Ethanolmoleküle (C14 g
