Was du auf dieser Seite lernst
Du lernst, wie Carbonsäuren und Alkohole in einer Kondensationsreaktion zu Estern und Wasser reagieren. Am Beispiel des Estergleichgewichts (Essigsäure + Ethanol) wird deutlich, dass sowohl Hin- als auch Rückreaktion zum gleichen Endzustand führen – ein klassisches Beispiel für ein chemisches Gleichgewicht.
Grundlagen aus der 10. Klasse
Die Grundlagen zu Carbonsäuren und Alkoholen hast du bereits in der 10. Klasse kennengelernt:
→ Essigsäure / Ethansäure (Kl. 10) ·
→ Alkohole / Alkanole (Kl. 10)
2.5 Estergleichgewicht
Allgemeine Reaktion
Carbonsäure + Alkohol ⇌ Ester + Wasser
Wer sich an die 10. Klasse erinnern kann, kann ja mal versuchen, die Reaktionsgleichung für Ethansäure und Ethanol zu formulieren.
Tipp 1: Es handelt sich um eine Kondensationsreaktion – zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (hier: Wasser).
Tipp 2: Es reagieren meist die funktionellen Gruppen miteinander und selten die Alkylgruppen.
Allgemeine Reaktionsgleichung (Summenformeln)
R–COOH + R'–OH ⇌ R–COO–R' + H2O
Carbonsäure + Alkohol ⇌ Ester + Wasser | Katalysator: H+ (z. B. konz. H2SO4)
Lösung: Reaktionsgleichung Ethansäure + Ethanol
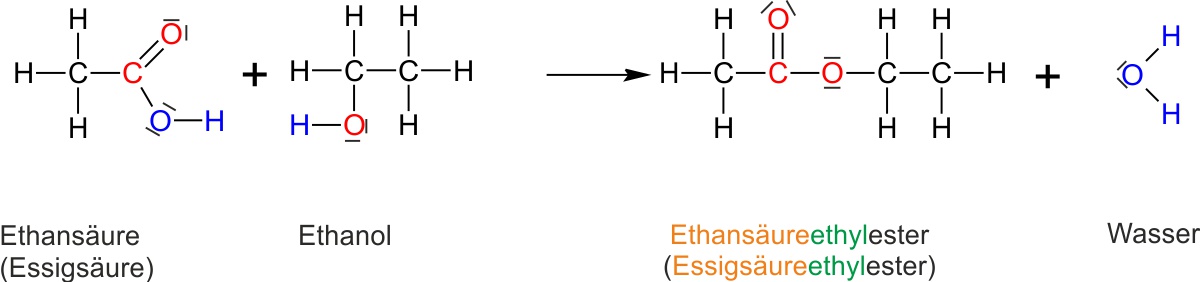
Mechanismus der Veresterung (säurekatalysiert)
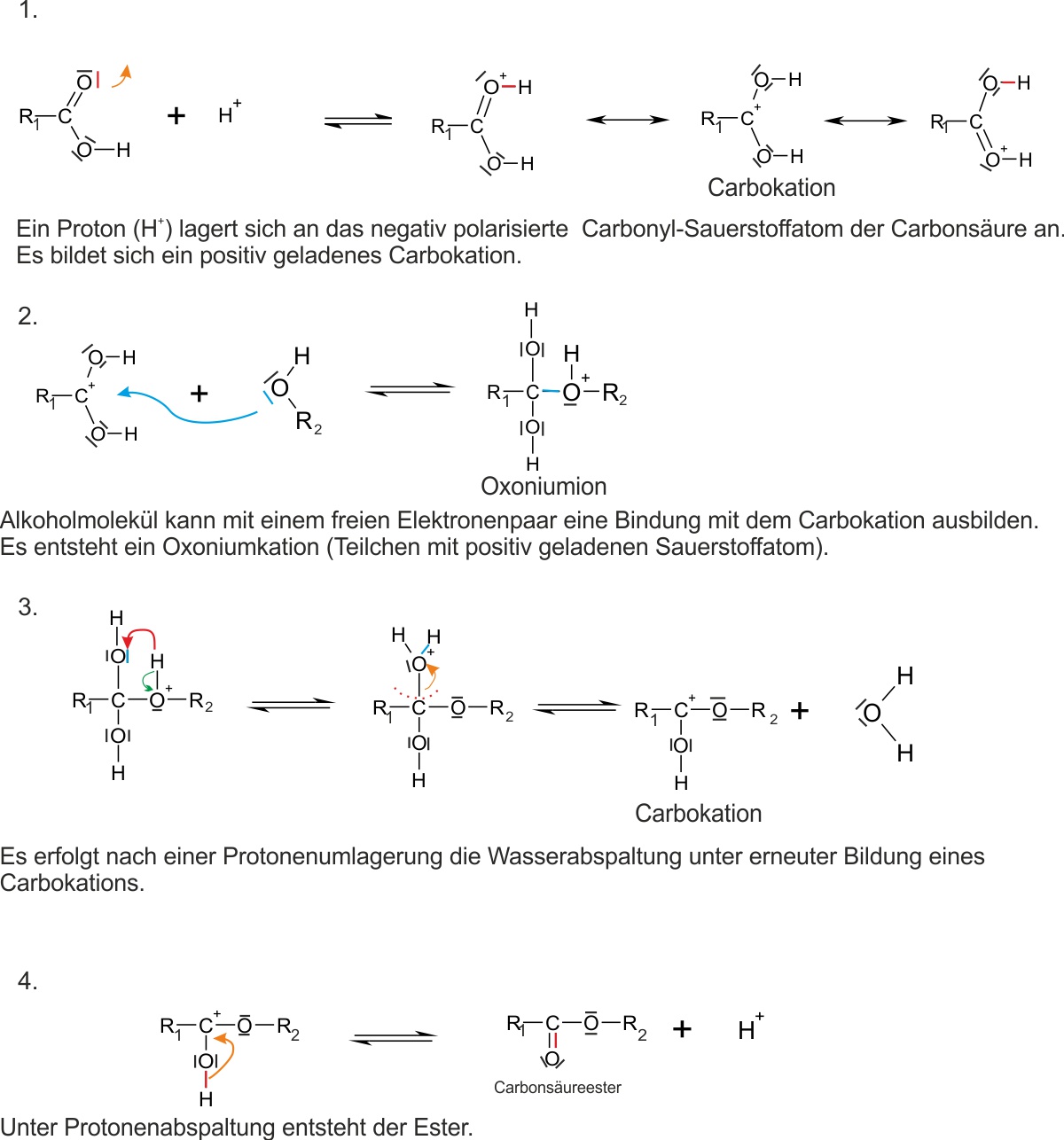
Der Mechanismus der säurekatalysierten Veresterung verläuft in vier reversiblen Teilschritten. Der Katalysator (H+) wird am Ende wieder freigesetzt:
↑ Zum Vergrößern klicken
Die 4 Teilschritte in Kurzform
1. Protonierung der Carbonylfunktion der Carbonsäure → Carbokation
2. Nukleophiler Angriff des Alkohols (freies Elektronenpaar) → Oxoniumion
3. Protonenumlagerung → Wasserabspaltung → erneutes Carbokation
4. Protonenabspaltung (H+ wird regeneriert) → Carbonsäureester
Alle Teilschritte sind reversibel (⇌). Der H+-Katalysator beschleunigt die Reaktion, verschiebt aber das Gleichgewicht nicht.
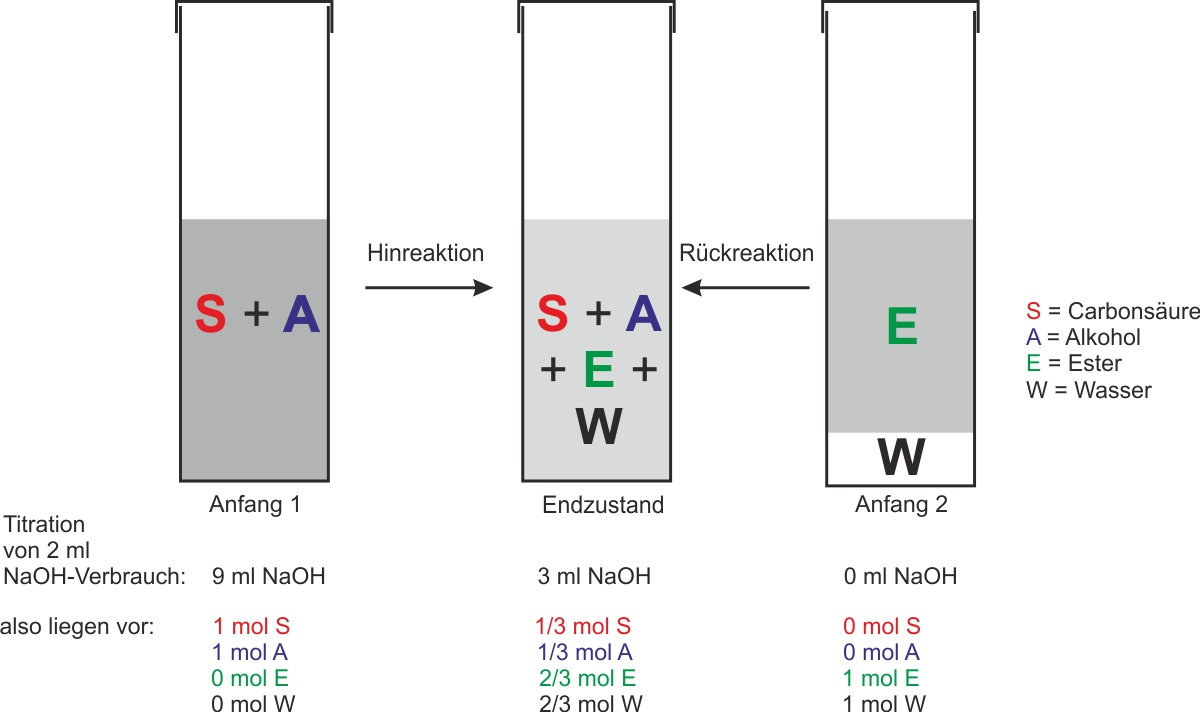
Das Estergleichgewicht – Nachweis durch zwei Versuchsansätze
Versuchsansatz 1 (Hinreaktion): Man gibt 1 mol Carbonsäure und 1 mol Alkohol zusammen.
Versuchsansatz 2 (Rückreaktion): Man gibt 1 mol Ester und 1 mol Wasser zusammen.
Tipp: Was erwartest du?
Schau dir nochmals die Merkmale eines chemischen Gleichgewichts an. Ein echtes Gleichgewicht wird vom gleichen Endzustand aus erreicht – egal von welcher Seite man startet.
Lösung: Ergebnis des Experiments
Ergebnis: Man erhält in beiden Fällen denselben Endzustand.
↑ Zum Vergrößern klicken
Reaktionsgleichung und Mengenverhältnisse im Gleichgewicht
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
| Zeitpunkt | n(CH3COOH) | n(C2H5OH) | n(Ester) | n(H2O) |
|---|---|---|---|---|
| Anfang 1 (Hinreaktion) | 1 mol | 1 mol | 0 mol | 0 mol |
| Gleichgewicht | ⅓ mol | ⅓ mol | ⅔ mol | ⅔ mol |
| Anfang 2 (Rückreaktion) | 0 mol | 0 mol | 1 mol | 1 mol |
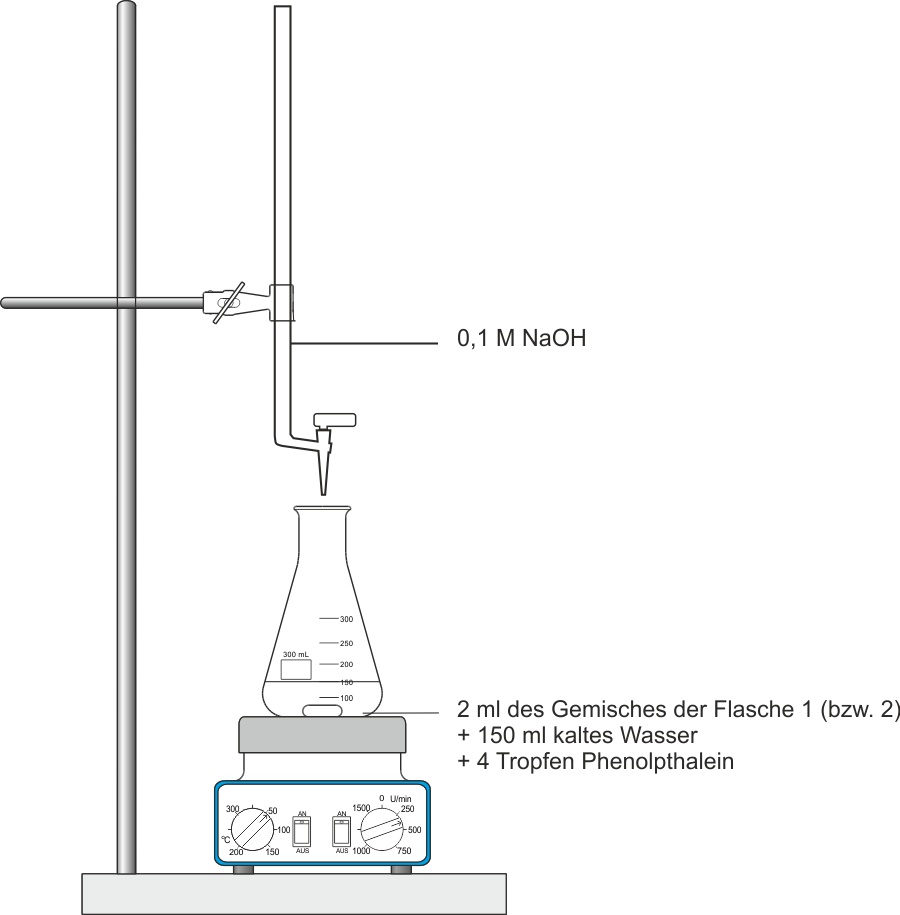
Quantitativer Nachweis: Titration der Carbonsäure
Man kann in beiden Versuchsansätzen die vorhandene Carbonsäuremenge durch quantitative Reaktion mit Natronlauge (Titration) messen.
Reaktionsgleichung der Titration (Summenformeln)
CH3COOH + NaOH → CH3COONa + H2O
Essigsäure reagiert vollständig und quantitativ mit NaOH. Mit 0,1 M NaOH und dem Verbrauch kann die Säuremenge berechnet werden: n(CH3COOH) = c(NaOH) · V(NaOH)
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
KONDENSATIONSREAKTION
Bei der Veresterung verbinden sich Carbonsäure und Alkohol unter Abspaltung von Wasser – typische Kondensationsreaktion.
MECHANISMUS
4 reversible Schritte: Protonierung → Carbokation → Oxoniumion → Wasserabspaltung → Ester. H+ ist Katalysator.
GLEICHGEWICHT
Hin- und Rückreaktion erreichen denselben Endzustand: ⅔ mol Ester + ⅔ mol Wasser (aus je 1 mol Edukt).
TITRATION
Der Gleichgewichtszustand lässt sich quantitativ nachweisen: Die Carbonsäuremenge wird durch Titration mit NaOH bestimmt.
Häufige Fragen – Estergleichgewicht
Was ist eine Kondensationsreaktion und warum ist die Veresterung eine solche?
Bei einer Kondensationsreaktion verbinden sich zwei Moleküle unter Abspaltung eines kleinen Moleküls – hier Wasser. Bei der Veresterung reagiert die Carboxylgruppe (–COOH) der Carbonsäure mit der Hydroxylgruppe (–OH) des Alkohols: Beide funktionellen Gruppen treten miteinander in Wechselwirkung, und als Nebenprodukt entsteht ein Wassermolekül. Mehr zur Carboxylgruppe findest du auf der Seite Funktionelle Gruppe der Monocarbonsäuren (Kl. 10).
Wie läuft der Mechanismus der säurekatalysierten Veresterung ab?
Der Mechanismus verläuft in vier reversiblen Schritten: (1) Ein Proton (H+) lagert sich an das Carbonyl-Sauerstoffatom der Carbonsäure – es entsteht ein Carbokation. (2) Ein freies Elektronenpaar des Alkohols greift das Carbokation an – es bildet sich ein Oxoniumkation. (3) Nach einer Protonenumlagerung wird Wasser abgespalten und erneut ein Carbokation gebildet. (4) Durch Protonenabspaltung entsteht der fertige Ester, und H+ wird regeneriert.
Warum führen Hin- und Rückreaktion zum gleichen Endzustand?
Weil es sich um ein echtes chemisches Gleichgewicht handelt. Das Gleichgewicht wird dynamisch erreicht: Hin- und Rückreaktion laufen gleichzeitig ab, bis ihre Geschwindigkeiten gleich groß sind. Egal ob man mit 1 mol Carbonsäure + 1 mol Alkohol (Hinreaktion) oder mit 1 mol Ester + 1 mol Wasser (Rückreaktion) startet – der Endzustand ist identisch: ca. ⅔ mol Ester und ⅔ mol Wasser liegen neben ⅓ mol Carbonsäure und ⅓ mol Alkohol vor. Mehr zu den Merkmalen eines Gleichgewichts: Merkmale eines chemischen Gleichgewichts.
Wie kann man das Estergleichgewicht zugunsten des Esters verschieben?
Nach dem Prinzip von Le Chatelier kann das Gleichgewicht verschoben werden, indem man:
• einen der Reaktionspartner im Überschuss einsetzt (z. B. mehr Alkohol),
• ein Produkt laufend entzieht (z. B. Wasser durch Destillation oder mit einem Trockenmittel entfernt).
Hinweis: Ein Katalysator (konz. H2SO4) beschleunigt lediglich die Gleichgewichtseinstellung – er verschiebt das Gleichgewicht nicht.
Mehr dazu: Prinzip von Le Chatelier.
Wie wird das Estergleichgewicht experimentell nachgewiesen?
Man misst quantitativ die verbliebene Carbonsäuremenge durch Titration mit Natronlauge (NaOH) und dem Indikator Phenolphthalein. Aus dem NaOH-Verbrauch lässt sich n(Carbonsäure) berechnen: n = c(NaOH) · V(NaOH). Beim Gleichgewichtsansatz verbraucht man nur noch ⅓ des ursprünglichen NaOH-Verbrauchs, was zeigt, dass ⅔ der Essigsäure abreagiert haben. Mehr zur Säure-Base-Titration: Säure-Base-Titration (Kursstufe).
Lernkarten – Estergleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist eine Kondensationsreaktion? Nenne ein Beispiel.
Zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (z. B. H2O). Beispiel: Veresterung – Carbonsäure + Alkohol → Ester + Wasser.
Welche Zwischenstufen entstehen im Mechanismus der säurekatalysierten Veresterung?
1. Carbokation (nach Protonierung der Carbonsäure)
2. Oxoniumkation (nach Angriff des Alkohols)
3. erneutes Carbokation (nach Wasserabspaltung)
→ Ester + H+ (regeneriert)
Was beweist das Estergleichgewicht-Experiment mit zwei Ansätzen?
Beide Ansätze (1 mol S + 1 mol A bzw. 1 mol E + 1 mol W) führen zum gleichen Endzustand – Beweis für ein echtes dynamisches Gleichgewicht.
Nenne zwei Maßnahmen, um das Estergleichgewicht auf die Esterseite zu verschieben.
1. Überschuss eines Reaktionspartners (z. B. mehr Alkohol)
2. Entzug eines Produkts (z. B. Wasser abdestillieren oder binden)
→ Prinzip von Le Chatelier
Nicht geeignet: Katalysator – beschleunigt nur, verschiebt nicht.
Beim GG-Ansatz (1 mol CH3COOH + 1 mol C2H5OH) verbraucht die Titration von 2 ml Probe 3 ml NaOH (0,1 M). Wie viel mol Essigsäure sind noch vorhanden, wenn der Gesamtansatz 50 ml beträgt?
n(NaOH) pro 2 ml Probe = 0,003 l · 0,1 mol/l = 3·10−4 mol
→ Hochrechnung auf 50 ml: n(CH3COOH) = 3·10−4 · 25 = 7,5·10−3 mol ≈ ⅓ der Ausgangsmenge (erwartet: ⅓ mol)
Weiter im Kapitel Gleichgewichtsreaktionen
← Merkmale eines chemischen Gleichgewichts → Schreibweise und Kollisionsmodell
🔁 Grundlagen aus Klasse 10: Essigsäure / Ethansäure (Kl. 10) · Alkohole / Alkanole (Kl. 10) · Funktionelle Gruppe der Monocarbonsäuren (Kl. 10)
⬇️ Weiter im Kapitel: Prinzip von Le Chatelier · Massenwirkungsgesetz · Ammoniaksynthese
