Was du auf dieser Seite lernst
Du lernst, was die Reaktionsenthalpie ΔH ist und was ein negatives Vorzeichen bedeutet. An drei Beispielreaktionen (NaOH lösen, H₂SO₄ verdünnen, Eisen + Schwefel) werden exotherme Reaktionen und ihre Enthalpiediagramme erklärt. Außerdem wird das Prinzip von Thomson und Berthelot (Energieprinzip) vorgestellt – und seine Grenzen aufgezeigt.
8 Enthalpie – H
8.1 Exotherme Reaktionen und Vorgänge
Einige Beispiele:
a) Natriumhydroxid wird in Wasser gelöst
NaOH(s) + H₂O(l) → Na⁺(aq) + OH⁻(aq) + H₂O(l)
Die Hydrationsenthalpie ist größer als die Gitterenthalpie. → vgl. 7.2 Lösungsenthalpien
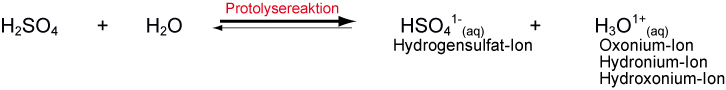
b) Konzentrierte Schwefelsäure wird zu Wasser gegeben
↑ Zum Vergrößern klicken
✕
c) Ein Gemisch aus Eisen und Schwefel wird kurz erhitzt (heißer Draht)
↑ Zum Vergrößern klicken
✕
Auswertung der Versuche
↑ Zum Vergrößern klicken
✕
Bei allen 3 Versuchen wird Energie in Form von Wärme an die Umgebung abgegeben. Die Reaktionen a) und b) laufen spontan ab, die Reaktion c) ist „gehemmt" und muss erst aktiviert werden. Das System verarmt dabei an Energie. Die vom System abgegebene Energie wird mit negativem Vorzeichen angegeben. Reaktionen, bei denen Wärme an die Umgebung abgegeben wird, nennt man exotherm.
Merke: Die Reaktionswärme, die bei konstantem äußerem Druck ausgetauscht wird, bezeichnet man als Reaktionsenthalpie (Symbol ΔH).
Allgemeines Beispiel – Formel zur Enthalpieberechnung:
↑ Zum Vergrößern klicken
✕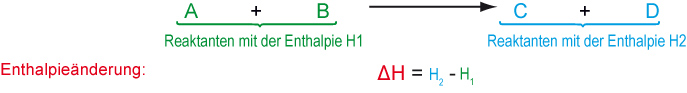
Bei exothermen Reaktionen ist die Reaktionsenthalpie ΔH negativ.
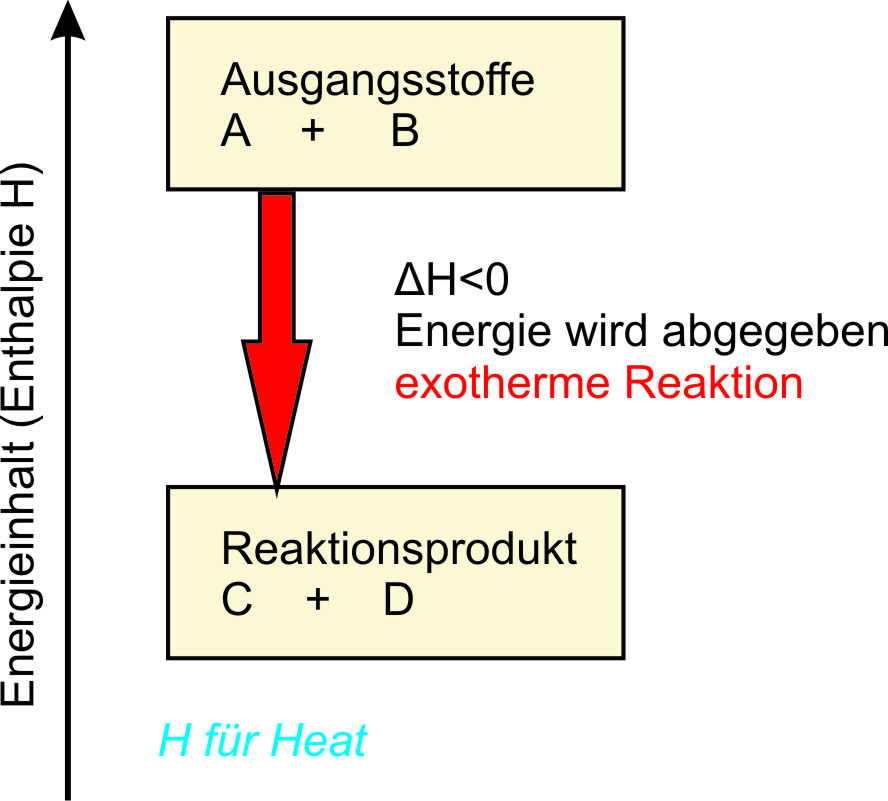
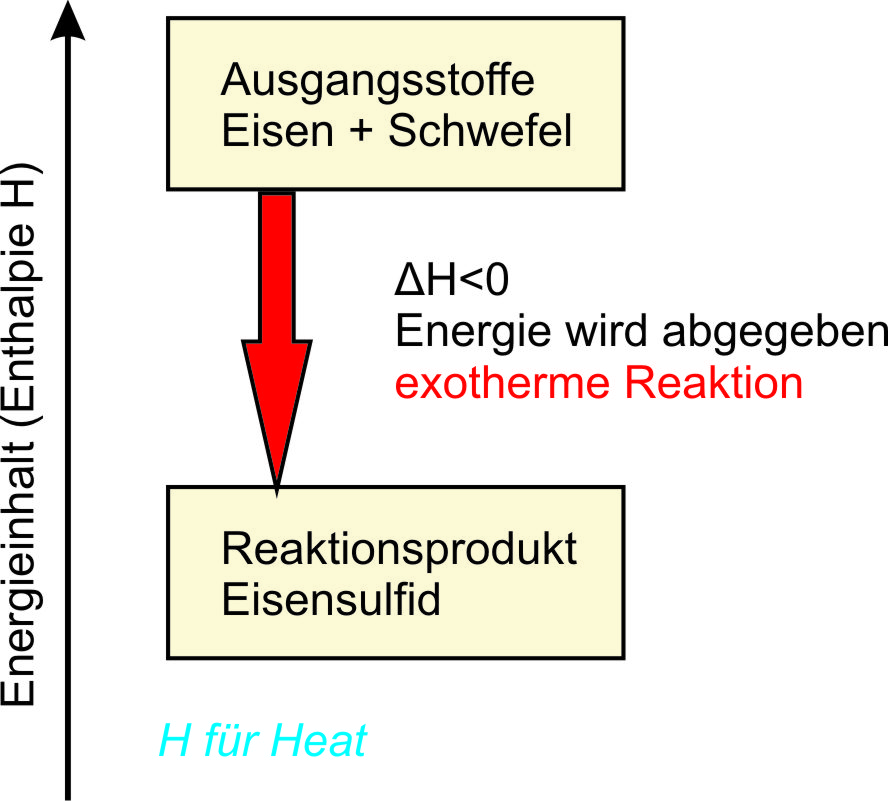
Enthalpieschema (ohne Aktivierungsenergie):
links: allgemeines Schema; rechts: für die Reaktion von Eisen mit Schwefel.
 ✕
✕
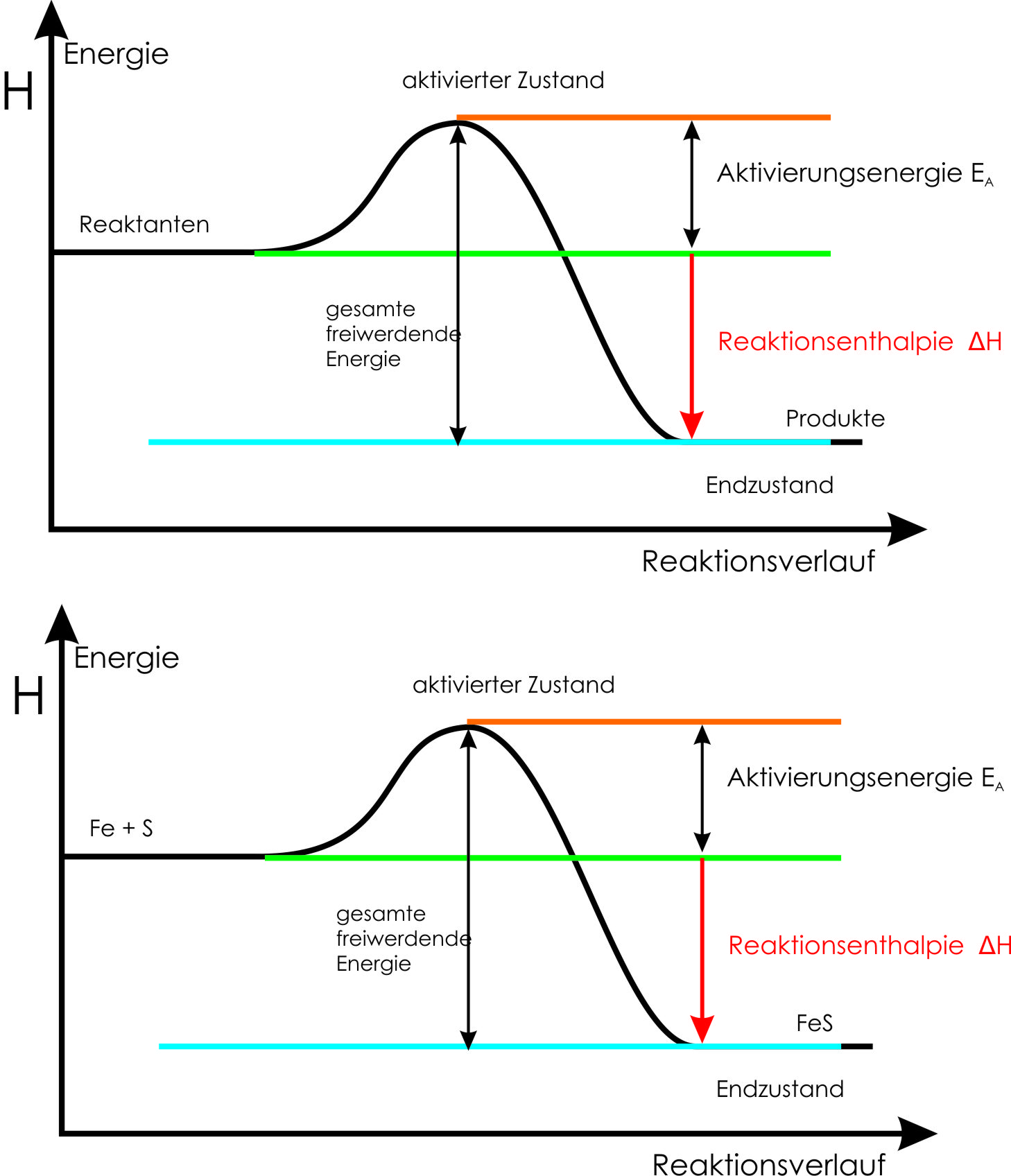
Enthalpieschema mit Reaktionsverlauf und Aktivierungsenergie:
↑ Zum Vergrößern klicken
✕
ΔH < 0 ⇨ exotherme (aber gehemmte) Reaktion (vgl. Metastabile Verbindungen).
Merke: Bei exothermen Vorgängen ist der Endzustand energieärmer als der Ausgangszustand.
Prinzip von Thomson und Berthelot (= Energieprinzip)
Die Wärmetönung stellt ein Maß für die Affinität (Triebkraft) einer chemischen Reaktion dar. Es laufen die Prozesse (Vorgänge, Reaktionen) ab, die zu einem energieärmeren Zustand führen.
Andere Formulierung: Die Systeme streben einem Minimum an Enthalpie entgegen (bei konstantem Druck).
Achtung: Diese Aussage trifft jedoch nur bei einseitig verlaufenden Reaktionen zu; sie steht im Widerspruch zu Gleichgewichtsreaktionen, die in bestimmten Zustandsbereichen auch im entgegengesetzten Sinne erfolgen. Eine vollständige Beschreibung der Reaktionstendenz liefert erst die Gibbs-Energie ΔG, die neben ΔH auch die Entropie ΔS berücksichtigt.
Auf einen Blick – die wichtigsten Aussagen
Reaktionsenthalpie ΔH
ΔH = H(Produkte) − H(Edukte). Bei konstantem äußerem Druck entspricht ΔH der ausgetauschten Reaktionswärme Q.
Exotherm: ΔH < 0
Wärme wird abgegeben. Der Endzustand ist energieärmer als der Ausgangszustand. Die Umgebung erwärmt sich.
Aktivierungsenergie
Auch exotherme Reaktionen können „gehemmt" sein und benötigen eine Zündenergie (z. B. Fe + S). ΔH beschreibt nur die Bilanz, nicht den Reaktionsweg.
Energieprinzip (Grenzen)
Thomson & Berthelot: Reaktionen streben Enthalpie-Minimum an – gilt nur für einseitige Reaktionen. Vollständig: ΔG = ΔH − T·ΔS.
Häufige Fragen zur Reaktionsenthalpie
Was ist die Reaktionsenthalpie ΔH und wie ist sie definiert?
Die Reaktionsenthalpie ΔH gibt die Wärmemenge an, die ein chemisches System bei konstantem äußerem Druck mit der Umgebung austauscht. Es gilt: ΔH = H(Produkte) − H(Edukte). Da die absolute Enthalpie H nicht messbar ist, interessiert nur die Differenz ΔH. → Mehr unter 3. Innere Energie U und 4. Volumenarbeit W.
Was bedeutet ein negatives Vorzeichen von ΔH?
ΔH < 0 bedeutet: Das System gibt Wärme ab (exotherm). Die Produkte befinden sich auf einem niedrigeren Energieniveau als die Edukte. Die Differenz wird als Wärme an die Umgebung abgegeben, was eine Temperaturerhöhung der Umgebung verursacht. Beispiele: Verbrennung, Neutralisation, Lösen von NaOH.
Warum muss man Fe + S erst zünden, obwohl die Reaktion exotherm ist?
Obwohl ΔH < 0 (die Reaktion ist energetisch begünstigt), muss zunächst eine Aktivierungsenergie EA aufgewendet werden, um die Reaktion zu starten. Erst wenn genug Teilchen diese Energiebarriere überwinden, läuft die Reaktion selbstständig weiter. Solche Reaktionen nennt man gehemmt oder metastabil. Vgl. auch Wasserstoff + Sauerstoff (Knallgas) oder die Verbrennung von Holz.
Was besagt das Prinzip von Thomson und Berthelot – und warum ist es unvollständig?
Das Prinzip besagt, dass Reaktionen ablaufen, die zu einem energieärmeren Zustand führen (Streben nach minimalem ΔH). Dies erklärt viele exotherme Reaktionen korrekt. Es versagt aber bei endothermen Reaktionen, die trotzdem spontan ablaufen (z. B. Lösen von KNO₃, Schmelzen von Eis). Der Grund: Neben der Enthalpie spielt auch die Entropie ΔS eine Rolle. Die vollständige Beschreibung liefert die Gibbs-Energie ΔG = ΔH − T·ΔS.
Wie liest man ein Enthalpiediagramm?
Die y-Achse zeigt die Enthalpie H (in kJ/mol). Edukte und Produkte liegen auf unterschiedlichen Niveaus. Bei exothermen Reaktionen liegen die Produkte tiefer. Die Differenz der Niveaus entspricht |ΔH|. Das Diagramm mit Aktivierungsenergie zeigt zusätzlich den Übergangszustand (‚Energieberg') als Hochpunkt der Kurve. ΔH beschreibt nur die Bilanz zwischen Start und Ziel, nicht den Weg dazwischen.
Lernkarten – Enthalpie und exotherme Reaktionen
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist die Reaktionsenthalpie ΔH und bei welcher Bedingung ist sie definiert?
ΔH = H(Produkte) − H(Edukte)
Definiert bei konstantem äußerem Druck. ΔH entspricht der ausgetauschten Reaktionswärme Qp.
Was bedeutet ΔH < 0? Nenne ein Beispiel aus dem Unterricht.
ΔH < 0 → exotherm: Das System gibt Wärme ab. Beispiel: Fe(s) + S(s) → FeS(s), ΔH < 0 (nach Zündung selbstständig).
Was ist der Unterschied zwischen dem Enthalpieschema ohne und mit Aktivierungsenergie?
Ohne EA: Nur Edukt- und Produktniveau mit ΔH.
Mit EA: Zusätzlich der Übergangszustand (Energieberg). ΔH bleibt gleich, zeigt nur Bilanz.
Was besagt das Energieprinzip von Thomson & Berthelot – und wo versagt es?
Reaktionen streben ein Enthalpie-Minimum an. Versagt bei endothermen spontanen Reaktionen (z. B. KNO₃ lösen, Eis schmelzen) → Entropie fehlt. Vollständig: ΔG = ΔH − T·ΔS.
🔢 Bei der Reaktion 2 H₂(g) + O₂(g) → 2 H₂O(l) werden 572 kJ freigesetzt. Wie groß ist ΔH pro Mol H₂O? Exo- oder endotherm?
ΔH(gesamt) = −572 kJ (Wärme wird abgegeben → negatives Vorzeichen)
Pro Mol H₂O: ΔH = −572 kJ / 2 = −286 kJ/mol
→ exotherm
Weiter im Kapitel Energetik
← 7.2 Neutralisationsenthalpie → 8.2 Endotherme Reaktionen 5. Reaktionswärme Q 8.6 Satz von Hess 11. Entropie S 12. Gibbs-Energie G
