Was du auf dieser Seite lernst
Jeder Stoff trägt Energie in sich – als Schwingungs-, Bindungs- oder Kernenergie. Diese innere Energie U ist eine Zustandsgröße: ihr aktueller Wert hängt nicht davon ab, wie das System in diesen Zustand gelangte. Messbar ist nur die Änderung ΔU = Q + W (Wärme + Arbeit).
3 Innere Energie – U
Jeder Stoff hat in sich Energie in irgendeiner Form gespeichert = Innere Energie U,
äußere Energie = potenzielle Energie (wie z.B. Bügeleisen auf dem Schrank) + kinetische Energie (z.B. das Bügeleisen fliegt runter) ⇨ spielt keine Rolle für chemische Reaktionen.
Man unterscheidet vereinfacht:
- den physikalisch-thermischen (Bsp.: Rotationsenergie, Schwingungsenergie), Uth
- den chemischen (die potentielle Energie der Bindungskräfte bzw. die Bindungsenergie) Uch und
- den kernphysikalischen (potentielle Energie, die in den Atomkernen vorhanden) UK
.....Anteil der inneren Energie (U = UK + Uch + Uth)
Es lässt sich kein Absolutbetrag U stofflicher Systeme angeben, da sich kein Energienullpunkt festlegen lässt. Bestimmbar sind nur Änderungen der inneren Energie ΔU
↑ Zum Vergrößern klicken
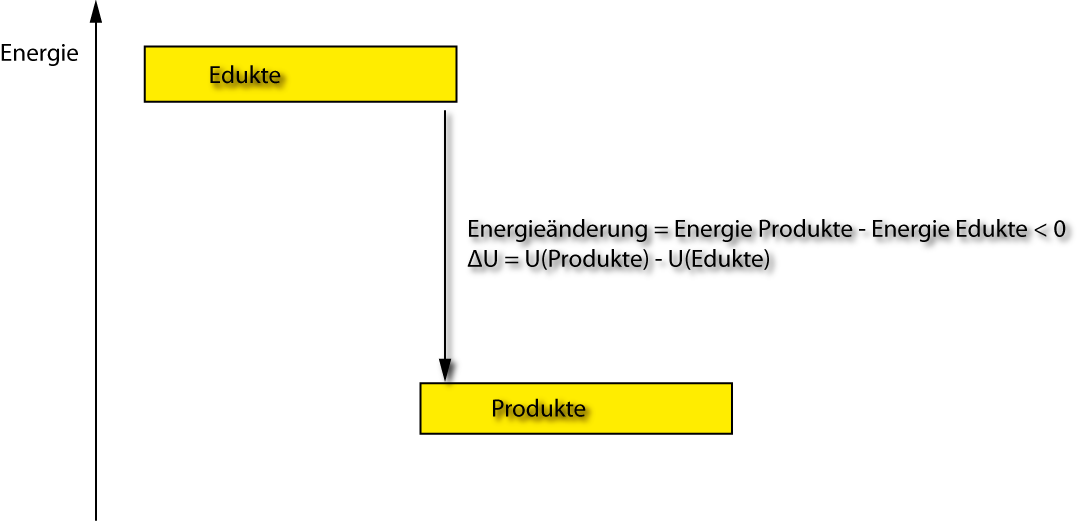
ΔU = U₂ – U₁
ΔU > 0 : Energie wird aufgenommen
ΔU < 0 : Energie wird abgegeben
U₂: Summe der inneren Energien der Produkte
U₁: Summe der inneren Energien der Reaktanden (Edukte)
Änderung der inneren Energie = Wärme + Arbeit
ΔU = U₂ – U₁ = Q + W
Innere Energie = Zustandsgröße
Zustandsgrößen: in einem bestimmten Zustand hat die Zustandsgröße einen bestimmten Wert. Dabei ist es egal, wie man diesen Zustand erreicht hat, also welchen Weg dafür beschritten hat.
Bsp.: Für die momentane potentielle Energie einer Person auf einem Berggipfel (Zustandsgröße) ist es gleichgültig, auf welchem Weg die Person den Gipfel erreicht hat. Die aufgewendete Arbeit hingegen, die die Person aufbringen muss, um diese potentielle Energie zu erreichen, hängt natürlich vom zurückgelegten Weg ab.
Zustandsgrößen: Volumen, Druck, Temperatur sind unabhängig von der Vorgeschichte des Systems (ob es vorher 50°C oder 20°C war).
Die Arbeit ist bei chemischen Reaktionen meistens Volumenarbeit.
Auf einen Blick – die wichtigsten Aussagen
Definition
U = gesamte gespeicherte Energie eines Stoffes: UK + Uch + Uth
Messbarkeit
Kein Absolutwert messbar – nur die Änderung ΔU ist bestimmbar.
Formel
ΔU = Q + W
Wärme + Arbeit (meist Volumenarbeit)
Zustandsgröße
Der Wert von U hängt nur vom aktuellen Zustand ab – nicht vom Weg dorthin.
Häufige Fragen zur inneren Energie
Was genau ist die innere Energie U?
Die innere Energie U ist die gesamte in einem Stoff gespeicherte Energie. Sie setzt sich zusammen aus dem thermischen Anteil Uth (Schwingungs- und Rotationsbewegungen der Teilchen), dem chemischen Anteil Uch (Bindungsenergie der Moleküle) und dem kernphysikalischen Anteil UK (Energie der Atomkerne). Bei chemischen Reaktionen ist vor allem Uch relevant.
Warum lässt sich kein Absolutwert von U angeben?
Es gibt keinen festlegbaren Energienullpunkt für ein Stoffsystem. Man kann nicht sagen, wie viel Energie ein Stoff „insgesamt" enthält – nur wie viel sich ändert, wenn der Stoff an einer Reaktion beteiligt ist. Deshalb arbeitet die Thermodynamik stets mit der Änderung ΔU = U₂ − U₁.
Was bedeutet ΔU > 0 bzw. ΔU < 0?
Ist ΔU > 0, nimmt das System Energie auf. Ist ΔU < 0, gibt das System Energie ab. Die Vorzeichen-Konvention folgt dem System: Energie hinein ist positiv, Energie heraus ist negativ. Achtung: Den Begriff exotherm verknüpft man in der Chemie üblicherweise mit ΔH < 0 (Enthalpie bei konstantem Druck) – nicht direkt mit ΔU.
Was ist eine Zustandsgröße?
Eine Zustandsgröße hat in einem bestimmten Zustand einen eindeutigen Wert – unabhängig davon, wie dieser Zustand erreicht wurde. Beispiele: Druck, Volumen, Temperatur, innere Energie U. Im Gegensatz dazu sind Wärme Q und Arbeit W Prozessgrößen: sie hängen vom Weg ab.
Wie hängen ΔU, Wärme Q und Arbeit W zusammen?
Nach dem ersten Hauptsatz der Thermodynamik gilt: ΔU = Q + W. Die Änderung der inneren Energie ist die Summe aus zugeführter Wärme Q und geleisteter Arbeit W. Bei chemischen Reaktionen in offenen Gefäßen ist W meist die Volumenarbeit (→ 4 Volumenarbeit).
Lernkarten – Innere Energie U
Klicke auf eine Karte, um die Antwort zu sehen.
Aus welchen drei Anteilen setzt sich die innere Energie U zusammen?
U = UK (kernphysikalisch)
+ Uch (chemisch / Bindungsenergie)
+ Uth (thermisch / Schwingung, Rotation)
Warum kann man den Absolutwert der inneren Energie nicht angeben?
Es gibt keinen festlegbaren Energienullpunkt. Messbar ist nur die Änderung ΔU.
Was bedeuten die Vorzeichen von ΔU?
ΔU > 0 → System nimmt Energie auf
ΔU < 0 → System gibt Energie ab
Achtung: „exotherm/endotherm" bezieht sich auf ΔH (bei konstantem Druck), nicht auf ΔU!
Nenne die Grundformel für die Änderung der inneren Energie.
ΔU = Q + W
(Wärme + Arbeit)
Bei chem. Reaktionen: W meist = Volumenarbeit
Warum ist die innere Energie eine Zustandsgröße?
Weil ihr Wert nur vom aktuellen Zustand des Systems abhängt – nicht davon, auf welchem Weg dieser Zustand erreicht wurde.
Weiter im Kapitel Energetik
← 2 Energieerhaltungssatz → 4 Volumenarbeit W → 8 Enthalpie H ← 1 Systeme