Was du auf dieser Seite lernst
Am zweiten Beispiel Calciumhydroxid vertiefst du das Prinzip der umkehrbaren Reaktionen: Calciumoxid (gebrannter Kalk) reagiert mit Wasser exotherm zu Calciumhydroxid (Löschkalk). Beim Erhitzen läuft die Rückreaktion ab. Du lernst das Protolyseschema für diesen Vorgang und die wichtigsten Anwendungen von Kalk in Alltag und Technik.
Vorheriges Beispiel
Das Prinzip der umkehrbaren Reaktion und das Protolyseschema (Bergab/Bergauf) wurden am ersten Beispiel eingeführt: → 1.1 Beispiel: Ammoniumchlorid
1.2 Beispiel: Calciumhydroxid
Calciumoxid
„gebrannter Kalk"
Calciumhydroxid
„gelöschter Kalk" / „Löschkalk"
Kalkwasser
gesättigte wässrige Lösung
a) Bildung von Calciumhydroxid – „Löschen von gebranntem Kalk"
↑ Zum Vergrößern klicken
✕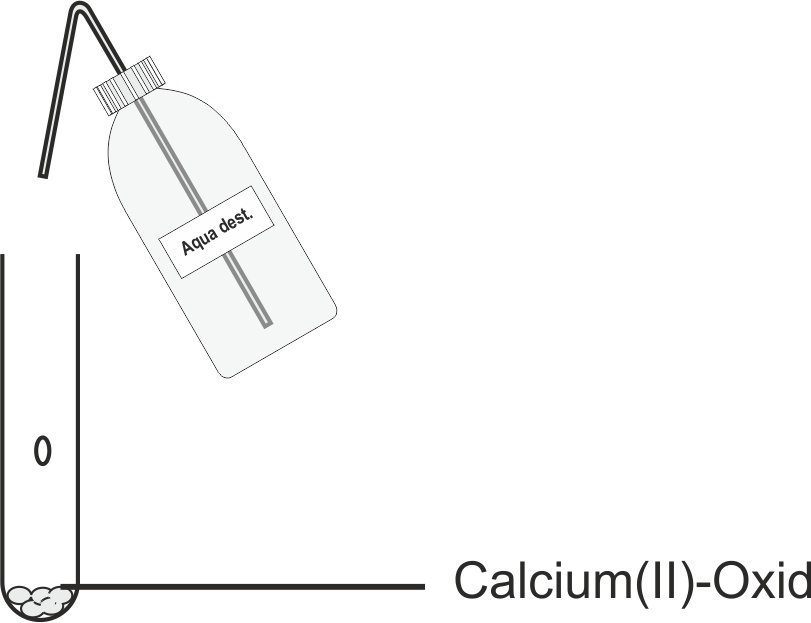
Experiment: Man gibt destilliertes Wasser auf Calciumoxid (CaO, gebrannter Kalk).
Beobachtung:
- Die Reaktion verläuft stark exotherm – der Feststoff wird sehr heiß, zischt und dampft.
- Das Calciumoxid bläht sich auf und zerfällt zu einem weißen, krümeligen Pulver.
- Eine wässrige Lösung (Kalkwasser) ist alkalisch (pH > 7).
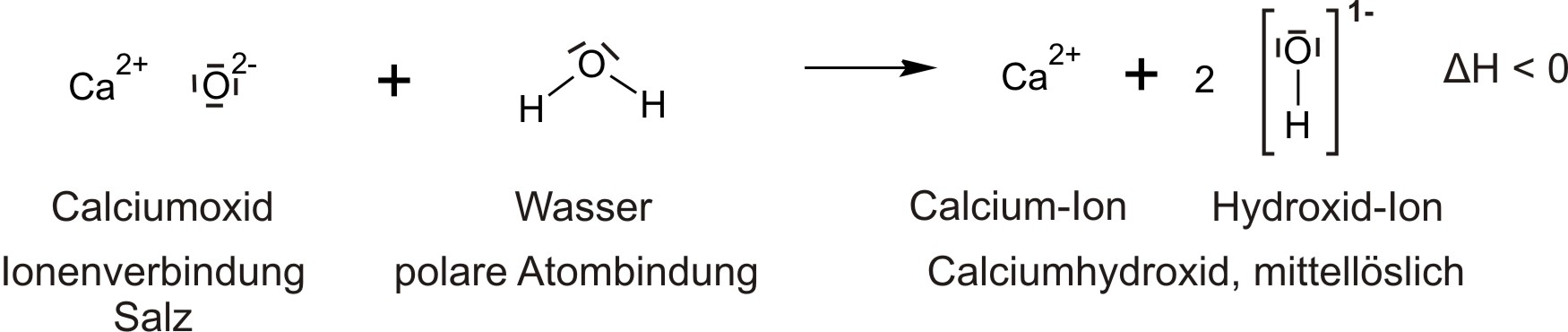
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕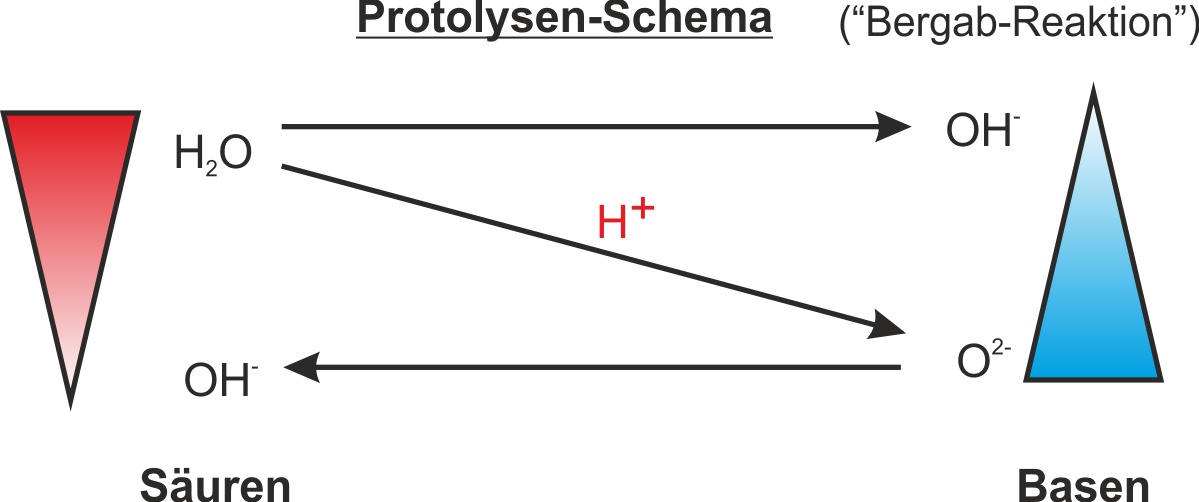
Bergab-Reaktion: Das Oxid-Ion O2− ist eine sehr starke Base – stärker als OH−. Daher überträgt H2O (Säure) ein Proton auf O2− (stärkere Base) → freiwillige, exotherme Reaktion (ΔH < 0).
b) Erhitzen von Calciumhydroxid
Experiment: Man erhitzt festes Calciumhydroxid Ca(OH)₂ stark.
Beobachtung:
- Das Calciumhydroxid zerfällt bei starkem Erhitzen (ab ca. 512 °C) wieder in CaO und H₂O.
- Wasserdampf entweicht.
- Es bleibt weißes Calciumoxid zurück.
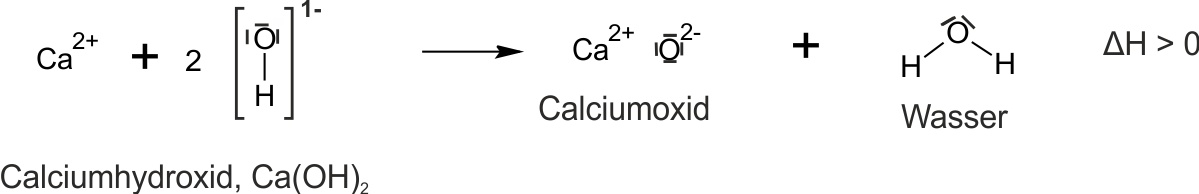
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕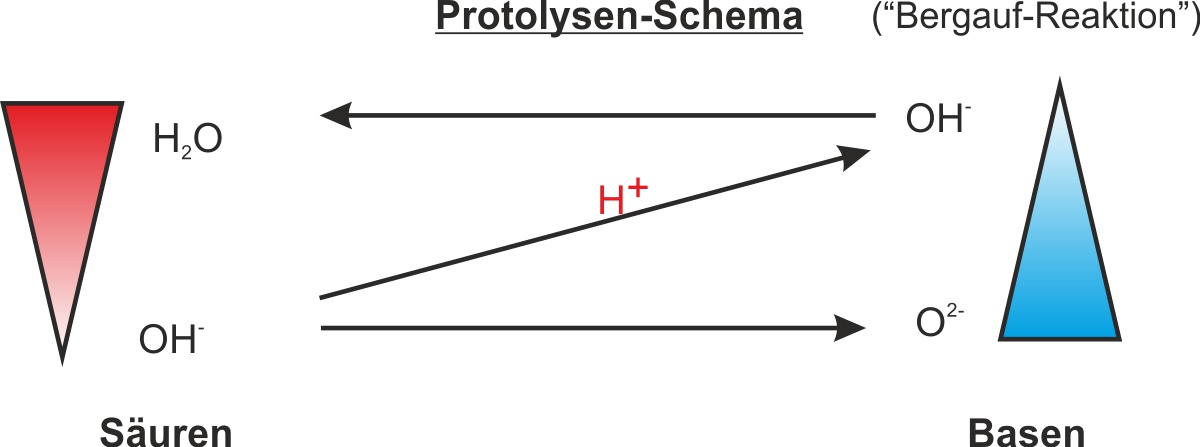
Bergauf-Reaktion: OH− ist eine schwächere Säure als H2O. Um H+ auf ein O2− zu übertragen und so H2O und CaO zurückzubilden, muss Energie (Wärme) zugeführt werden – erzwungene, endotherme Reaktion (ΔH > 0).
c) Bildung und Zerlegung – Zusammenfassung
Calciumoxid + Wasser ⇌ Calciumhydroxid
Anwendungen von Kalk
Calciumoxid und Calciumhydroxid spielen in Technik und Alltag eine große Rolle. Das Verständnis der umkehrbaren Reaktion CaO + H₂O ⇌ Ca(OH)₂ ist der Schlüssel zu diesen Anwendungen.
🏗️ Bauindustrie – Kalkputz & Mörtel
Ca(OH)₂ (Löschkalk) wird zu Mörtel und Kalkputz verarbeitet.
Beim Abbinden reagiert Ca(OH)₂ mit CO₂ der Luft zu festem Calciumcarbonat:
Ca(OH)₂ + CO₂ → CaCO₃ + H₂O
Das ist der „Carbonatisierungsprozess" (Ca(OH)₂ „erhärtet").
🧪 CO₂-Nachweis – Kalkwasser
Kalkwasser (gesättigte Ca(OH)₂-Lösung) trübt sich durch CO₂-Einleiten weiß:
Ca(OH)₂ + CO₂ → CaCO₃↓ + H₂O
CaCO₃ ist schwer löslich und fällt als weißer Feststoff aus.
Klassischer Nachweisreaktion für CO₂!
🌱 Landwirtschaft – Kalkung des Bodens
Saure Böden werden mit gebranntem Kalk (CaO) oder Löschkalk (Ca(OH)₂) gekalkt, um den pH-Wert anzuheben und Nährstoffe verfügbar zu machen.
⚠️ Sicherheitshinweis
Das Löschen von Kalk erzeugt sehr hohe Temperaturen (bis ~300 °C an der Oberfläche). CaO und Ca(OH)₂ sind stark basisch (pH ≈ 12,5) und reizen Augen und Haut – Schutzausrüstung verwenden!
Auf einen Blick – die wichtigsten Aussagen
Kalklöschen
CaO + H2O → Ca(OH)2
Stark exotherm (ΔH ≪ 0), freiwillig
Erhitzen
Ca(OH)2 → CaO + H2O
Endotherm (ΔH > 0), braucht Energie
CO₂-Nachweis
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Kalkwasser trübt sich weiß
O²⁻ – stärkste Base
O2− ist stärkere Base als OH− → Bergab-Protolyse durch H2O
Häufige Fragen – Calciumhydroxid / Kalk
Warum ist die Bildung von Ca(OH)₂ so stark exotherm?
Das Oxid-Ion O2− im CaO ist eine außerordentlich starke Base – stärker als OH−. Es zieht Protonen regelrecht aus Wassermolekülen heraus: O2− + H₂O → 2 OH−. Da diese Protolyse sehr weit „bergab" geht (von einer sehr starken Base zu einer deutlich schwächeren), wird viel Energie frei (ΔH ≪ 0). Sichtbar: Die Masse wird sehr heiß, Wasserdampf entweicht.
Wie unterscheiden sich gebrannter Kalk, Löschkalk und Kalkwasser?
Gebrannter Kalk (Branntkalk, Ätzkalk): CaO – weißer Feststoff, entsteht durch
Brennen von Kalkstein (CaCO₃) bei ca. 900 °C.
Löschkalk (gelöschter Kalk): Ca(OH)₂ – weißes Pulver, entsteht durch Löschen
(Zugabe von Wasser zu CaO).
Kalkwasser: Ca(OH)₂ (aq) – gesättigte wässrige Lösung von Calciumhydroxid,
schwach basisch (pH ≈ 12,5). Dient als CO₂-Nachweis.
Wie funktioniert der CO₂-Nachweis mit Kalkwasser?
Leitet man CO₂ in Kalkwasser ein, entsteht schwer lösliches Calciumcarbonat: Ca(OH)₂ + CO₂ → CaCO₃↓ + H₂O. Das ausgefallene CaCO₃ macht die Lösung milchig trüb – ein einfacher, sicherer Nachweis für Kohlenstoffdioxid. Bei zu viel CO₂ löst sich das CaCO₃ wieder auf (CaCO₃ + CO₂ + H₂O → Ca(HCO₃)₂), die Lösung wird wieder klar.
Warum ist die Zerlegung von Ca(OH)₂ eine Bergauf-Reaktion?
OH− ist eine schwächere Säure als H₂O. Um OH− zur Protonenabgabe zu zwingen und O2− zurückzubilden, muss man Energie (Wärme) zuführen – die Reaktion läuft bergauf im Protolyseschema und ist endotherm (ΔH > 0). Erst oberhalb von ca. 512 °C wird Ca(OH)₂ thermisch zersetzt.
Warum verwendet man Kalk im Bau?
Ca(OH)₂ (Löschkalk) wird mit Sand zu Kalkputz oder -mörtel gemischt. Beim Abbinden (Trocknen) reagiert Ca(OH)₂ mit CO₂ der Luft: Ca(OH)₂ + CO₂ → CaCO₃ + H₂O. Festes Calciumcarbonat (CaCO₃) ist hart und druckfest. Kalkputz ist dampfdiffusionsoffen (reguliert Feuchtigkeit) und fungizid (hemmt Schimmel) durch seinen hohen pH-Wert. Mehr zur Reaktion Säure-Base: Neutralisation (Kursstufe).
Lernkarten – Calciumhydroxid
Klicke auf eine Karte, um die Antwort zu sehen.
Welche Reaktionsgleichung beschreibt das Löschen von Kalk?
CaO + H2O → Ca(OH)2
(stark exotherm, ΔH ≪ 0, freiwillig = Bergab)
Warum reagiert CaO so heftig mit Wasser?
O2− ist eine sehr starke Base – stärker als OH−. Protolyse verläuft sehr weit bergab → große Energiefreisetzung.
Wie weist man CO₂ mit Kalkwasser nach?
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Kalkwasser trübt sich weiß → CO₂ nachgewiesen.
Nenne drei Anwendungen von Kalk.
1. Kalkputz/Mörtel (Bau)
2. CO₂-Nachweis (Kalkwasser)
3. Bodenkalkung (Landwirtschaft)
Aufgabe: Bergab oder Bergauf?
a) CaO + H₂O → Ca(OH)₂
b) Ca(OH)₂ →(Δ) CaO + H₂O
a) Bergab – freiwillig, exotherm, ΔH < 0
b) Bergauf – erzwungen durch Wärme, endotherm, ΔH > 0
Weiter im Kapitel Gleichgewichtsreaktionen
← 1.1 Beispiel: Ammoniumchlorid → 2. Das chemische Gleichgewicht
📌 Weiterführend: Prinzip von Le Chatelier · Säure-Base-Reaktionen in Salzlösungen
