Was du auf dieser Seite lernst
Chemische Reaktionen laufen meist bei konstantem Druck ab – dabei verrichtet das System Volumenarbeit gegen den Atmosphärendruck. Die Formel W = −p · ΔV beschreibt, wie viel Energie dabei übertragen wird, und warum das Vorzeichen negativ ist. Diese Arbeit geht direkt in die Energiebilanz ΔU = Q − p · ΔV ein.
4 Volumenarbeit - W
Def.:
- isobar = gleicher Druck [gr. isos = gleich; barys = schwer]
- isotherm = gleiche Temperatur;
- isochor = gleiches Volumen
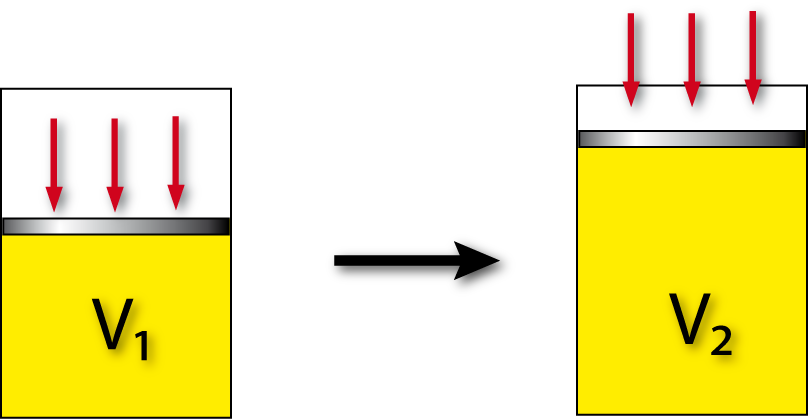
Volumenänderung bei konstanten Druck (= isobar : p = const.):
ΔV = V₂ – V₁
↑ Zum Vergrößern klicken
Ein externer Druck übt eine der Ausdehnung entgegengesetzte Kraft aus. Für uns ist das i.d.R. der Atmosphärendruck (= Konstant) (für ein sich ändernder Außendruck = reversibler Vorgang ist dann die UNI zuständig).
Ist der externe Druck 0 (= Vakuum), wir keine Arbeit verrichtet!
Allgemein:
Vom System abgegebene Energie ⇨ negatives Vorzeichen
Da bei Volumenvergrößerung V₂ – V₁ > 0 vom System Volumenarbeit an die Umgebung abgeführt wird, wird die Volumenarbeit mit einem negativen Vorzeichen definiert.
W = Wmech = - p • ΔV
Bei Volumenabnahme wird dem System Volumenarbeit zugeführt (von der Umgebung)
Herleitung:
Querschnitt des Kolbens: A
Von außen auf den Kolben wirkende Kraft: F = A · p
Wenn der Kolben um eine Wegstrecke s nach außen geschoben wird: ΔV = V₂ – V₁ = A ∙ s
Geleistete Arbeit = Kraft x Strecke = Fläche x Druck x Strecke = Fläche x Strecke x Druck = Volumenänderung x Druck
W = F ∙ s = A ∙ p ∙ s = ΔV ∙ p
ΔU = Q – p ∙ ΔV
Gegendruck = Atmosphärendruck:
101325 Pa = 1013,25 hPa (Hektopascal) = 1,01325 bar = 1013,25 mbar
(= Normalbedingung (T = 0°C); = Standardbedingung (T=25 °C))
1 atm = 1,01325 • 10⁵ Pa = 101 325 Pa
SI-Einheiten:
Druck: 1 Pa (=1 kg/(m•s²) = 1 N/m²)
Auf einen Blick – die wichtigsten Aussagen
Formel
W = −p · ΔV
gilt bei konstantem Druck (isobar)
Vorzeichen
Ausdehnung (ΔV > 0) → System gibt Energie ab → W negativ
Sonderfall Vakuum
p = 0 → W = 0
Keine Arbeit wird verrichtet
Energiebilanz
ΔU = Q − p · ΔV
Wärme minus Volumenarbeit
Häufige Fragen zur Volumenarbeit
Was ist Volumenarbeit und wann tritt sie auf?
Volumenarbeit tritt auf, wenn ein System sein Volumen gegen einen äußeren Druck ändert – z. B. wenn bei einer chemischen Reaktion Gase entstehen und den Kolben eines Gefäßes nach außen drücken. In der Laborchemie ist dieser äußere Druck meist der konstante Atmosphärendruck (isobarer Prozess). Die geleistete Arbeit ergibt sich aus Kraft mal Strecke, was sich vereinfacht zu W = −p · ΔV zusammenfassen lässt.
Warum ist das Vorzeichen der Volumenarbeit negativ?
Die Vorzeichen-Konvention folgt dem System: Energie, die das System abgibt, erhält ein negatives Vorzeichen. Bei einer Ausdehnung (ΔV > 0) drückt das System den Kolben nach außen und leistet dabei Arbeit an der Umgebung – es verliert also Energie. Daher: W = −p · ΔV < 0. Umgekehrt gilt: Bei Kompression (ΔV < 0) wird dem System von außen Arbeit zugeführt, W wird positiv.
Was passiert bei Außendruck = 0 (freie Expansion ins Vakuum)?
Ist der äußere Druck null – zum Beispiel bei Expansion in ein Vakuum – dann gilt W = −0 · ΔV = 0. Es wird keine Arbeit verrichtet, egal wie groß die Volumenänderung ist. Das System dehnt sich aus, ohne Energie abzugeben. Dieser Sonderfall spielt in der Laborpraxis kaum eine Rolle, ist aber für das konzeptionelle Verständnis wichtig.
Was bedeuten isobar, isotherm und isochor?
Isobar (p = const.) bedeutet konstanter Druck – der häufigste Fall im Labor, da man meist gegen den Atmosphärendruck arbeitet. Isotherm (T = const.) bedeutet konstante Temperatur. Isochor (V = const.) bedeutet konstantes Volumen – in diesem Fall ist ΔV = 0, also W = 0, und die gesamte Energieänderung entspricht der Wärme: ΔU = Q.
Wie hängt Volumenarbeit mit der inneren Energie zusammen?
Aus dem ersten Hauptsatz der Thermodynamik (→ 3 Innere Energie) gilt allgemein ΔU = Q + W. Setzt man die Volumenarbeit W = −p · ΔV ein, ergibt sich ΔU = Q − p · ΔV. Diese Beziehung ist die Grundlage für den Begriff der Enthalpie H, die bei isobaren Prozessen besonders praktisch ist (→ 8 Enthalpie).
Lernkarten – Volumenarbeit W
Klicke auf eine Karte, um die Antwort zu sehen.
Wie lautet die Formel der Volumenarbeit bei konstantem Druck?
W = −p · ΔV
mit ΔV = V₂ − V₁
gilt für isobare Prozesse (p = const.)
Warum trägt die Formel ein negatives Vorzeichen?
Bei Ausdehnung (ΔV > 0) gibt das System Energie an die Umgebung ab.
Energieabgabe = negativ (Systemsicht).
Was bedeutet isobar, isotherm, isochor?
🔵 isobar → p = const. (gleicher Druck)
🟡 isotherm → T = const. (gleiche Temperatur)
🟢 isochor → V = const. (gleiches Volumen)
Wie viel Volumenarbeit wird bei Expansion ins Vakuum verrichtet?
W = 0
Da p = 0: W = −0 · ΔV = 0
Keine Arbeit trotz Volumenänderung.
Wie lautet ΔU, wenn Volumenarbeit berücksichtigt wird?
ΔU = Q − p · ΔV
(Wärme minus Volumenarbeit)
Bei isochorem Prozess (ΔV=0): ΔU = Q
Weiter im Kapitel Energetik
← 3 Innere Energie U → 5 Reaktionswärme Q → 8 Enthalpie H ↑ 1 Systeme