Was du auf dieser Seite lernst
Du lernst, was eine Pufferlösung ist, wie sie funktioniert und warum ihr pH-Wert bei Zugabe kleiner Mengen Säure oder Base nahezu konstant bleibt. Am Beispiel des Acetatpuffers wird die Henderson-Hasselbalch-Gleichung hergeleitet. Abschließend lernst du die wichtigsten Puffersysteme im menschlichen Blut kennen.
Grundlagen – Kursstufe Säure-Base
Voraussetzungen für diese Seite: → Henderson-Hasselbalch-Gleichung (4.6.3) · → Indikatoren (Umschlagbereich pKS ± 1) · → Prinzip von Le Chatelier
7. Pufferlösungen
Eine Pufferlösung hält ihren pH-Wert bei Zusatz von nicht zu großen Mengen an Oxonium-Ionen bzw. Hydroxid-Ionen nahezu konstant.
Eine Pufferlösung enthält immer zwei Komponenten:
fängt zugesetzte OH−-Ionen weg
fängt zugesetzte H3O+-Ionen weg
Bedingung: Säure und Base dürfen sich nicht gegenseitig unwirksam machen → daher immer eine schwache Säure mit ihrer konjugierten Base (korrespondierendes Paar).
Beispiel: Acetatpuffer
Man mischt gleiche Volumina Essigsäure (HAc) und Natriumacetatlösung (Na+ Ac−) derselben Konzentration → gleiche Stoffmenge beider Komponenten liegt vor.
pH-Wert dieser Pufferlösung: pH = pKS(HAc) = 4,74
(da c(HAc) = c(Ac−) → lg(1) = 0 in der Henderson-Hasselbalch-Gleichung)
I) Pufferwirkung
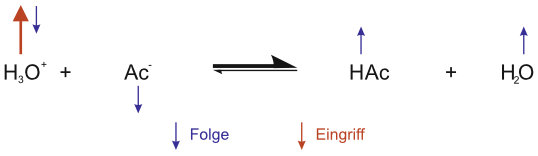
a) Zusatz von H₃O⁺-Ionen (Säurezusatz):
Die zugesetzten H3O+-Ionen werden von der Acetat-Base (Ac−) abgefangen:
↑ Zum Vergrößern klicken
✕
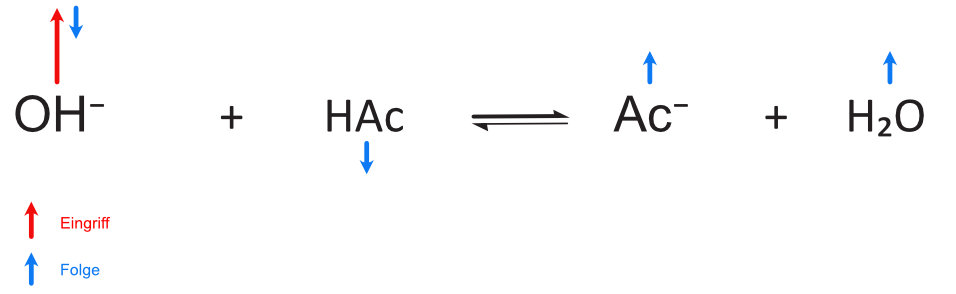
b) Zusatz von OH⁻-Ionen (Basenzusatz):
Die zugesetzten OH−-Ionen werden von der Essigsäure (HAc) abgefangen:
Lösung Wie sieht die Pufferwirkung beim Zusatz von OH−-Ionen aus?
Wenn genügend Ac− bzw. HAc vorhanden sind, reagieren die zugesetzten H3O+- bzw. OH−-Ionen zum größten Teil ab. Dadurch ändert sich das Mengenverhältnis von HAc und Ac− – aber der pH-Wert bleibt nahezu konstant.
II) Änderung des pH-Wertes – Henderson-Hasselbalch-Gleichung
Wie stark ändert sich der pH-Wert, wenn das Mengenverhältnis HAc : Ac− durch den Puffervorgang verschoben wird?
HAc + H2O ⇌ H3O+ + Ac−
Herleitung der Henderson-Hasselbalch-Gleichung für den Acetatpuffer:
↑ Zum Vergrößern klicken
✕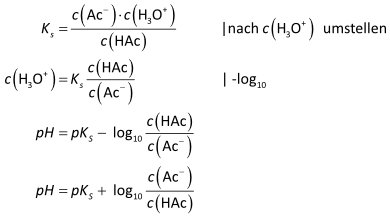
Henderson-Hasselbalch-Gleichung (Puffergleichung):
pH = pKS + lg (c(Ac−) / c(HAc))
Beim Mengenverhältnis HAc : Ac− = 1 : 1 gilt c(H3O+) = KS, also pH = pKS.
Pufferbereich: Gute Pufferwirkung besteht nur, wenn das Konzentrationsverhältnis
von Säure und Base nicht größer als 10 : 1 oder 1 : 10 ist.
Das entspricht dem pH-Bereich: pH = pKS ± 1.
Außerhalb dieses Bereichs ist der Puffer erschöpft.
7.1 Puffersysteme im menschlichen Blut
Ohne Puffersysteme würden bereits kleinste Mengen Säure (z. B. Laktat aus dem Muskelstoffwechsel) genügen, um den Organismus ernsthaft zu schädigen: Proteine (z. B. Enzyme, Hämoglobin) denaturieren bei pH-Änderungen außerhalb eines engen Bereichs und verlieren ihre Funktion.
Letal (lebensbedrohlich) nach kurzer Zeit: pH < 7,0 oder pH > 7,7
Die wichtigsten Blutpuffer im Überblick
| Puffersystem | Säure-Komponente | Base-Komponente |
|---|---|---|
| Hydrogencarbonat-/Kohlensäure-Puffer | H2CO3 | HCO3− |
| Hämoglobin-Puffer | Hämoglobin (HHb) | Hämoglobin-Anion (Hb−) |
| Protein-Puffer | Protein (H-Protein) | Proteinat (Protein−) |
| Phosphat-Puffer | H2PO4− | HPO42− |
(I) Hydrogencarbonat-/Kohlensäure-Puffer
Dieser Puffer ist das wichtigste Puffersystem im Blut. Er ist eng mit der Atmung verknüpft, weil CO2 über die Lunge abgeatmet werden kann.
Blut wird alkalischer Formuliere die Reaktionsgleichung, wenn OH−-Ionen zugeführt werden.
H2CO3 + OH− ⇌ HCO3− + H2O
Die Kohlensäure fängt die OH−-Ionen ab → pH bleibt konstant.
Blut wird sauer Formuliere die Reaktionsgleichung, wenn H3O+-Ionen zugeführt werden.
HCO3− + H3O+ ⇌ H2CO3 + H2O ⇌ CO2 + 2 H2O
Das CO2 wird über die Lunge abgeatmet → das Gleichgewicht wird dauerhaft nach rechts gezogen.
Blut wird alkalisch
⇒ Hypoventilation (vermindertes Abatmen)
⇒ mehr CO2 verbleibt im Blut
⇒ Gleichgewicht nach links → pH sinkt wieder
Blut wird sauer
⇒ Hyperventilation (vermehrtes Abatmen)
⇒ mehr CO2 wird abgegeben
⇒ Gleichgewicht nach rechts → pH steigt wieder
Zusätzlich werden bei Ansäuerung des Blutes H3O+-Ionen über den Ammoniak-Puffer abgefangen und renal ausgeschieden:
H3O+ + NH3 ⇌ NH4+ + H2O → Ausscheidung über die Niere
Auf einen Blick – die wichtigsten Aussagen
Pufferprinzip
Schwache Säure + konjugierte Base fangen H3O+ bzw. OH− ab → pH bleibt konstant
Henderson-Hasselbalch
pH = pKS + lg(c(A−)/c(HA))
Bei c(A−) = c(HA): pH = pKS
Pufferbereich
Wirksam nur im Bereich
pH = pKS ± 1
(Verhältnis 1:10 bis 10:1)
Blut-pH
Physiologisch: 7,35–7,45
Letal: < 7,0 oder > 7,7
Wichtigster Puffer: HCO3−/H2CO3
Häufige Fragen – Pufferlösungen
Was ist eine Pufferlösung und warum ändert sich ihr pH-Wert kaum?
Eine Pufferlösung enthält eine schwache Säure und ihre konjugierte Base in vergleichbarer Konzentration. Wird H3O+ zugesetzt, reagiert es mit der Base-Komponente; wird OH− zugesetzt, reagiert es mit der Säure-Komponente. Da jeweils nur das Konzentrationsverhältnis verschoben wird und die Henderson-Hasselbalch-Gleichung pH = pKS + lg(c(A−)/c(HA)) den pH nur logarithmisch mit dem Verhältnis verknüpft, bleibt der pH-Wert trotz Zusatz von Säure oder Base nahezu konstant.
Warum muss ein Puffer aus einem korrespondierenden Säure-Base-Paar bestehen?
Würde man eine starke Säure und eine starke Base mischen, würden sie sich sofort neutralisieren. Ein Puffer braucht eine schwache Säure und ihre konjugierte Base, weil sie miteinander im Gleichgewicht stehen. Wird das Gleichgewicht durch Zugabe von H3O+ oder OH− gestört, verschiebt es sich nach Le Chatelier – aber ohne die große pH-Änderung, die bei einem ungepufferten System auftreten würde.
Warum ist der Pufferbereich auf pH = pKS ± 1 begrenzt?
Nach der Henderson-Hasselbalch-Gleichung ändert sich der pH um 1, wenn das Verhältnis c(A−)/c(HA) von 1:1 auf 10:1 oder 1:10 verschoben wird. Jenseits dieser Grenzen überwiegt eine Komponente stark – die andere ist für weitere Pufferwirkung praktisch erschöpft. Daher ist ein Puffer nur im Bereich pKS ± 1 wirksam.
Wie reguliert das Blut seinen pH-Wert bei Übersäuerung?
Der wichtigste Blutpuffer ist das Hydrogencarbonat/Kohlensäure-System: HCO3− + H3O+ ⇌ H2CO3 ⇌ CO2 + H2O. Das entstehende CO2 wird über die Lunge abgeatmet (Hyperventilation). Außerdem werden H3O+-Ionen über den Ammoniakpuffer (NH3 + H3O+ → NH4+) abgefangen und renal ausgeschieden.
Welchen pH hat der Acetatpuffer, wenn c(HAc) : c(Ac⁻) = 1 : 10 ist?
Henderson-Hasselbalch: pH = pKS(HAc) + lg(c(Ac−)/c(HAc))
= 4,74 + lg(10/1) = 4,74 + 1 = 5,74.
Das entspricht dem oberen Rand des Pufferbereichs (pKS + 1).
Bei noch größerem Verhältnis ist der Puffer erschöpft.
Lernkarten – Pufferlösungen
Klicke auf eine Karte, um die Antwort zu sehen.
Was enthält eine Pufferlösung? Welche Bedingung muss erfüllt sein?
Eine schwache Säure + ihre konjugierte Base (korrespondierendes Paar) in vergleichbarer Konzentration. Sie dürfen sich nicht gegenseitig neutralisieren.
Welchen pH hat ein Acetatpuffer bei gleichen Mengen HAc und Ac−?
c(Ac−) = c(HAc) → lg(1) = 0
→ pH = pKS(HAc) = 4,74
Was passiert, wenn dem Acetatpuffer OH−-Ionen zugesetzt werden?
HAc + OH− → Ac− + H2O
c(HAc) ↓, c(Ac−) ↑ → pH steigt leicht,
bleibt aber innerhalb des Pufferbereichs.
Wie reguliert der Hydrogencarbonatpuffer das Blut bei Hyperventilation?
Mehr CO2 wird abgeatmet → H2CO3-Konzentration sinkt → Gleichgewicht nach rechts → mehr HCO3− → pH steigt → wirkt saurer Blutlage entgegen.
Rechenaufgabe: Acetatpuffer, c(Ac−)/c(HAc) = 5. Wie groß ist der pH?
pH = 4,74 + lg(5)
= 4,74 + 0,70
= 5,44
Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← Säure-Base-Titration ↑ Zusammenfassung Säure-Base 4.6
🔁 Grundlagen: Henderson-Hasselbalch (4.6.3) · Indikatoren (pKS ± 1) · Le Chatelier
