Was du auf dieser Seite lernst
Du lernst, was endotherme Reaktionen sind und warum ihre Reaktionsenthalpie ΔH positiv ist. An drei Schulversuchen (Eisschmelzen, NH₄NO₃ lösen, Ba(OH)₂ + NH₄SCN) wird erklärt, wie das System Wärme aus der Umgebung aufnimmt. Das Enthalpiediagramm zeigt, dass der Endzustand energiereicher als der Ausgangszustand ist.
8.2 Endotherme Reaktionen und Vorgänge
Einige Beispiele:
a) Eis schmilzt
H₂O(s) → H₂O(l)
b) Ammoniumnitrat (oder Ammoniumchlorid) wird in Wasser gelöst
NH₄NO₃(s) + H₂O(l) → NH₄⁺(aq) + NO₃⁻(aq)
Ammoniumnitrat → Ammonium-Ion + Nitrat-Ion
c) Bariumhydroxid und Ammoniumthiocyanat (Ammoniumrhodanid)
Ba(OH)₂ · 8 H₂O(s) + 2 NH₄SCN(s) → Ba²⁺(aq) + 2 SCN⁻(aq) + 2 NH₃(g) + 10 H₂O(l)
Unter Gasentwicklung verflüssigt sich die feste Mischung. Es wird eine starke Abkühlung des Systems beobachtet – das Gemisch kann auf einer feuchten Holzplatte festfrieren.
Auswertung der Versuche:
↑ Zum Vergrößern klicken
Bei allen drei Beispielen wird vom System Wärme aus der Umgebung aufgenommen. Die Umgebung kühlt sich dabei ab. Das System erhöht seinen Energieinhalt. Die vom System aufgenommene Energie wird mit positivem Vorzeichen angegeben. Reaktionen, bei denen Wärme aus der Umgebung aufgenommen wird, nennt man endotherm.
Bei endothermen Reaktionen ist die Reaktionsenthalpie ΔH positiv.
Enthalpiediagramm – allgemeine endotherme Reaktion mit Reaktionsverlauf:
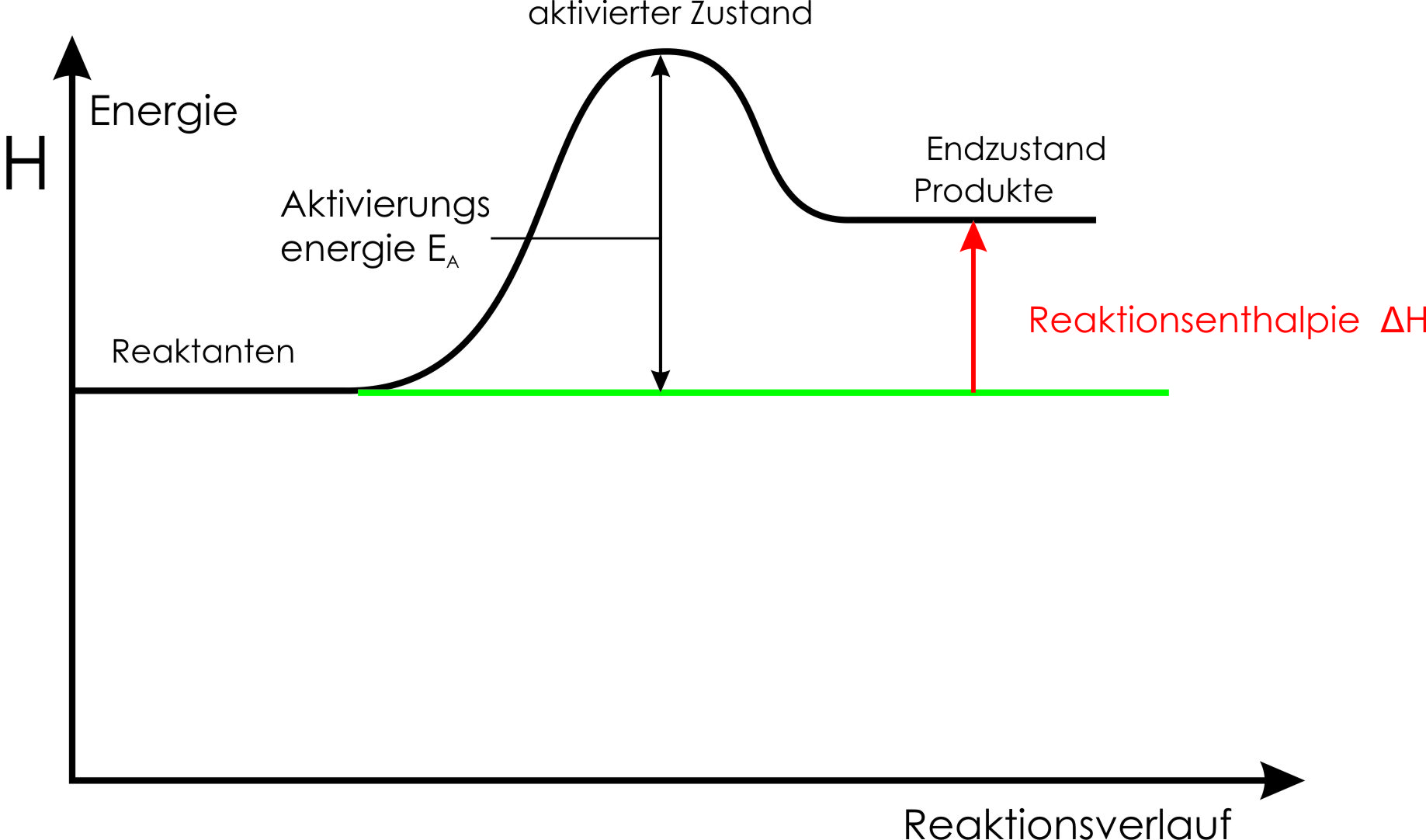
↑ Zum Vergrößern klicken
ΔH > 0 ⇨ endotherme Reaktion
Merke: Bei endothermen Reaktionen (Vorgängen) ist der Endzustand energiereicher als der Ausgangszustand.
Auf einen Blick – die wichtigsten Aussagen
Endotherm: ΔH > 0
Das System nimmt Wärme auf. Die Umgebung kühlt sich ab. Der Endzustand ist energiereicher als der Ausgangszustand.
3 Schulbeispiele
a) Eis schmelzen · b) NH₄NO₃ in Wasser lösen · c) Ba(OH)₂ + NH₄SCN – alle drei kühlen die Umgebung ab.
Enthalpiediagramm
Produkte liegen energetisch höher als Edukte. ΔH = H(Produkte) − H(Edukte) > 0. Pfeil im Diagramm zeigt nach oben.
Spontan trotz ΔH > 0?
Ja – wenn die Entropiezunahme ΔS groß genug ist. Vollständige Triebkraft: ΔG = ΔH − T·ΔS < 0.
Häufige Fragen zu endothermen Reaktionen
Was ist der Unterschied zwischen exo- und endotherm?
Bei exothermen Reaktionen gibt das System Wärme an die Umgebung ab (ΔH < 0), der Endzustand ist energieärmer. Bei endothermen Reaktionen nimmt das System Wärme auf (ΔH > 0), der Endzustand ist energiereicher. Im Enthalpiediagramm liegen die Produkte bei exothermen Reaktionen tiefer, bei endothermen Reaktionen höher als die Edukte. → Vgl. 8.1 Exotherme Reaktionen
Warum ist das Lösen von Ammoniumnitrat endotherm?
Bei der Auflösung muss zunächst der Ionenkristall aufgebrochen werden – dafür ist die Gitterenthalpie aufzuwenden (positiver Energiebeitrag). Die anschließend freiwerdende Hydrationsenthalpie ist bei NH₄NO₃ kleiner als die Gitterenthalpie, sodass per Saldo Energie aufgenommen wird: ΔHsolv > 0. Die Lösung kühlt sich ab. → Vgl. 7.2 Lösungsenthalpien
Was passiert beim Versuch mit Ba(OH)₂ und NH₄SCN genau?
Bariumhydroxid-Octahydrat und Ammoniumthiocyanat reagieren unter Gasentwicklung (NH₃) und starker Abkühlung. Die Temperatur kann auf unter −20 °C fallen – das feuchte Holzbrett, auf dem die Bechergläser stehen, friert fest. Die Reaktion ist endotherm (ΔH ≈ +170 kJ/mol): Das System entzieht der Umgebung so viel Wärme, dass Wasser gefriert. Die Spontaneität erklärt sich durch die große Entropiezunahme (Übergang von Feststoffen zu Ionen, Wasser und Gas): ΔG = ΔH − T·ΔS < 0.
Kann eine endotherme Reaktion spontan ablaufen?
Ja – das Prinzip von Thomson und Berthelot (Enthalpie-Minimum) ist hier nicht ausreichend. Endotherme Reaktionen laufen spontan ab, wenn die Entropiezunahme (ΔS > 0) groß genug ist, um den Enthalpienachteil zu überkompensieren. Die vollständige Triebkraft einer Reaktion beschreibt die Gibbs-Energie: ΔG = ΔH − T·ΔS. Eine Reaktion läuft spontan ab, wenn ΔG < 0.
Woran erkenne ich im Enthalpiediagramm eine endotherme Reaktion?
Die Produkte liegen auf einem höheren Energieniveau als die Edukte. Der Pfeil für ΔH zeigt nach oben. Bei einem Diagramm mit Reaktionsverlauf ist der Endpunkt der Kurve höher als der Startpunkt. Im Vergleich: Bei exothermen Reaktionen liegt der Endpunkt tiefer. Die Aktivierungsenergie (Übergangszustand, Hochpunkt der Kurve) kann bei endothermen Reaktionen kleiner sein als bei exothermen.
Lernkarten – Endotherme Reaktionen
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist eine endotherme Reaktion? Nenne das Vorzeichen von ΔH und was mit der Umgebung passiert.
Das System nimmt Wärme aus der Umgebung auf.
ΔH > 0 (positiv).
Die Umgebung kühlt sich ab. Der Endzustand ist energiereicher als der Ausgangszustand.
Nenne drei Schulbeispiele für endotherme Vorgänge und erkläre kurz, woran man die Endothermie beobachtet.
a) Eis schmelzen: Temperatur bleibt bei 0 °C → Energie wird aufgenommen
b) NH₄NO₃ lösen: Lösung kühlt ab
c) Ba(OH)₂ + NH₄SCN: starke Abkühlung, Brett friert fest
Wie unterscheiden sich exo- und endotherme Reaktionen im Enthalpiediagramm?
Exotherm: Produkte tiefer als Edukte, ΔH-Pfeil nach unten, ΔH < 0
Endotherm: Produkte höher als Edukte, ΔH-Pfeil nach oben, ΔH > 0
Warum kann eine endotherme Reaktion trotzdem spontan ablaufen? Welche Größe entscheidet?
Weil die Entropiezunahme ΔS groß genug sein kann.
Entscheidend ist die Gibbs-Energie:
ΔG = ΔH − T·ΔS < 0 → spontan
Beispiel: Ba(OH)₂ + NH₄SCN
🔢 Beim Lösen von 0,2 mol NH₄NO₃ in Wasser sinkt die Temperatur von 22,0 °C auf 17,5 °C (m = 150 g). Berechne ΔHsolv.
Q = m · c · ΔT = 150 g · 4,18 J/(g·K) · (−4,5 K) = −2821 J
Das System hat +2821 J aufgenommen:
ΔHsolv = +Q/n = +2821 J / 0,2 mol = +14,1 kJ/mol
(endotherm ✓)
Weiter im Kapitel Energetik
← 8.1 Exotherme Reaktionen → 8.3 Standardbildungsenthalpie 7.2 Lösungsenthalpien 8.6 Satz von Hess 11. Entropie S 12. Gibbs-Energie G
