Was du auf dieser Seite lernst
Chlorwasserstoff-Gas (HCl) reagiert mit Wasser zu Oxonium- und Chlorid-Ionen – das ist eine Protolyse-Reaktion nach Brønsted. Du lernst den Springbrunnenversuch zu erklären, Reaktionsgleichungen in Summenformel- und Lewis-Schreibweise aufzustellen und das Protolysen-Schema (Bergab-Reaktion) zu lesen und anzuwenden.
3 Protolyse-Reaktionen
3.1 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
Chlorwasserstoff: Summenformel HCl · polare Atombindung · Gas · stechender Geruch
Wasser: Summenformel H2O · polare Atombindung · Flüssigkeit · geruchslos
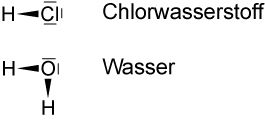
Lewis-Formeln
| H — Cl: | Chlorwasserstoff |
| H — O: | Wasser |
| | | |
| H |
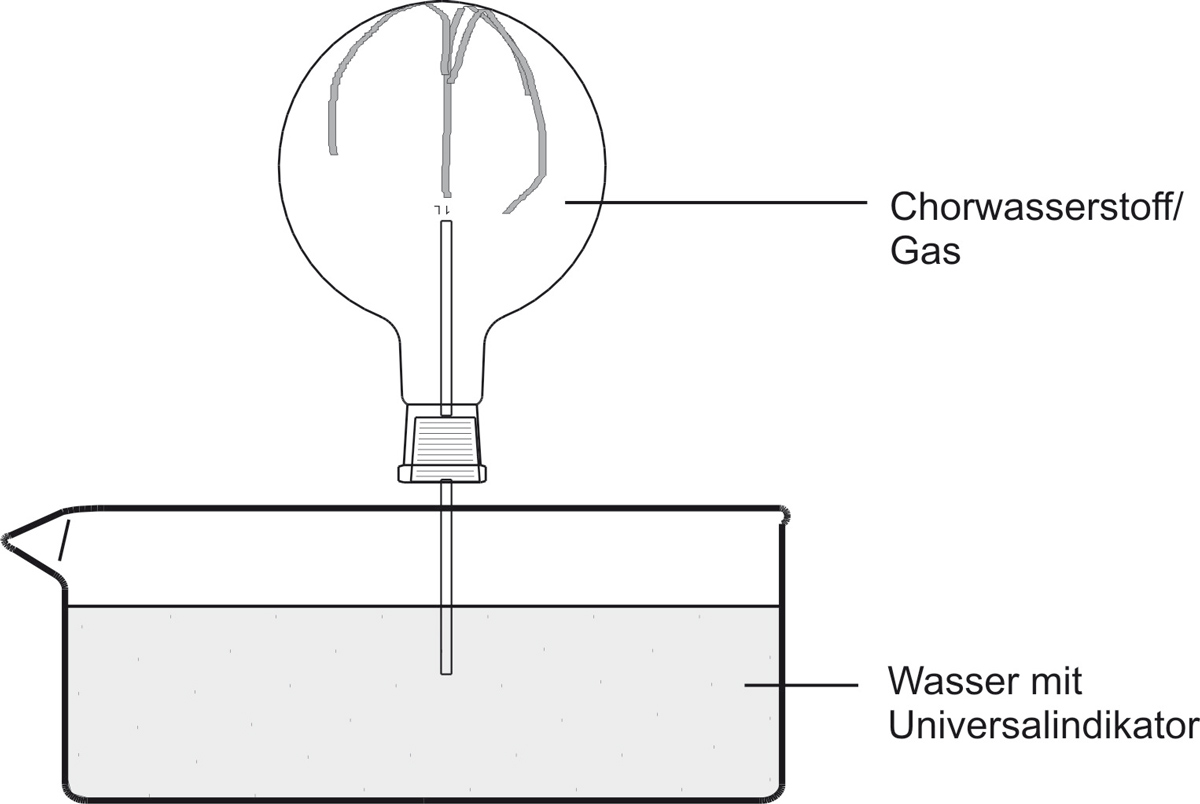
a) Versuch:
↑ Zum Vergrößern klicken
✕
⚠️ Hinweis: Im Bild steht „Chorwasserstoff" – korrekte Schreibweise: Chlorwasserstoff.
b) Beobachtung:
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach rot/gelb um. Die rote wässrige Lösung ist geruchlos.
c) Reaktionsgleichung – Struktur/Lewisformel:
Es gibt zwei mögliche Reaktionsgleichungen (wenn man zunächst die Säurestärke vernachlässigt). Welche zwei Reaktionsgleichungen sind das?
{slider title="Lösung" open="false" class="icon"}1. Möglichkeit – HCl als Säure, H2O als Base (korrekte Reaktion):
H2O(l) + HCl(g) ⟶ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
⇒ bildet zusammen: „Salzsäure"

2. Möglichkeit – H2O als Säure, HCl als Base:
↑ Zum Vergrößern klicken
✕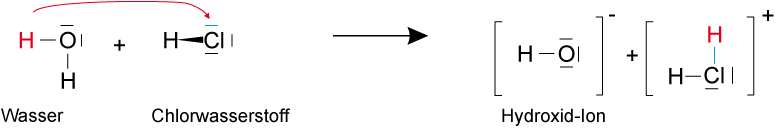
Chlorwasserstoff ist die stärkere Säure, Hydroxid-Ion (OH−) wäre eine sehr starke Base. Durch Elektrolyse wird die 1. Möglichkeit bestätigt: HCl wirkt als Säure.
{/sliders}Nachweis der gebildeten Ionen:
- Leitfähigkeitsmessung: Die Lösung leitet elektrischen Strom → Ionen sind vorhanden.
- Elektrolyse: An der Anode (Pluspol) entsteht Cl2-Gas → Chlorid-Ionen (Cl−) müssen vorliegen.
↑ Zum Vergrößern klicken
✕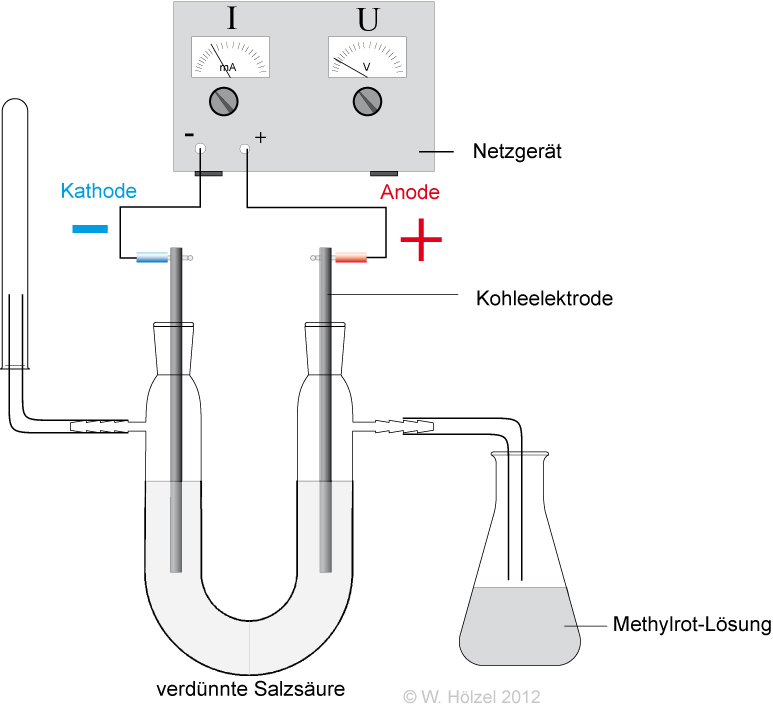
- Indikator: Bromthymolblau färbt gelb → Oxonium-Ionen (H3O+) sind vorhanden.
Komplette Lösung:
{slider title="Lösung" open="false" class="icon"}Reaktionsgleichung (Lewis-Formel):
↑ Zum Vergrößern klicken
✕
Reaktionsgleichung (Summenformel):
H2O(l) + HCl(g) ⇌ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
„Salzsäure"

Verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen sowie Wassermolekule.
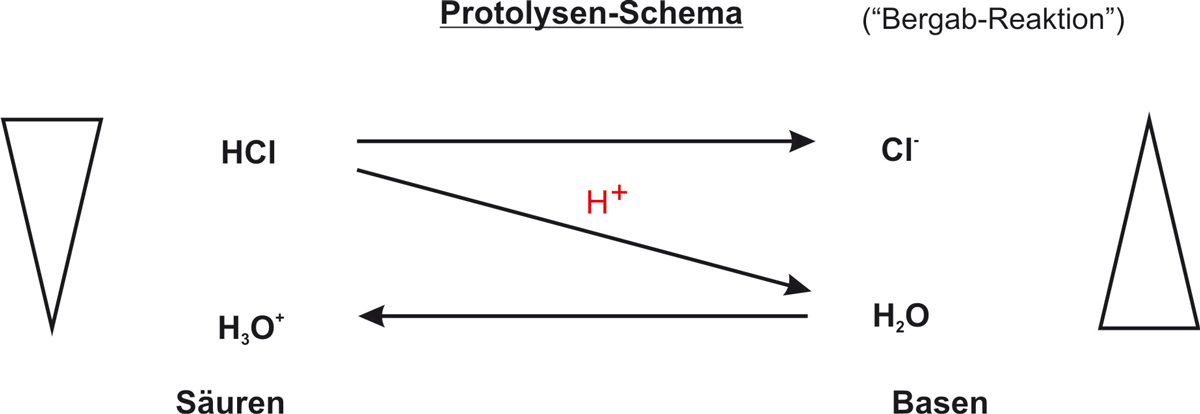
d) Protolysen-Schema:
↗ Originalbild des Protolysen-Schemas ansehen
✕ {/sliders}
{/sliders}
e) Erklärung:
Chlorwasserstoff-Gas reagiert mit Wasser zu Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Im Kolben entsteht durch das vollständige Auflösen ein Unterdruck. Die H3O+-Ionen färben den Universalindikator bzw. Bromthymolblau rot/gelb.
Salzsäure = wässrige Lösung des Gases Chlorwasserstoff
Leitet man sehr viel HCl-Gas in Wasser ein, reagieren nicht mehr alle HCl-Moleküle mit H2O. Diese HCl-Moleküle liegen „gelöst" vor – es entsteht rauchende bzw. konzentrierte Salzsäure.
| Leitfähigkeit | Geruch | Indikatorpapier | Teilchen | |
|---|---|---|---|---|
| Verdünnte Salzsäure | + | − | rot | H2O, H3O+, Cl− |
| Rauchende Salzsäure | + | + | rot | H2O, H3O+, Cl−, HCl |
Auf einen Blick – die wichtigsten Aussagen
Protolyse (Brønsted)
Eine Protolyse ist die Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
Springbrunnen
HCl löst sich vollständig in H2O auf → Ionen bilden sich → Unterdruck entsteht → Atmosphärendruck drückt Wasser hoch.
Bergab-Reaktion
Das Proton wandert von der stärkeren Säure (HCl) zur stärkeren Base (H2O) – immer zur schwächeren Säure/Base hin.
Salzsäure
Salzsäure = wässrige Lösung von HCl. Enthält H3O+, Cl− und H2O; konzentriert zusätzlich gelöstes HCl.
Häufige Fragen – Protolyse-Reaktionen
Warum schießt das Wasser beim Springbrunnenversuch in den Kolben?
HCl-Gas reagiert sofort mit dem eingetretenen Wasser zu H3O+- und Cl−-Ionen. Dadurch sinkt der Gasdruck im Kolben stark. Der Atmosphärendruck drückt das Wasser durch das Glasrohr nach oben – der „Springbrunnen-Effekt". Die Indikatorfarbe zeigt: die Lösung ist sauer (H3O+-Ionen).
Was ist der Unterschied zwischen Chlorwasserstoff und Salzsäure?
Chlorwasserstoff (HCl) ist ein farbloses Gas mit stechendem Geruch. Salzsäure ist die wässrige Lösung dieses Gases: HCl löst sich in H2O und bildet dabei Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Verdünnte Salzsäure ist geruchlos, da kein HCl mehr als Gas vorliegt.
Was versteht man unter einer Protolyse nach Brønsted?
Nach Brønsted ist eine Säure ein Protonendonator (gibt H+ ab) und eine Base ein Protonenakzeptor (nimmt H+ auf). Eine Protolyse ist die Übertragung eines Protons. Das Protolysen-Schema zeigt: Die Reaktion läuft stets von der stärkeren Säure/Base zu den schwächeren Produkten – die sogenannte Bergab-Reaktion. Mehr dazu: Brønsted-Definition (Kl. 9).
Wie weist man Chlorid-Ionen in Salzsäure nach?
Durch Elektrolyse: An der Anode (Pluspol) entwickelt sich Chlorgas (Cl2), das durch Oxidation von Cl− entsteht – direkter Nachweis. Außerdem fällt bei Zugabe von Silbernitrat-Lösung (AgNO3) ein weißer Niederschlag aus Silberchlorid (AgCl) aus.
Was enthält rauchende Salzsäure im Vergleich zu verdünnter Salzsäure?
Verdünnte Salzsäure enthält nur H2O, H3O+ und Cl− – alles HCl hat mit Wasser reagiert. In konzentrierter (rauchender) Salzsäure ist so viel HCl gelöst, dass nicht mehr alle Moleküle mit H2O reagieren können. Sie liegen als undissoziiertes HCl vor → stechender Geruch, „Rauchen" an feuchter Luft. Mehr zur Konzentration: Konzentration von Lösungen (Kl. 9).
Lernkarten – Protolyse von Chlorwasserstoff
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist eine Protolyse-Reaktion nach Brønsted?
Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
Erkläre den Springbrunnenversuch mit HCl!
HCl löst sich schnell in H2O → Ionenbildung → Gasdruck sinkt → Atmosphärendruck drückt Wasser nach oben in den Kolben.
Warum wirkt HCl als Säure und H2O als Base?
HCl ist die stärkere Säure. Im Protolysen-Schema reagiert immer die stärkere Säure mit der stärkeren Base (Bergab-Reaktion).
Welche Teilchen enthält verdünnte vs. rauchende Salzsäure?
Verdünnt: H2O, H3O+, Cl−
Rauchend: zusätzlich gelöstes HCl → stechender Geruch
Berechne: Welche Masse HCl (M = 36,5 g/mol) steckt in 250 mL 0,2-mol/L-Salzsäure?
n = c · V = 0,2 mol/L · 0,25 L = 0,05 mol
m = n · M = 0,05 mol · 36,5 g/mol = 1,825 g
Weiter im Kapitel Säure-Base-Reaktionen
→ 3.2 Chlorwasserstoff und Ammoniak → Brønsted-Definition → Stärke von Säuren und Basen
🔗 Verwandte Themen: pH-Wert und Oxonium-Ionen · Konzentration von Lösungen · Neutralisation
ⓘ Die verlinkten Seiten wurden nicht gegen die aktuelle Sitemap verifiziert – bitte vor dem Veröffentlichen prüfen.
