Was du auf dieser Seite lernst
Diese Seite fasst die wichtigsten pH- und pOH-Formeln für starke und schwache Säuren bzw. Basen zusammen. Außerdem lernst du die Henderson-Hasselbalch-Gleichung kennen, die pH-Berechnung in Pufferlösungen und beim Indikator-Umschlagspunkt ermöglicht.
Grundlagen – Kursstufe Säure-Base
Diese Seite fasst die Abschnitte 4.1–4.5 zusammen: → pKS-Wert · → pKB-Wert · → pH-Wert starker und schwacher Säuren · → Salzlösungen
4.6 Zusammenfassung: pH-Wert und Basenstärke
4.6.1 pH-Wert unterschiedlich starker Säuren
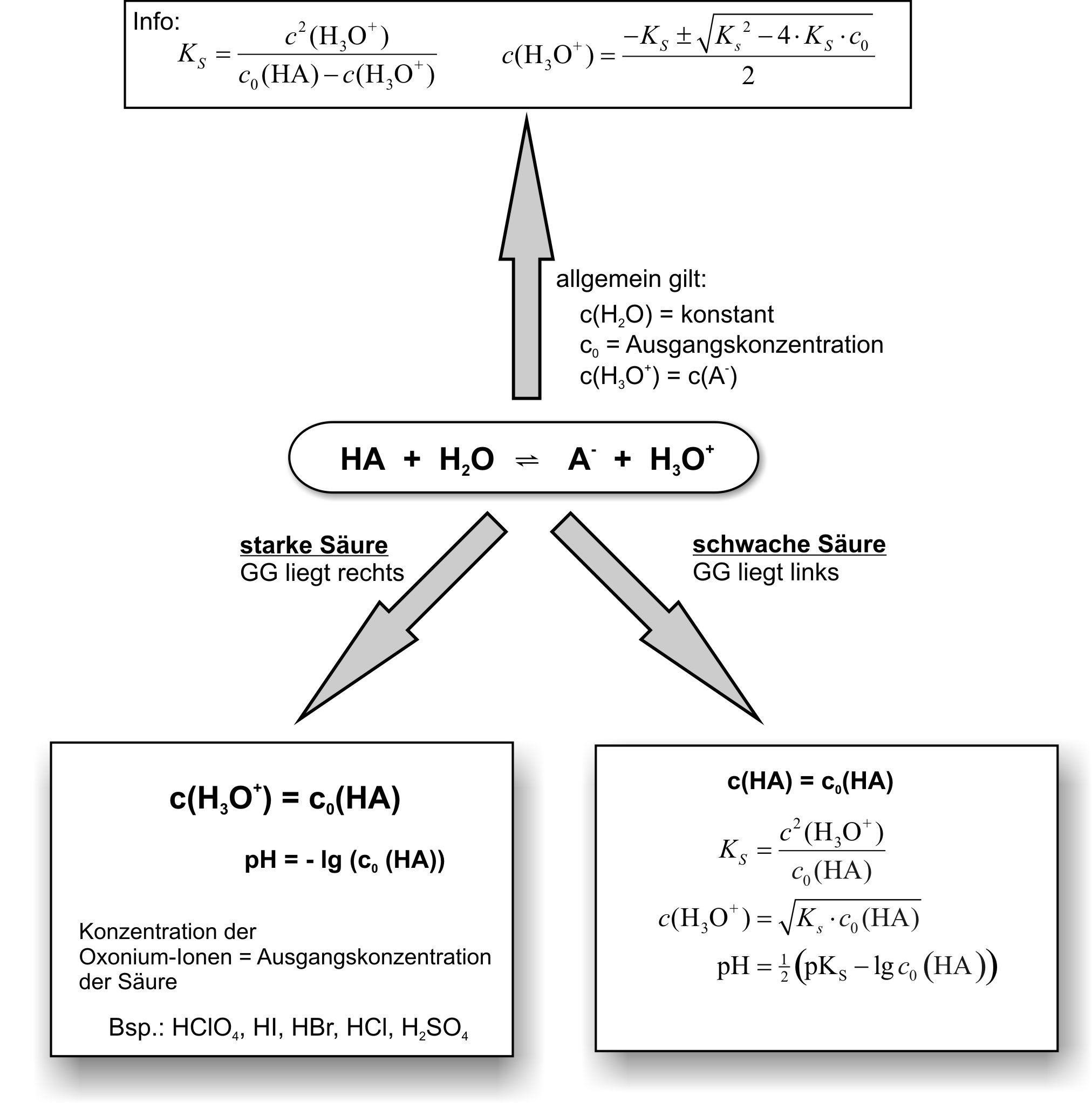
Die folgende Übersicht zeigt, welche Formel man für den pH-Wert einer Säurelösung verwendet – abhängig davon, ob es sich um eine starke oder schwache Säure handelt:
↑ Zum Vergrößern klicken
✕
Erläuterung zum Schema
Ausgangspunkt ist immer die allgemeine Protolysereaktion:
HA + H2O ⇌ A− + H3O+
mit den allgemeinen Vereinfachungen: c(H2O) = konst., c₀ = Ausgangskonzentration, c(H3O+) = c(A−).
Je nach Lage des Gleichgewichts ergeben sich zwei Fälle:
Starke Säure – GG liegt rechts
Vollständige Reaktion → c(H3O+) = c₀(HA)
pH = −lg c₀(HA)
Bsp.: HClO4, HI, HBr, HCl, H2SO4
Schwache Säure – GG liegt links
Näherung c(HA) ≈ c₀(HA):
pH = ½ · (pKS − lg c₀)
Gilt wenn c₀ ≫ c(H3O+), d. h. Protolysegrad < ~5 %
Allgemeine exakte Lösung (wenn die Näherung nicht zulässig ist):
Aus KS = c²(H3O+) / [c₀(HA) − c(H3O+)]
folgt die quadratische Gleichung x² + KS·x − KS·c₀ = 0
→ c(H3O+) = (−KS + √(KS² + 4·KS·c₀)) / 2
(nur positive Lösung)
4.6.2 pOH-Wert unterschiedlich starker Basen
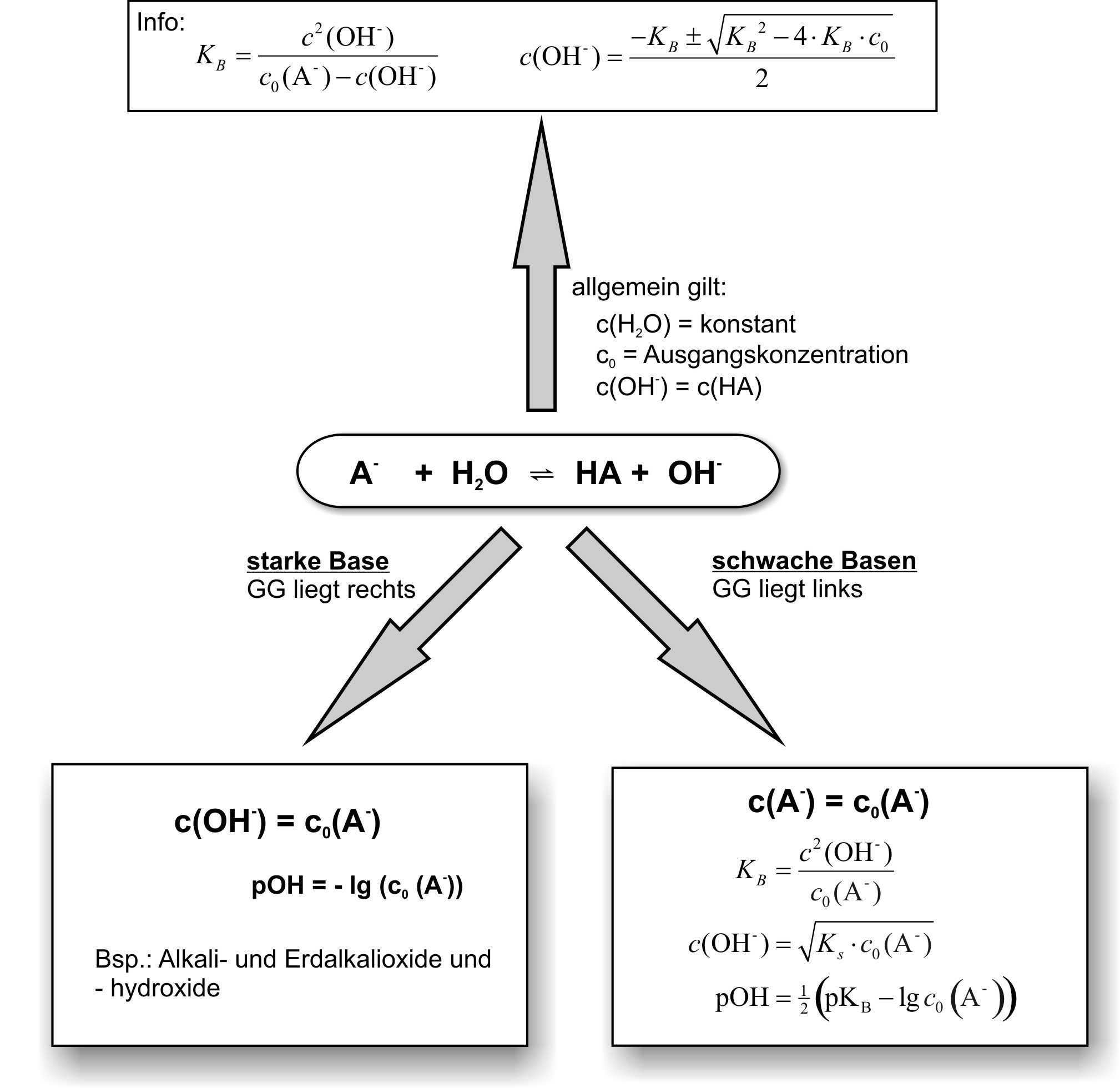
Das Schema für Basen ist vollständig analog zum Säuren-Schema – man ersetzt lediglich c(H3O+) durch c(OH−), pH durch pOH, HA durch A− (die Base) und KS durch KB. Den pH-Wert erhält man anschließend über pH = 14 − pOH.
↑ Zum Vergrößern klicken
✕
Erläuterung zum Schema
Ausgangspunkt ist die allgemeine Protolyse einer Base:
A− + H2O ⇌ HA + OH−
mit c(OH−) = c(HA) als Vereinfachung (analog zur Säure).
Starke Base – GG liegt rechts
Vollständige Reaktion → c(OH−) = c₀(A−)
pOH = −lg c₀(A−)
pH = 14 − pOH
Bsp.: Alkali- und Erdalkalioxide und -hydroxide (NaOH, KOH, Ca(OH)2)
Schwache Base – GG liegt links
Näherung c(A−) ≈ c₀(A−):
pOH = ½ · (pKB − lg c₀)
pH = 14 − pOH
Bsp.: NH3, Acetat−, Carbonat2−
Allgemeine exakte Lösung:
KB = c²(OH−) / [c₀(A−) − c(OH−)]
→ quadratische Gleichung
→ c(OH−) = (−KB + √(KB² + 4·KB·c₀)) / 2
4.6.3 Henderson-Hasselbalch-Gleichung
Aus dem Massenwirkungsgesetz für die Protolyse einer schwachen Säure HA lässt sich eine besonders nützliche Formel ableiten, die den pH-Wert direkt aus den Konzentrationen der Säure HA und ihrer konjugierten Base A− berechnet:
↑ Zum Vergrößern klicken
✕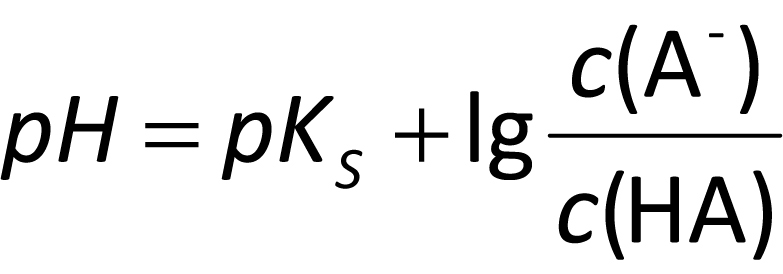
pH = pKS + lg (c(A−) / c(HA))
Die Gleichung hat zwei besonders wichtige Anwendungen:
Indikator-Umschlag
Am Umschlagspunkt eines Indikators gilt c(A−) = c(HA),
also lg(1) = 0 → pH = pKS.
Der Umschlag findet im Bereich pKS ± 1 statt.
Mehr dazu: Indikatoren
Pufferlösungen
In einem Puffer liegen schwache Säure und ihre konjugierte Base nebeneinander vor. Die Henderson-Hasselbalch-Gleichung berechnet direkt den pH aus dem Konzentrationsverhältnis. Im Puffer-Optimum: c(A−) = c(HA) → pH = pKS. Mehr dazu: Pufferlösungen
Herleitung: KS = c(H3O+) · c(A−) / c(HA) → c(H3O+) = KS · c(HA)/c(A−) → −lg: pH = pKS + lg(c(A−)/c(HA))
Auf einen Blick – die wichtigsten Formeln
Starke Säure
pH = −lg c₀(HA)
Vollständige Protolyse
Schwache Säure
pH = ½·(pKS − lg c₀)
Näherung: c(HA) ≈ c₀
Schwache Base
pOH = ½·(pKB − lg c₀)
→ pH = 14 − pOH
Henderson-Hasselbalch
pH = pKS + lg(c(A−)/c(HA))
Puffer & Indikatoren
Häufige Fragen – Formeln und Zusammenfassung
Woran erkenne ich, ob ich die einfache oder die quadratische Formel verwenden muss?
Die Näherungsformel pH = ½·(pKS − lg c₀) gilt, wenn das Gleichgewicht weit auf der linken Seite liegt, d. h. wenn c₀(HA) ≫ c(H3O+). Als Faustregel: Die Näherung ist zulässig, wenn c₀/KS > 100 (bzw. der Protolysegrad < ~5 %). Ist die Säure zu stark oder die Konzentration zu gering, muss man die quadratische Gleichung x² + KS·x − KS·c₀ = 0 lösen.
Was ist der Unterschied zwischen pOH und pH – und wie hängen sie zusammen?
pH = −lg c(H3O+) beschreibt die Säurestärke einer Lösung, pOH = −lg c(OH−) die Basenstärke. Aus der Autoprotolyse des Wassers folgt bei 25 °C immer: pH + pOH = 14. Für Basen berechnet man zunächst pOH mit der Näherungsformel und erhält den pH über pH = 14 − pOH. Mehr dazu: Autoprotolyse des Wassers.
Was besagt die Henderson-Hasselbalch-Gleichung und wann wird sie verwendet?
Die Gleichung pH = pKS + lg(c(A−)/c(HA)) drückt den pH-Wert durch das Konzentrationsverhältnis von konjugierter Base zu schwacher Säure aus. Sie wird vor allem für Pufferlösungen verwendet (wenn beide Komponenten gleichzeitig vorliegen) und für Indikatoren, um den Umschlagsbereich zu bestimmen. Am Halbäquivalenzpunkt einer Titration gilt c(A−) = c(HA), also pH = pKS.
Welche Formel gilt für eine Salzlösung (z. B. Ammoniak-Salz oder Acetat-Salz)?
Ein Salz einer schwachen Base (z. B. NH4Cl) wird über das Kation als schwache Säure behandelt: pH = ½·(pKS(NH4+) − lg c₀). Ein Salz einer schwachen Säure (z. B. Natriumacetat) wird über das Anion als schwache Base behandelt: pOH = ½·(pKB(Acetat−) − lg c₀), dann pH = 14 − pOH. Ausführlich erklärt auf der Seite Säure-Base-Reaktionen in Salzlösungen.
Welche Formel gilt bei einer Mischung aus schwacher Säure und ihrer konjugierten Base?
Genau das ist eine Pufferlösung. Hier gilt die Henderson-Hasselbalch-Gleichung direkt: pH = pKS + lg(c(A−)/c(HA)). Im Puffer-Optimum (c(A−) = c(HA)) ist pH = pKS, und der Puffer arbeitet im Bereich pKS ± 1 am effektivsten. Alles Weitere: Pufferlösungen.
Lernkarten – Formeln und Zusammenfassung
Klicke auf eine Karte, um die Antwort zu sehen.
Welche pH-Formel gilt für eine starke Säure? Warum?
pH = −lg c₀(HA)
Vollständige Protolyse → c(H3O+) = c₀(HA),
kein Gleichgewicht zu berechnen.
Welche Näherungsformel gilt für schwache Säuren?
pH = ½·(pKS − lg c₀)
Gilt wenn c₀ ≫ c(H3O+), d. h. Gleichgewicht liegt weit links.
Wie berechnet man pH aus pOH?
pH = 14 − pOH (bei 25 °C)
Folgt aus der Autoprotolyse: pH + pOH = pKW = 14
Wie lautet die Henderson-Hasselbalch-Gleichung?
pH = pKS + lg(c(A−) / c(HA))
Gilt für Pufferlösungen und Indikator-Umschlagsbereich.
Rechenaufgabe: 0,10 mol/L NH3-Lösung, pKB(NH3) = 4,74. Welchen pH hat die Lösung?
pOH = ½·(4,74 − lg 0,10) = ½·(4,74 + 1) = ½·5,74 = 2,87
pH = 14 − 2,87 = 11,13
Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← Säure-Base-Reaktionen in Salzlösungen → Indikatoren
🔁 Einzelne Abschnitte: pKS-Wert · pKB-Wert · Der pH-Wert · Autoprotolyse / pKW
📌 Weiterführend: Indikatoren · Säure-Base-Titration · Pufferlösungen
