Was du auf dieser Seite lernst
Nicht jede Neutralisationsreaktion ergibt eine neutrale Lösung. Du lernst, warum Kationen als Säuren und Anionen als Basen wirken können, was Hydrogensalze besonders macht und wie man den pH-Wert einer Salzlösung mit Hilfe der pKS- bzw. pKB-Werte abschätzt.
Grundlagen – Kursstufe Säure-Base
Diese Seite baut auf den vorherigen Abschnitten auf: → pKB-Wert: pKS + pKB = 14 · → pH-Wert starker und schwacher Säuren
4.5 Säure-Base-Reaktionen in Salzlösungen
Neutralisationsreaktion: Säure + Base ⇌ Salz + Wasser
⇒ Die entstehende Lösung muss nicht unbedingt neutral sein.
4.5.1 Kationen als Säuren
a) Kationen als korrespondierende Säuren schwacher Basen
Das Kation muss ein Proton abgeben können:
NH4+ + H2O ⇌ NH3 + H3O+
(NH3 = schwache Base; NH4+ = korrespondierende Säure)
b) Hydratisierte Metall-Kationen (z. B. Fe3+(aq), Al3+(aq))
[Fe(H2O)6]3+ + H2O ⇌ [Fe(OH)(H2O)5]2+ + H3O+
↑ Zum Vergrößern klicken
✕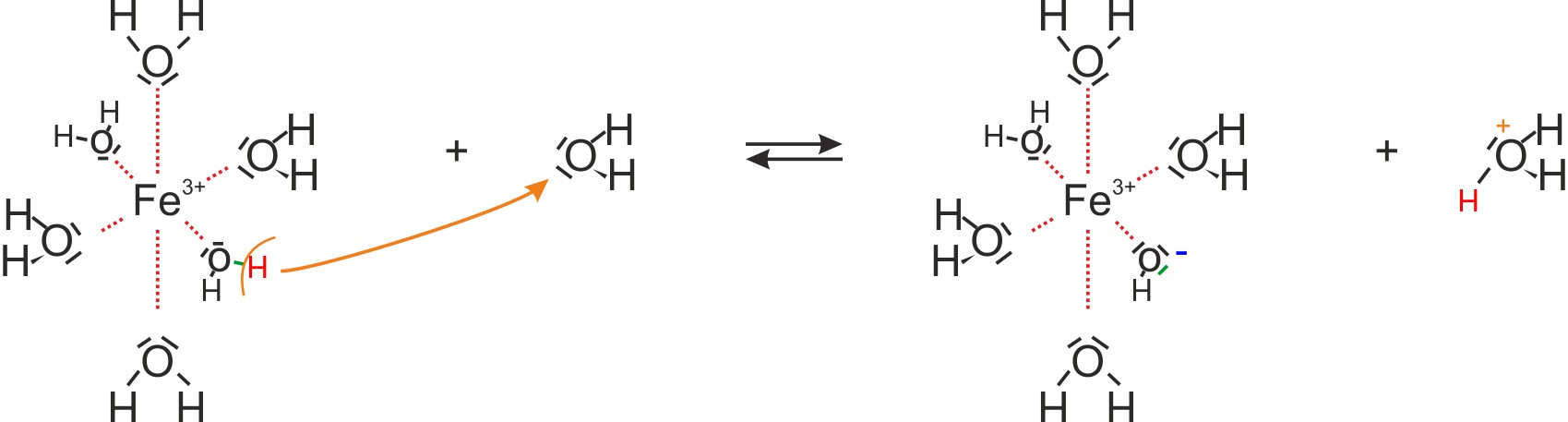
Bei mehrfach positiv geladenen Metallionen werden die Wassermoleküle der Hydrathülle so stark polarisiert, dass es zur Abspaltung eines Protons kommen kann.
Die Säurestärke nimmt zu, je …
- … höher die Ladung des Metallkations ist
- … kleiner der Ionenradius des Metallkations ist
⇒ je größer die Ladungsdichte ist, desto stärker die Säurewirkung.
Alkali- und Erdalkalimetallkationen → geringe Ladungsdichte → geringe Säurestärke → Säurewirkung vernachlässigbar
4.5.2 Anionen als Basen
a) Anionen als korrespondierende Basen schwacher Säuren
Beispiel: Natriumacetat
CH3COO− + H2O ⇌ CH3COOH + OH−
- Acetat-Ion reagiert mit Wasser als Base
- Hydratisierte Natrium-Ionen reagieren nicht mit Wasser
- ⇒ alkalische Lösung (pH > 7)
b) Anionen sehr starker und vieler starker Säuren
Diese sind schwache bis sehr schwache Basen → keine nennenswerten Säure-Base-Reaktionen mit Wasser.
Beispiele für „neutrale Anionen": Cl−, Br−, I−, NO3−, ClO4−, SO42−
4.5.3 Hydrogensalze
Hydrogensalze können sowohl als Säuren wie auch als Basen reagieren (amphoteres Verhalten).
Beispiele: HSO4−, H2PO4−, HCO3−
4.5.4 Neutrale Salzlösungen
Eine Salzlösung ist neutral (pH = 7), wenn:
- Die Kationen haben eine geringe Säurestärke und die Anionen eine geringe Basenstärke (Beispiel: NaCl)
- Die Säurestärke der Kationen und die Basenstärke der Anionen sind gleich groß (pKS(Kation) = pKB(Anion); Beispiel: NH4CN, Ammoniumacetat)
4.5.5 Abschätzung des pH-Wertes einer Salzlösung
Abschätzung mit Hilfe der pKS- oder pKB-Werte:
| Salz | pK-Wert | Reaktion |
|---|---|---|
| Natriumhydrogensulfat NaHSO4 | pKS(HSO4−) = 1,92 | sauer |
| Eisen(III)-chlorid FeCl3 | pKS([Fe(H2O)6]3+) = 2,22 | sauer |
| Kaliumcarbonat K2CO3 | pKB(CO32−) = 3,60 | basisch |
| Ammoniumacetat NH4(CH3COO) | pKS(NH4+) = pKB(Ac−) = 9,25 | neutral |
4.5.6 Zusammenfassung: Regeln zum pH-Charakter von Salzlösungen
Generelle Voraussage über den sauren oder basischen Charakter einer Salzlösung:
Regel 1 – pH = 7
Starke Base + starke Säure
Bsp.: NaCl, KNO3, Ba(ClO3)2
Regel 2 – pH > 7 (basisch)
Starke Base + schwache Säure
Bsp.: KNO2, Ca(CH3COO)2, NaCN
Regel 3 – pH < 7 (sauer)
Schwache Base + starke Säure
Bsp.: NH4NO3, FeBr3, AlCl3
Regel 4 – sauer oder basisch
Schwache Base + schwache Säure
pH abhängig davon, ob pKS(Kation) < oder > pKB(Anion).
Bsp.: NH4CN, Cu(NO2)2
Auf einen Blick – die wichtigsten Aussagen
Kationen als Säuren
NH4+ und hydratisierte Metallionen können Protonen abgeben → saure Lösung
Anionen als Basen
Anionen schwacher Säuren (z. B. Acetat−) nehmen Protonen auf → basische Lösung
Ladungsdichte entscheidet
Hohe Ladung + kleiner Radius = hohe Ladungsdichte → starke Säurewirkung hydratisierter Kationen
pH-Abschätzung
Kleiner pKS- oder pKB-Wert → stärkere Wirkung des Ions auf den pH der Salzlösung
Häufige Fragen – Säure-Base-Reaktionen in Salzlösungen
Warum ist eine Natriumacetat-Lösung basisch, obwohl es sich um ein Salz handelt?
Natriumacetat entsteht aus der Neutralisation von Essigsäure (schwache Säure) mit Natronlauge (starke Base). Das Acetat-Ion ist die korrespondierende Base der Essigsäure und reagiert mit Wasser: CH3COO− + H2O ⇌ CH3COOH + OH−. Da OH−-Ionen entstehen, ist die Lösung alkalisch (pH > 7). Das Na+-Ion reagiert nicht mit Wasser (geringe Ladungsdichte). Mehr zur pH-Berechnung: pH-Wert schwacher Basen.
Warum wirkt FeCl3-Lösung sauer?
Das Eisen(III)-Ion liegt in Wasser als hexaqua-Komplex [Fe(H2O)6]3+ vor. Durch die dreifach positive Ladung bei gleichzeitig kleinem Ionenradius ist die Ladungsdichte sehr hoch. Dadurch werden die koordinierten Wassermoleküle so stark polarisiert, dass ein Proton leicht abgespalten werden kann: [Fe(H2O)6]3+ + H2O ⇌ [Fe(OH)(H2O)5]2+ + H3O+. Der pKS-Wert beträgt 2,22 – eine merklich saure Lösung.
Was sind Hydrogensalze und warum verhalten sie sich amphoter?
Hydrogensalze wie HCO3−, H2PO4− oder HSO4− enthalten noch eine abgebbare OH-Gruppe oder ein Proton. Sie können sowohl als Säure (Protonenabgabe) als auch als Base (Protonenaufnahme) reagieren – man nennt das amphoteres Verhalten. Ob eine Hydrogensalz-Lösung sauer oder basisch ist, hängt davon ab, welche Reaktion überwiegt (Vergleich der pKS- und pKB-Werte).
Wie schätzt man den pH-Wert einer Salzlösung ab?
Man vergleicht die pK-Werte der beteiligten Ionen:
– Kleiner pKS-Wert des Kations → stark saure Lösung
– Kleiner pKB-Wert des Anions → stark basische Lösung
– Sind beide Werte gleich (z. B. Ammoniumacetat: pKS = pKB = 9,25) →
neutrale Lösung.
Für eine quantitative Berechnung verwendet man die Näherungsformeln aus
Abschnitt 4.4
mit pKB = 14 − pKS.
Warum sind Cl−- oder NO3−-Ionen in Wasser „neutral"?
Diese Anionen sind die konjugierten Basen sehr starker Säuren (HCl, HNO3). Da starke Säuren einen extrem kleinen pKS-Wert haben, ist der pKB-Wert ihrer konjugierten Base nach pKS + pKB = 14 sehr groß – sie reagieren praktisch nicht mit Wasser. Mehr dazu: pKB-Wert und Basenstärke.
Lernkarten – Salzlösungen und ihr pH-Wert
Klicke auf eine Karte, um die Antwort zu sehen.
Warum ist eine Lösung von NH4Cl sauer?
NH4+ ist die korrespondierende Säure der schwachen Base NH3 und gibt ein Proton an Wasser ab → H3O+ entsteht → pH < 7.
Welche Eigenschaft eines Metallions bestimmt seine Säurestärke in Wasser?
Die Ladungsdichte: je höher die Ladung und je kleiner der Ionenradius, desto stärker wird die Hydrathülle polarisiert und desto leichter wird ein Proton abgegeben.
Wann ergibt eine Salzlösung genau pH = 7?
Entweder: Kation und Anion haben beide vernachlässigbare Säure-/Basenwirkung (z. B. NaCl).
Oder: pKS(Kation) = pKB(Anion) – die Wirkungen heben sich auf.
Was ist das besondere an Hydrogensalzen wie HCO3−?
Sie sind amphoter: können sowohl als Säure (Proton abgeben) als auch als Base (Proton aufnehmen) reagieren. Das Überwiegen hängt von den pK-Werten ab.
Aufgabe: Ist Kaliumcarbonat-Lösung sauer, neutral oder basisch? (pKB(CO32−) = 3,60)
pKB = 3,60 → kleiner Wert → starke Basenwirkung.
CO32− + H2O ⇌ HCO3− + OH−
→ K2CO3-Lösung ist basisch (pH > 7).
Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← pH-Wert starker und schwacher Säuren → Zusammenfassung Säure-Base
🔁 Grundlagen: pKS + pKB = 14 · Neutralisation (Kursstufe) · Brønsted-Definition (Kl. 9)
📌 Weiterführend: Säure-Base-Titration · Pufferlösungen
