6.2 Alkanone (Ketone)
6.2.1 Herstellung von Alkanonen (Ketonen)
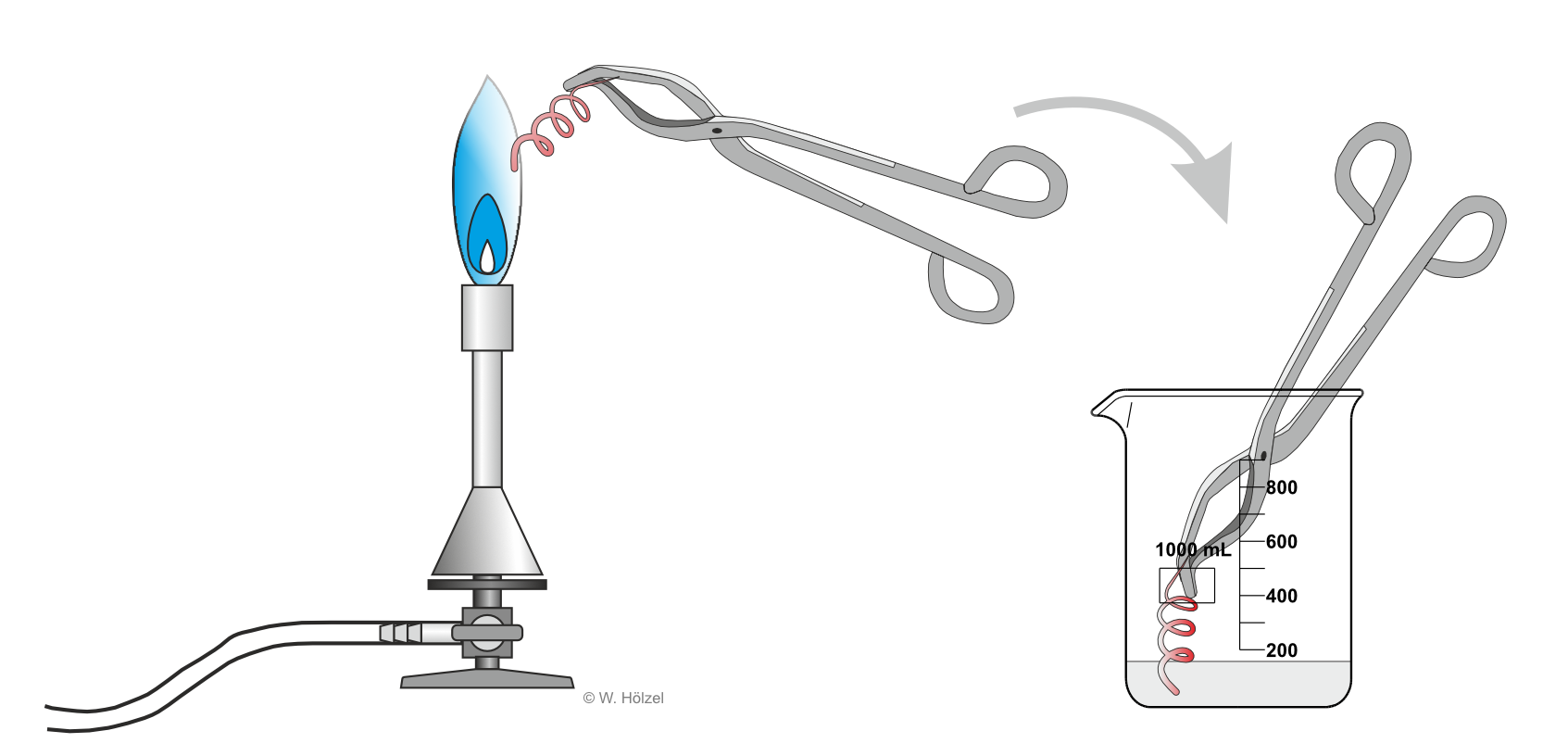
Versuch
Die heiße CuO-Spirale wird mehrmals in 2-Propanol getaucht.
Beobachtung
Der schwarze Überzug verschwindet; es entsteht blankes Kupfer. Zusätzlich tritt ein charakteristischer Geruch auf.
Zugabe von FSS zur abgekühlten Lösung gibt keine Violettfärbung.
Auswertung
Es handelt sich um eine Redoxreaktion. Die Cu²⁺-Ionen werden zu Kupfer reduziert und 2-Propanol (Isopropanol) wir zu Propanon (Aceton) oxidiert.
Reaktionsgleichung
Versucht einmal für diese Herstellung die Reaktionsgleichung mit Hilfe von Strukturformeln zu formulieren. Wer Hilfen braucht, kann ja ein paar Seiten vorher schauen, wo die primären Alkohole oxidiert wurden.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Merke: Alle sekundären Alkohole lassen sich durch Oxidation (bzw. Dehydrierung) in Ketone (Alkanone) überführen.
6.2.2 Funktionelle Gruppe der Alkanone (Ketone)
Die Alkanone besitzen (auch) eine „Carbonyl-Gruppe“.
Speziell hier: „Keto-Gruppe“
6.2.3 Eigenschaften und Verwendung von Aceton (Propanon)
Aceton ist eine farblose, charakteristisch riechende Flüssigkeit (Sdp.: 56 °C). Aceton ist brennbar. Aceton löst sowohl hydrophile (z.B. H₂O, C₂H₅OH ⇨ kann mit diesen Molekülen auch H-Brücken eingehen) als auch hydrophobe Stoffe. ⇨ Verwendung: Lösungsmittel.
Erkennbar, dass Aceton ein gutes Lösungsmittel ist, zeigt die nächste Abbildung. Was dort rot gefärbt ist, zeigt näherungsweise die negative Partialladung (anders als bei meiner Farbgebung) umd den Stauerstoff und was blau gefärbt ist, die positive Partialladung.