5.3 Chemische Reaktionen von Alkohol, Alkanol (am Beispiel von Ethanol)
5.3.1 Bindungsverhältnisse
5.3.2 Ethanol und Natrium (Redoxreaktion)
Ein Thema, welches schon zuvor angesprochen wurde.
5.3.3 Verbrennung von Ethanol
Übung: Formuliere eine Reaktionsgleichung für die vollständige Verbrennung von Ethanol. Bestimme hierfür auch die Atome, die oxidiert und die reduziert wurden und begründe Deine Wahl.
{slider title="Lösung" open="false" class="icon"}
Oxidation = Erhöhung der Oxidationszahlen („e- Abgabe“) ⇨ C
Reduktion = Erniedrigung der Oxidationszahlen („e- Aufnahme“) ⇨O (nur der Luftsauerstoff)
{/sliders}
5.3.4 Reaktion von Ethanol mit Bromwasserstoffsäure
Im Mikroglasbaukasten werden 1ml Ethanol mit 4 ml HBr erhitzt. Das entstehende Produkt wird in Wasser eingeleitet. Das neue Produkt (Bromethan) besitzt eine größere Dichte als Wasser.
Ablauf der Reaktion:
1. Schritt: Protonierung
⇒ Säure-Base-Reaktion
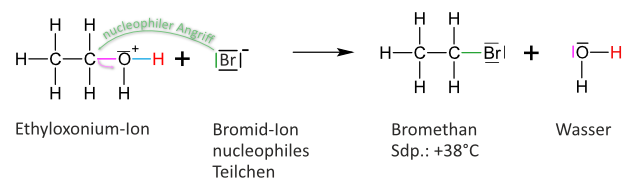
2. Schritt: Nucleophile Substitution
Es handelt sich also um eine nucleophile Substitution, SN-Reaktion.
Substitution an Alkoholen laufen meist erst nach Protonierung ab! Ein Hydroxidion (OH⁻ ) ist stärker nucleophil und viel schwerer abzuspalten als ein Wassermolekül (schwach nucleophil).