4.2 Atomradien
{slider title="Link zur interaktiven Übungsseite mit Bildern" open="false" class="icon"}
{/sliders}
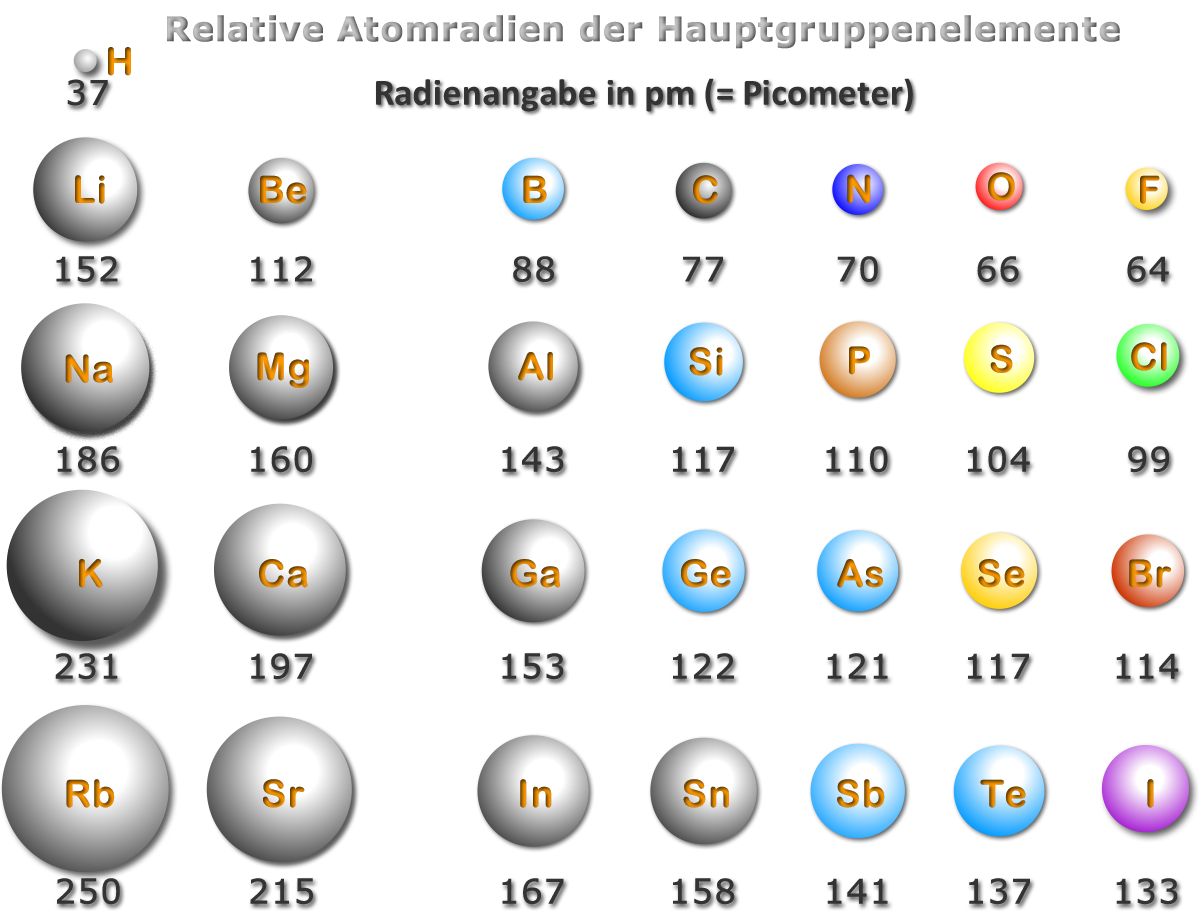
Folgende Abbildung zeigt, wie der Zusammenhang der Atomradien und das PSE ist.
Überlegt Euch die Erklärungen dafür, dass die Atomradien von oben nach unten und von rechts nach links zunehmen.
Innerhalb einer Hauptgruppe:
{slider title="Lösung" open="false" class="icon"}
Atomradien nehmen von oben nach unten zu, da die Anzahl der Schalen zunimmt.
{/sliders}
Innerhalb einer Periode:
{slider title="Lösung" open="false" class="icon"}
Atomradien nehmen von links nach rechts ab. Da die Anzahl der Protonen steigt, werden die Elektronen stärker vom Atomkern angezogen.
Diese Anziehung überwiegt die Abstoßung der Elektronen untereinander.
{/sliders}