Was du auf dieser Seite lernst
Du verstehst, warum reines Wasser elektrisch leitfähig ist, und lernst die Autoprotolyse (Eigenprotolyse) des Wassers kennen. Du leitest das Ionenprodukt KW über das Massenwirkungsgesetz her und berechnest die H3O+- und OH−-Konzentration in reinem Wasser bei 25 °C.
1.1 Das Ionenprodukt des Wassers
↑ Zum Vergrößern klicken
✕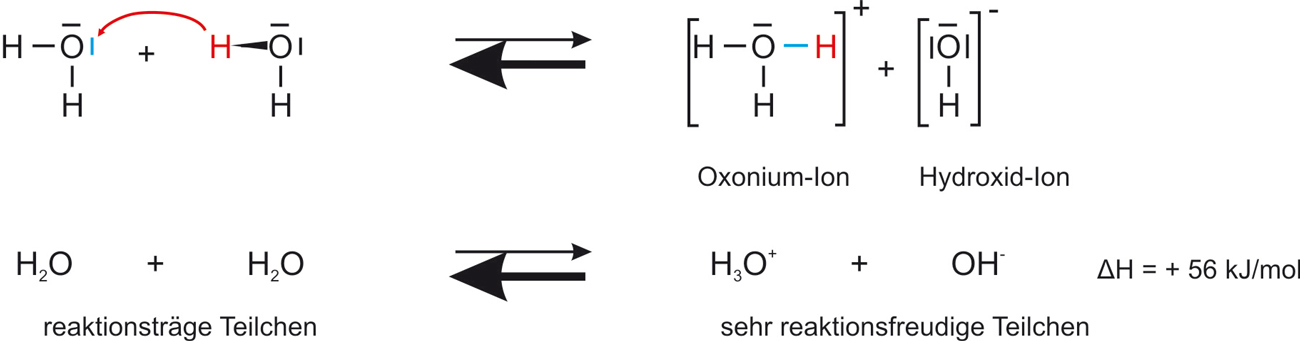
Destilliertes Wasser besitzt eine geringe elektrische Leitfähigkeit – ein Hinweis auf das Vorhandensein von Ionen. Diese Ionen entstehen durch eine Protolyse-Reaktion zweier Wassermoleküle miteinander (Autoprotolyse).
Hinweis zum MWG: Bei der Aufstellung des Massenwirkungsgesetzes steht das Oxonium-Ion in der Regel im Zähler:
Überlegungen – wie groß ist c(H2O)?
- 1 mol Wasser hat die Masse 18,0 g → M(H2O) = 18 g/mol
- 1 L Wasser besitzt bei 25 °C die Masse 997 g
Wie groß ist die Konzentration c(H2O) in Wasser?
| Dichte: | σ = m V ⇒ m = σ · V |
| Stoffmenge: | M = m n ⇒ n = m M = ρ · V M |
| Konzentration: | c = n V = ρ · V M · V = ρ M |
= 55,4 · 6,022 · 1023 Wassermoleküle pro Liter!
Die H2O-Konzentration in Wasser beträgt also konstant 55,4 mol/L.
Durch Leitfähigkeitsmessung lässt sich bei 25 °C bestimmen:
Diese Werte in das MWG einsetzen:
KC ist extrem klein → das Gleichgewicht liegt weitgehend auf der linken Seite → Die Konzentration von H2O ist daher auch bei Gleichgewichtsverschiebungen praktisch konstant. Sie kann mit KC zu einer neuen Konstanten KW (Ionenprodukt des Wassers) vereinigt werden:
KC · c²(H2O) = KW = c(H3O+) · c(OH−) = 1,00 · 10−14 mol²/L²
√KW = c(H3O+) = c(OH−) = (1,00 · 10−14 mol²/L²)½ = 1,00 · 10−7 mol/L
⚠️ Achtung: In reinem Wasser und in neutralen wässrigen Lösungen beträgt die Konzentration der Oxonium-Ionen und der Hydroxid-Ionen jeweils 10−7 mol/L.
Es haben also nur 2 Wassermoleküle von einer Milliarde zu einem Oxonium-Ion und einem Hydroxid-Ion reagiert.
Auf einen Blick – die wichtigsten Aussagen
Autoprotolyse
H2O + H2O ⇌ H3O+ + OH−
Gleichgewicht liegt links · endotherm (ΔH = +56 kJ/mol)
Ionenprodukt KW
KW = c(H3O+) · c(OH−) = 10−14 mol²/L² bei 25 °C
Neutrales Wasser
c(H3O+) = c(OH−) = 10−7 mol/L
→ pH = 7
Gleichgewichtslage
KC = 3,26 · 10−18 → extrem klein
Nur 2 von 109 H2O-Molekülen reagieren
Häufige Fragen zur Autoprotolyse
Warum leitet destilliertes Wasser Strom, obwohl keine Salze gelöst sind?
Durch die Autoprotolyse bilden sich in jeder wässrigen Lösung stets geringe Mengen an Oxonium-Ionen (H3O+) und Hydroxid-Ionen (OH−). Diese geladenen Teilchen ermöglichen einen sehr schwachen Stromfluss. Da das Gleichgewicht aber weit auf der linken Seite liegt, ist die Leitfähigkeit von reinem Wasser sehr gering – messbar, aber kaum spürbar.
Was ist der Unterschied zwischen KC und KW?
KC ist die allgemeine Gleichgewichtskonstante aus dem MWG: KC = c(H3O+) · c(OH−) / c²(H2O). Da die Wasserkonzentration mit 55,4 mol/L praktisch konstant ist, wird sie in KC eingearbeitet: KW = KC · c²(H2O). KW enthält dann nur noch die Ionenkonzentrationen und ist einfacher zu handhaben.
Ändert sich KW mit der Temperatur?
Ja – KW ist temperaturabhängig. Bei 25 °C gilt KW = 10−14 mol²/L². Da die Autoprotolyse endotherm ist, verschiebt sich das Gleichgewicht bei höherer Temperatur nach rechts → KW wird größer. Bei 37 °C (Körpertemperatur) gilt KW ≈ 2,4 · 10−14 mol²/L², der neutrale pH-Wert liegt dann bei ca. 6,8 – obwohl die Lösung chemisch neutral ist!
Was passiert mit c(OH−), wenn ich eine Säure zugebe?
Gibt man eine Säure hinzu, steigt c(H3O+). Da KW = c(H3O+) · c(OH−) bei konstanter Temperatur konstant bleibt, sinkt c(OH−) entsprechend. Beispiel: c(H3O+) = 10−3 mol/L → c(OH−) = 10−14 / 10−3 = 10−11 mol/L. → Kapitel 2: pH-Wert
Warum kann c(H2O) als Konstante behandelt werden?
KC = 3,26 · 10−18 ist extrem klein – das Gleichgewicht liegt fast vollständig auf der linken Seite. Von einer Milliarde Wassermolekülen reagieren nur etwa 2. Die Änderung von c(H2O) ist daher vernachlässigbar klein, c(H2O) ≈ 55,4 mol/L bleibt praktisch konstant und kann in KW eingearbeitet werden.
Lernkarten – Autoprotolyse und Ionenprodukt
Klicke auf eine Karte, um die Antwort zu sehen.
Was versteht man unter der Autoprotolyse des Wassers?
Zwei H2O-Moleküle reagieren miteinander – eines gibt ein Proton ab, das andere nimmt es auf:
H2O + H2O ⇌ H3O+ + OH−
Wie lautet das Ionenprodukt des Wassers KW bei 25 °C?
KW = c(H3O+) · c(OH−)
= 1,00 · 10−14 mol²/L²
(gilt für alle wässrigen Lösungen bei 25 °C)
Welche Ionenkonzentration herrscht in neutralem Wasser bei 25 °C?
c(H3O+) = c(OH−)
= 1,00 · 10−7 mol/L
→ pH = 7 (neutral)
Warum wird c(H2O) in KW „eingebaut"?
c(H2O) ≈ 55,4 mol/L = konstant (GG liegt weit links, KC = 3,26 · 10−18)
→ KW = KC · c²(H2O)
Berechne c(OH−), wenn c(H3O+) = 1,00 · 10−4 mol/L (25 °C).
c(OH−) =
KW / c(H3O+)
= 10−14 / 10−4
= 10−10 mol/L
Weiter im Kapitel Säure-Base
↑ Übersicht Säure-Base-Reaktionen → Kapitel 2: pH-Wert → Kapitel 3: Protolyse-Reaktionen → Kapitel 4: pK-Werte
