Was du auf dieser Seite lernst
Du lernst, wie man den pH-Wert für starke und schwache Säuren bzw. Basen berechnet. Für sehr starke Säuren gilt direkt pH = −lg c₀(HA), für schwache Säuren wird die wichtige Näherungsformel pH = ½ · (pKS − lg c₀) hergeleitet – inklusive drei vollständig gelöster Beispielaufgaben.
Grundlagen – Kursstufe Säure-Base
Diese Seite baut direkt auf den vorherigen Abschnitten auf: → 4.1 Säurestärke – der pKS-Wert · → 4.2/4.3 pKB-Wert und pKS + pKB = 14 · → Der pH-Wert
4.4 pH-Wert unterschiedlich starker Säuren
Allgemeine Protolysereaktion einer Säure:
HA + H2O ⇌ A1− + H3O+
- c(H2O) = konst.
- c₀ = Ausgangskonzentration der Säure
- c(H+) = c(A1−) (Vernachlässigung der Autoprotolyse, gültig für c₀(HA) ≥ 10−6 mol/L)
Exkurs: Allgemeine Herleitung
Falls dir das Folgende schwerfällt, schau nochmals im Kapitel Gleichgewichtschemie – Massenwirkungsgesetz nach; dort wurde es bereits behandelt.
c) Allgemein
HA + H2O ⇌ A1− + H3O+
c(H+) = c(A1−) = x
| HA | ⇌ | A1− | + H+ | |
| Ausgangskonz. | c₀(HA) | 0 | 0 | |
| Im Gleichgewicht | c₀(HA) − c(H+) | c(H+) | c(H+) | |
| c₀ − x | x | x |
↑ Zum Vergrößern klicken
✕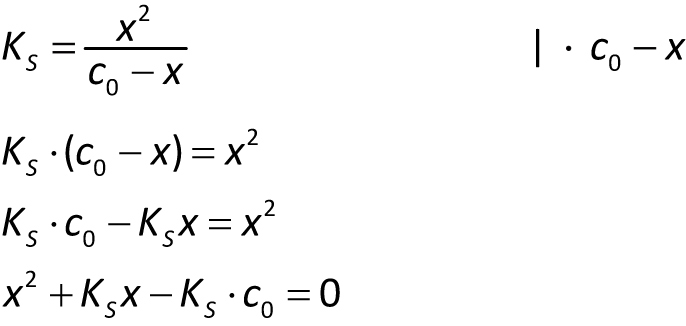
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕
a) Sehr starke Säuren (pKS < −1,74) und Basen (pKB < −1,74)
Sehr starke Säuren reagieren vollständig mit Wasser.
(Das Oxoniumion H3O+ ist die stärkste Säure, die in wässriger Lösung existieren kann.)
HA + H2O → A1− + H3O+
c(H3O+) = c₀(HA)
pH = − lg (c₀(HA))
Beispiel: Wie groß ist der pH-Wert von Salzsäure mit c₀(HCl) = 0,01 mol/L?
Da HCl eine sehr starke Säure ist:
c(H3O+) = c₀(HCl) = 0,01 mol/L = 10−2 mol/L
pH = 2
Starke Basen reagieren in wässrigen Lösungen vollständig mit Wasser.
c(OH−) = c₀(Base)
Beispiel: Wie groß ist der pH-Wert von Natronlauge mit c₀(NaOH) = 0,1 mol/L?
c(OH−) = 0,1 mol/L
pOH = − lg 10−1 = 1
pH = 14 − pOH = 13
b) Schwache Säuren und Basen
HA + H2O ⇌ A1− + H3O+
Das Gleichgewicht liegt fast vollständig auf der linken Seite (c₀ ≫ c(A1−)), daher gilt die Näherung:
c(HA) ≈ c₀(HA)
↑ Zum Vergrößern klicken
✕
Für Basen gilt entsprechendes (Ersetzung von c(H3O+) durch c(OH−), pH durch pOH, pKS durch pKB).
Aufgaben
Aufgabe 1 Nenne die Oxoniumionen-Konzentration und den pH-Wert einer Lösung von salpetriger Säure mit c₀(HNO2) = 0,10 mol/L bei 25 °C. (KS = 4,5 · 10−4 mol/L)
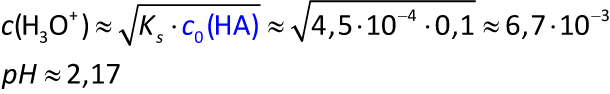
Aufgabe 2 Die Lösung einer schwachen Säure HX mit c₀ = 0,10 mol/L hat den pH-Wert 3,30. Wie groß sind KS und pKS?
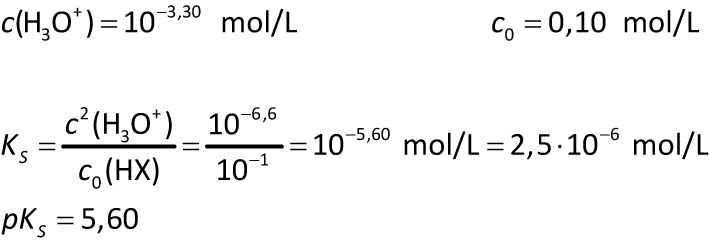
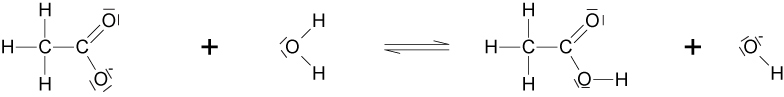
Aufgabe 3 Welchen pH-Wert hat eine Lösung von 0,1 mol/L Natriumacetat (pKS(CH3COOH) = 4,74)? Formuliere die Reaktionsgleichung als Strukturformeln.
 ✕
✕

Auf einen Blick – die wichtigsten Aussagen
Sehr starke Säuren
Vollständige Reaktion: c(H3O+) = c₀(HA)
→ pH = −lg c₀(HA)
Schwache Säuren
Näherung c(HA) ≈ c₀(HA):
→ pH = ½ · (pKS − lg c₀)
Starke Basen
c(OH−) = c₀(Base)
→ pOH = −lg c₀ → pH = 14 − pOH
Schwache Basen
Näherung c(Base) ≈ c₀:
→ pOH = ½ · (pKB − lg c₀)
→ pH = 14 − pOH
Häufige Fragen – pH-Wert starker und schwacher Säuren
Wie berechnet man den pH-Wert einer sehr starken Säure wie Salzsäure?
Sehr starke Säuren reagieren vollständig mit Wasser: Jedes Molekül HA gibt ein Proton ab. Daher ist die Oxoniumionen-Konzentration gleich der Ausgangskonzentration: c(H3O+) = c₀(HA). Der pH-Wert ergibt sich direkt zu: pH = −lg c₀(HA). Beispiel: c₀(HCl) = 0,01 mol/L → pH = 2. Dieses Prinzip gilt für alle Säuren mit pKS < −1,74.
Was ist die Näherungsformel für schwache Säuren und wann gilt sie?
Für schwache Säuren (pKS > 2, c₀ ≫ c(H3O+)) gilt die Näherung c(HA) ≈ c₀(HA), weil das Gleichgewicht stark auf der linken Seite liegt. Damit vereinfacht sich die KS-Formel zu KS = c²(H3O+) / c₀(HA), woraus folgt: pH = ½ · (pKS − lg c₀(HA)). Diese Näherung ist gültig, solange c₀(HA) ≥ 10−6 mol/L und der Protolysegrad unter ~5 % liegt.
Wie berechnet man KS, wenn pH-Wert und Ausgangskonzentration gegeben sind?
Man nutzt die Beziehung KS = c²(H3O+) / c₀(HA). Aus dem pH-Wert ergibt sich c(H3O+) = 10−pH. Beispiel (Aufgabe 2): pH = 3,30 → c(H3O+) = 10−3,30. KS = (10−3,30)² / 0,10 = 10−6,6 / 10−1 = 10−5,60 = 2,5 · 10−6 mol/L → pKS = 5,60. Mehr dazu auf der Seite pKS-Wert.
Wie berechnet man den pH-Wert einer Salzlösung (z. B. Natriumacetat)?
Salze schwacher Säuren bilden in Wasser eine basische Lösung, weil das Anion (z. B. Acetat−) als Base mit Wasser reagiert. Man berechnet zuerst pKB = 14 − pKS, dann pOH = ½ · (pKB − lg c₀) und schließlich pH = 14 − pOH. Für 0,1 mol/L Natriumacetat (pKS = 4,74): pKB = 9,26. Das Ergebnis ist eine schwach basische Lösung (pH > 7). Ausführlicher auf der Seite Säure-Base-Reaktionen in Salzlösungen.
Warum muss man bei sehr starken Säuren keine Gleichgewichtsrechnung durchführen?
Bei sehr starken Säuren (pKS < −1,74) liegt das Protolysegleichgewicht vollständig auf der Produktseite – die Reaktion verläuft praktisch irreversibel. Das Oxoniumion H3O+ ist die stärkste Säure, die in wässriger Lösung existieren kann (Nivellierungseffekt des Wassers). Daher entfällt das Einsetzen von Gleichgewichtsgrößen; die Oxoniumionenkonzentration entspricht direkt der eingesetzten Säurekonzentration. Hintergrund: Autoprotolyse des Wassers.
Lernkarten – pH-Wert starker und schwacher Säuren
Klicke auf eine Karte, um die Antwort zu sehen.
Wie lautet die pH-Formel für eine sehr starke Säure?
c(H3O+) = c₀(HA)
→ pH = −lg c₀(HA)
(vollständige Protolyse, pKS < −1,74)
Wie lautet die Näherungsformel für den pH-Wert einer schwachen Säure?
pH = ½ · (pKS − lg c₀(HA))
Gilt wenn: c₀ ≫ c(H3O+), d. h. das GG liegt links.
Wie berechnet man den pH-Wert einer starken Base wie NaOH (0,1 mol/L)?
c(OH−) = 0,1 mol/L
pOH = − lg (10−1) = 1
pH = 14 − 1 = 13
Wann darf man die Näherung c(HA) ≈ c₀(HA) verwenden?
Wenn das Gleichgewicht weit auf der linken Seite liegt:
c₀ ≫ c(A−), d. h. schwache Säure mit c₀ ≥ 10−6 mol/L
und pKS groß (Protolysegrad < ~5 %).
Rechenaufgabe: Welchen pH hat 0,10 mol/L Essigsäure (pKS = 4,74)?
pH = ½ · (4,74 − lg 0,10)
= ½ · (4,74 − (−1))
= ½ · 5,74
= pH ≈ 2,87
Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← pKB-Wert und Basenstärke → Säure-Base-Reaktionen in Salzlösungen
🔁 Grundlagen: Der pH-Wert (Kursstufe) · Autoprotolyse des Wassers – pKW · Massenwirkungsgesetz
📌 Weiterführend: Säure-Base-Titration · Pufferlösungen
