5.1.5 Induktiver Effekt (I-Effekt)
Ausschlaggebend: Elektronegativität (EN) der Substituenten (Atomgruppen, Atome die dranhängen). Dabei werden Elektronen über mehrere Bindungen angezogen oder „abgestoßen“.
Reichweite: 3 benachbarte Bindungen.
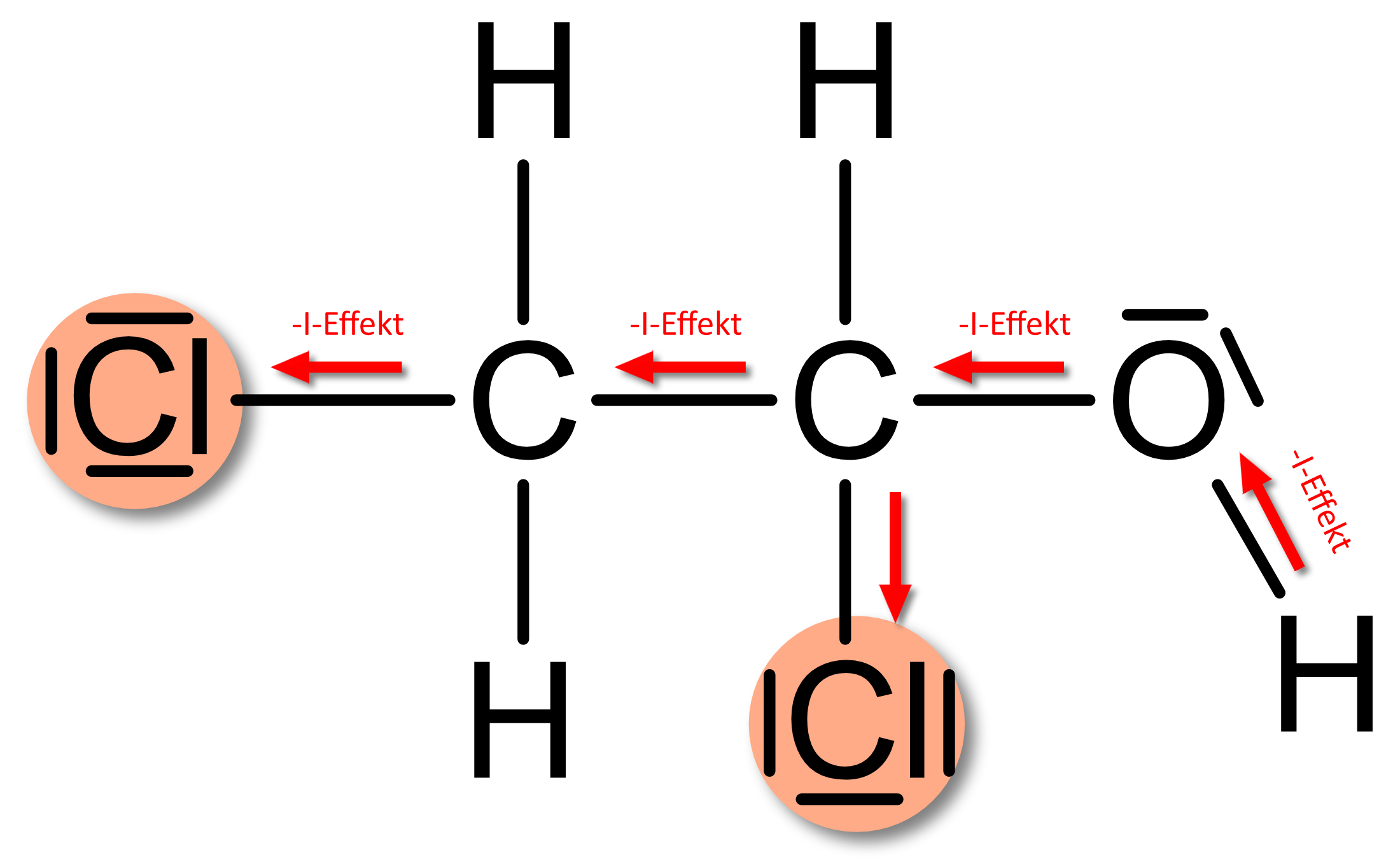
(-I)-Effekt (sprich: „minus I Effekt“; „negativer I Effekt“).
• Substituenten (Atomgruppen) mit höherer Elektronegativität (Bsp.: Halogene, Sauerstoff-Verbindungen, ...)• „Elektronenziehend“:
Ziehen Bindungselektronen zu sich
Auswirkung: z.B. Erleichterte Abspaltung eines Protons; Alkohol kann als Säure reagieren.
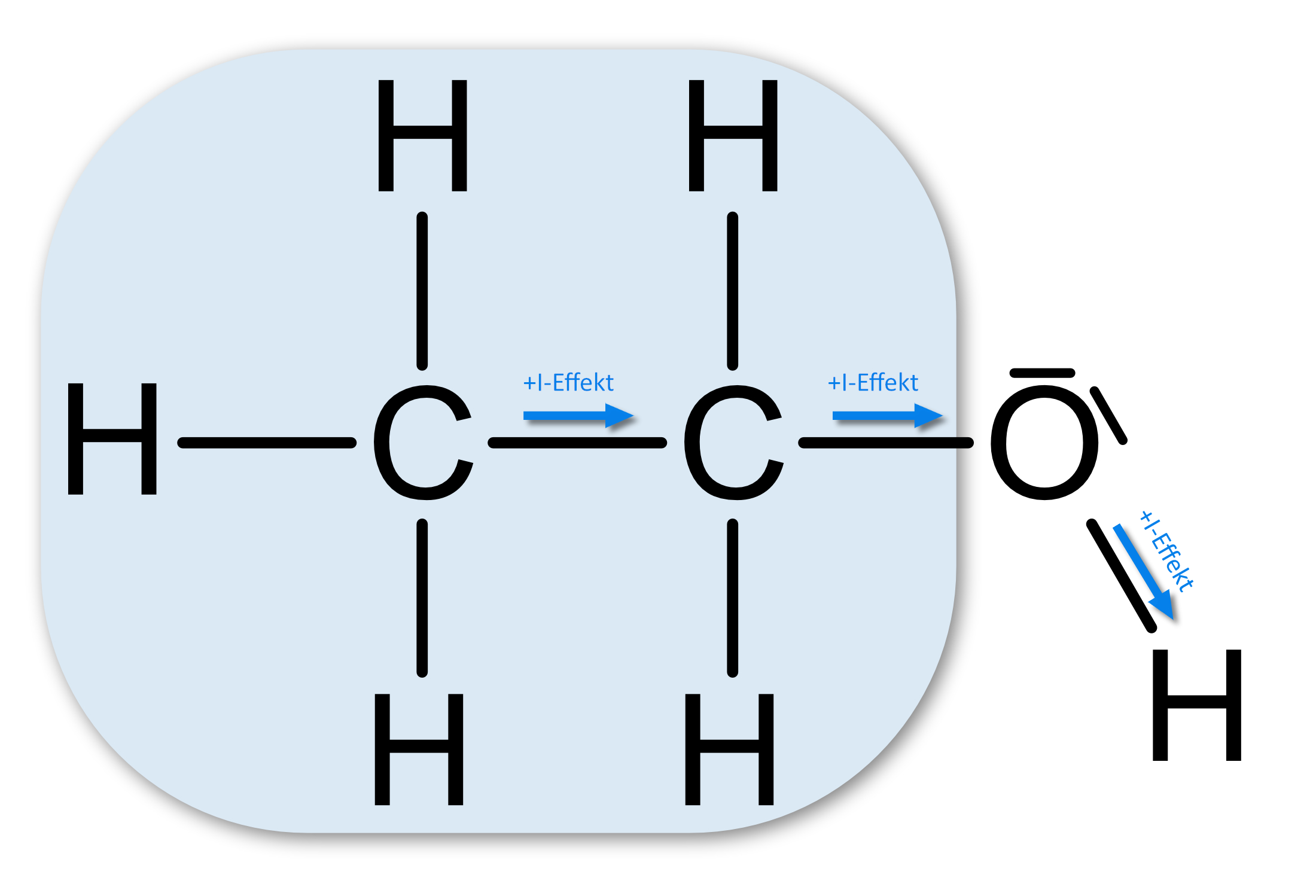
(+I)-Effekt (sprich: „plus I Effekt“; positiver I Effekt)
Elektropositiveren Substituenten (Bsp.: Alkylgruppen). Je mehr bzw. je länger die Alkylgruppe, umso stärker ist der +-I-Effekt.
„Elektronenschiebend“:
Auswirkung: z.B. geringere Säurestärke
Keinen I-Effekt haben Wasserstoffatome.
Auswirkung für das Experiment und Vergleich: Ethanol + Natrium und Wasser + Natrium
Bei diesem Experiment (siehe Seite zuvor) kommt es zu einer heftigeren Reaktion, wenn das Proton (vom Wasser oder Alkohol) leicht abgespalten wird. Je leichter es abgespalten wird, umso stärker ist ja auch seine Säure-Wirkung. Da Wasser keinen positiven induktiven Effekt hat (hat ja auch keine Alkylgruppe), reagiert es heftiger als Ethanol (positiver induktiver Effekt durch Alkylgruppe).