Alkine
-
03 Alkine
Was du in diesem Kapitel lernst
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung – noch reaktiver als die Alkene. Das wichtigste Alkin ist Ethin (Acetylen): du lernst seine Eigenschaften, seine technische Herstellung aus Calciumcarbid und die für Alkine typischen zweistufigen Additionsreaktionen kennen.
Grundlagen aus der 10. Klasse
Alkine bauen auf dem Wissen über ungesättigte Verbindungen auf – wiederhole bei Bedarf: → 2. Alkene – C=C-Doppelbindung, Bromwasserprobe, Additionsreaktion
Kapitelübersicht – 3. Alkine
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
3.1
Ethin (Acetylen)
Physikalische & chemische Eigenschaften · Summenformel C2H2 · Strukturformel · Bananenbindung
→ 3.1.1 Eigenschaften · 3.1.2 Formelermittlung3.1.3 – 3.1.5
Herstellung & Verwendung
Herstellung aus CaC2 · Carbidlampe · Verwendung als Brenngas & Ausgangsstoff
→ 3.1.3 Herstellung · 3.1.4 Carbidlampe · 3.1.5 Verwendung3.2
Reaktionstyp bei Alkinen
Elektrophile Addition · Bromierung · Wasseranlagerung · Übungsaufgaben
→ 3.2 Reaktionstyp & Übungen
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkine besitzen eine C≡C-Dreifachbindung (1 σ- + 2 π-Bindungen). Die Bindungslänge ist mit 120 pm kürzer als bei der Doppelbindung (134 pm). Allgemeine Formel: CnH2n−2.
Herstellung
Ethin entsteht aus Calciumcarbid und Wasser: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Diese Reaktion liefert das Gas auch in der Carbidlampe.
Reaktionstyp
Alkine reagieren durch elektrophile Addition. Die Reaktion läuft zweistufig ab: erst entsteht ein Alken-Zwischenprodukt, dann wird erneut addiert → schließlich ein Alkan oder Derivat.
Linearstruktur
Ethin ist linear: alle vier Atome liegen auf einer Geraden (Bindungswinkel 180°). Die Dreifachbindung besteht aus drei „Bananenbindungen" (sp-Hybridisierung).
Häufige Fragen – Alkine
Was sind Alkine, und was unterscheidet sie von Alkenen?
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung, bestehend aus einer σ-Bindung und zwei π-Bindungen. Die allgemeine Formel lautet CnH2n−2 (noch zwei H-Atome weniger als bei Alkenen: CnH2n). Alkine sind durch die Dreifachbindung noch reaktiver als Alkene. Das einfachste Alkin ist Ethin (C2H2), auch Acetylen genannt. Wie Alkene zeigen Alkine elektrophile Additionsreaktionen, jedoch oft zweistufig.
Wie wird Ethin (Acetylen) technisch hergestellt?
Ethin lässt sich aus Calciumcarbid (CaC2) und Wasser herstellen. Reaktionsgleichung: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Calciumcarbid wird in der Carbidlampe (Grubenlampe) genutzt: Das entstehende Ethin verbrennt mit einer hellen, stark leuchtenden Flamme. Industriell wird Ethin heute hauptsächlich durch Cracken von Erdgas gewonnen. → 3.1.3 Herstellung
Was ist die Besonderheit der linearen Struktur von Ethin?
Beim Ethin sind alle vier Atome linear angeordnet (Bindungswinkel 180°, sp-Hybridisierung). Die C≡C-Dreifachbindung besteht nach dem Bananenbindungsmodell aus drei gebogenen Bindungen (σ + 2 π). Die Bindungslänge beträgt nur 120 pm (zum Vergleich: C=C 134 pm, C–C 154 pm). Diese kompakte Struktur erklärt die hohe Reaktivität und die ausgeprägte elektrophile Addition. → 3.1 Ethin
Wie verläuft die Bromierung von Ethin – und warum ist sie zweistufig?
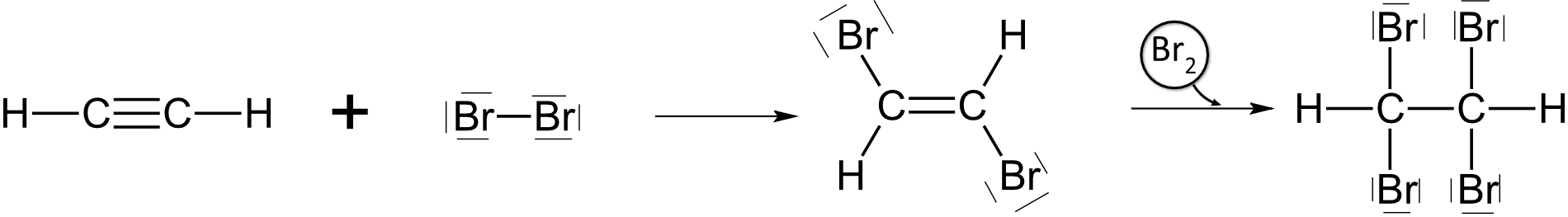
Ethin reagiert mit Brom in einer elektrophilen Addition, die zweistufig abläuft: In der ersten Stufe addiert Br2 an die Dreifachbindung → es entsteht das Zwischenprodukt trans-1,2-Dibromethen (noch eine Doppelbindung vorhanden). In der zweiten Stufe reagiert dieses mit weiterem Br2 → 1,1,2,2-Tetrabromethan (gesättigtes Endprodukt). Wird Br2 im Unterschuss eingesetzt, kann man die Reaktion auf der Dibromstufe stoppen. → 3.2 Reaktionstyp
Welche Verwendungen hat Ethin in Industrie und Technik?
Ethin (Acetylen) wird vielfältig genutzt: (1) Autogenschweißen und Schneiden: Die Verbrennung mit Sauerstoff erzeugt eine Flamme von über 3000 °C. (2) Ausgangsstoff in der Chemie: Aus Ethin werden wichtige Kunststoffe und Lösungsmittel hergestellt (z. B. PVC über Vinylchlorid). (3) Carbidlampen: Historisch als tragbare Lichtquelle in Bergbau und Feuerwehr. (4) Bei Pflanzen spielt das analoge Ethylen (= Ethen) als Phytohormon eine Rolle – Ethin kann diese Wirkung verstärken.
Lernkarten – Alkine
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkine, und woraus besteht sie?
Die C≡C-Dreifachbindung. Sie besteht aus einer σ-Bindung + zwei π-Bindungen. Bindungslänge: 120 pm. Hybridisierung: sp. Alle vier Atome in Ethin sind linear angeordnet (180°).
2Wie lautet die allgemeine Formel der Alkine? Nenne Ethin und Propin mit Formel.
CnH2n−2 (n ≥ 2)
Ethin: C2H2 (HC≡CH)
Propin: C3H4 (CH3–C≡CH)3Wie wird Ethin aus Calciumcarbid hergestellt? Nenne die Reaktionsgleichung.
CaC2 + 2 H2O
→ C2H2 + Ca(OH)2
Calciumcarbid reagiert mit Wasser zu Ethin und Calciumhydroxid.4Wie verläuft die Bromierung von Ethin – welche zwei Stufen gibt es?
Stufe 1: C2H2 + Br2 → C2H2Br2 (trans-1,2-Dibromethen, noch C=C)
Stufe 2: + Br2 → C2H2Br4 (1,1,2,2-Tetrabromethan)5Berechne: Wie viel g Br2 werden benötigt, um 26 g Ethin vollständig zu tetrabromieren?
C2H2 + 2 Br2 → C2H2Br4
M(C2H2) = 26 g/mol → n = 1 mol
n(Br2) = 2 mol → m = 2 · 160 g/mol = 320 g Br2
Weiter im Fach Chemie / 10. Klasse
← 2. Alkene → 5. Alkohole ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Cycloalkane · Aromaten – Benzol und seine Derivate
-
10. Klasse
Was du auf dieser Seite findest
In der 10. Klasse dreht sich alles um die Organische Chemie (Baden-Württemberg). Von den gesättigten Alkanen über Alkene und Alkine bis zu Alkoholen, Carbonylverbindungen und Carbonsäuren – hier findest du alle Kapitel direkt verlinkt.
Kapitel im Überblick
Kapitel 1
Alkane
Methan · Butan · homologe Reihe · Nomenklatur · radikalische Substitution
Kapitel 2
Alkene
Ethen · Doppelbindung · Nachweis · elektrophile Addition · Isomerie
Kapitel 3
Alkine
Ethin · Dreifachbindung · Bananenbindung · Herstellung
Kapitel 4 · bei ausreichend Zeit
Cycloverbindungen
Cycloalkane · (vertieft in der Kursstufe → Aromaten)
Kapitel 5
Alkohole (Alkanole)
Ethanol · Hydroxylgruppe · prim./sek./tert. · mehrwertige Alkohole
Kapitel 6
Carbonylverbindungen
Alkanale (Aldehyde) · Alkanone (Ketone) · Carbonylgruppe · Nachweise
Kapitel 7
Carbonsäuren
Essigsäure · Carboxylgruppe · ZMK · Säure-Base-Reaktionen
Kapitel 8 · ⚠️ noch nicht online
Ester
Veresterung · Estergleichgewicht (→ Kursstufe: Gleichgewichtsreaktionen)
Vollständige Inhaltsübersicht
1 Alkane
- 1.1 Methan
- 1.4 Butan
- 1.5 Homologe Reihe der Alkane
- 1.6 Genfer Nomenklatur der Alkane | → Übungen
- 1.7 Eigenschaften der Alkane
- 1.8 Angriffsfreudige Teilchen (Radikale)
- 1.9 Radikalische Substitution – Halogenalkane
2 Alkene
- 2.1 Ethen
- 2.1.5 Nachweis von Alkenen (Mehrfachbindungen)
- 2.1.6 Isomerien von Alkenen
- 2.2 Nomenklatur der Alkene
- 2.3 Katalytische Hydrierung
- 2.4 Vergleich Ethen / Ethan
3 Alkine
4 Cycloverbindungen (bei ausreichend Zeit)
- → Cycloalkane (Kursstufe) – kein eigener Klasse-10-Artikel
5 Alkohole (Alkanole)
- 5.1 Alkanol, Alkohol (Ethanol)
- 5.1.3 Formelermittlung von Ethanol | → Teil II
- 5.1.4 Versuch: Ethanol + Alkalimetall
- 5.1.5 Induktiver Effekt
- 5.2 Homologe Reihe der Alkohole
- 5.2.4 Primäre, sekundäre und tertiäre Alkohole
- 5.2.6 Mehrwertige Alkohole
- 5.3 Chemische Reaktionen von Alkoholen
6 Carbonylverbindungen (Alkanale und Alkanone)
- 6.1.1 Herstellung von Alkanalen
- 6.1.2 Funktionelle Gruppe der Alkanale (Aldehyde)
- 6.1.4 Aldehydnachweise
- 6.2 Alkanone (Ketone)
- 6.3 Unterscheidung Aldehyde / Ketone
7 Carbonsäuren
- 7.1 Essigsäure (Ethansäure)
- 7.2 Funktionelle Gruppe der Monocarbonsäuren
- 7.3 Vergleich der Siedepunkte – ZMK
- 7.4.1 Säure-Base-Reaktionen
- 7.4.2 Redoxreaktion Essigsäure + Magnesium
8 Ester (noch kein eigener Artikel)
- → Estergleichgewicht (Kursstufe: Gleichgewichtsreaktionen) – kein eigener Klasse-10-Artikel
Auf einen Blick – Organische Chemie Klasse 10
Homologe Reihe
Alkane, Alkene, Alkine und Alkanole bilden je eine homologe Reihe mit gleicher funktioneller Gruppe und sich regelmäßig ändernden Eigenschaften (je +CH₂).
Funktionelle Gruppe
Die funktionelle Gruppe bestimmt die chemischen Eigenschaften: –OH (Alkanole) · C=O (Carbonylverbindungen) · –COOH (Carbonsäuren).
Reaktionstypen
Alkane: radikalische Substitution · Alkene: elektrophile Addition · Alkohole: Oxidation zu Aldehyden/Ketonen · Carbonsäuren: Veresterung.
ZMK & Siedepunkte
Van-der-Waals-Kräfte (Alkane, Alkene) < Dipol-Kräfte < Wasserstoffbrücken (Alkanole, Carbonsäuren). Je stärker die ZMK, desto höher der Siedepunkt.
Häufige Fragen – Organische Chemie Klasse 10
Was ist eine homologe Reihe?
Eine homologe Reihe ist eine Gruppe organischer Verbindungen mit gleicher funktioneller Gruppe und gleichem Reaktionsverhalten, deren Glieder sich jeweils um eine CH₂-Einheit unterscheiden. Mit steigender Kettenlänge nehmen Siedepunkt und Viskosität zu, während die Löslichkeit in Wasser meist abnimmt. Beispiele: Methan–Ethan–Propan–Butan (Alkane) oder Methanol–Ethanol–Propanol (Alkohole).
Was versteht man unter einer funktionellen Gruppe?
Eine funktionelle Gruppe ist ein Atom oder eine Atomgruppe im Molekül, die das typische chemische Verhalten einer Stoffklasse bestimmt. In der Organischen Chemie der 10. Klasse begegnen dir: die Hydroxylgruppe –OH (Alkohole), die Carbonylgruppe C=O (Aldehyde und Ketone) und die Carboxylgruppe –COOH (Carbonsäuren).
Was unterscheidet Alkane, Alkene und Alkine voneinander?
Alkane (Formel CₙH₂ₙ₊₂) besitzen nur Einfachbindungen und reagieren durch radikalische Substitution. Alkene (CₙH₂ₙ) haben mindestens eine C=C-Doppelbindung und reagieren typischerweise durch elektrophile Addition. Alkine (CₙH₂ₙ₋₂) besitzen eine C≡C-Dreifachbindung und sind reaktiver als Alkane, aber ähnlich wie Alkene durch Addition reaktiv. → Vergleich Ethen/Ethan
Was ist der Unterschied zwischen primären, sekundären und tertiären Alkoholen?
Bei einem primären Alkohol trägt das C-Atom mit der –OH-Gruppe nur einen weiteren C-Substituenten (z. B. Ethanol). Beim sekundären Alkohol sind es zwei, beim tertiären drei C-Substituenten. Diese Unterscheidung ist wichtig für die Oxidierbarkeit: Primäre und sekundäre Alkohole können zu Aldehyden bzw. Ketonen oxidiert werden; tertiäre Alkohole sind unter normalen Bedingungen nicht oxidierbar. → Mehr dazu
Wie läuft die radikalische Substitution bei Alkanen ab?
Die radikalische Substitution verläuft in drei Schritten: Startreaktion (Homolytische Spaltung der Cl–Cl-Bindung durch UV-Licht → 2 Cl•), Kettenreaktion (Cl• + CH₄ → CH₃• + HCl; CH₃• + Cl₂ → CH₃Cl + Cl•) und Abbruchreaktion (zwei Radikale verbinden sich). Das Verhältnis der Produkte hängt von den Reaktionsbedingungen ab. → Radikalische Substitution
Lernkarten – Organische Chemie Klasse 10
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist ein Alkan? Gib die allgemeine Summenformel an.
Kohlenwasserstoff mit ausschließlich Einfachbindungen (gesättigt).
Allg. Formel: CₙH₂ₙ₊₂
Beispiele: Methan CH₄, Ethan C₂H₆, Propan C₃H₈2Welche funktionellen Gruppen kennzeichnen Aldehyde und Ketone? Worin unterscheiden sie sich?
Beide besitzen die Carbonylgruppe C=O.
Aldehyd: C=O am Kettenende (R–CHO)
Keton: C=O in der Kette (R–CO–R')
→ Aldehyde sind oxidierbar, Ketone nicht.3Warum haben Alkohole höhere Siedepunkte als Alkane gleicher Kettenlänge?
Die –OH-Gruppe ermöglicht die Ausbildung von
Wasserstoffbrückenbindungen zwischen den Molekülen.
Diese sind stärker als die Van-der-Waals-Kräfte der Alkane
→ höhere Siedetemperatur4Was ist eine elektrophile Addition? An welchem Bindungstyp läuft sie ab?
Addition an die C=C-Doppelbindung (Alkene).
Ein Elektrophil (e−-armes Teilchen) greift die π-Elektronen an.
Beispiel: Ethen + HBr → Bromoethan
(Markownikow-Regel bei unsymmetrischen Alkenen)5Gib Summenformeln und funktionelle Gruppen für Ethanol, Ethanal und Ethansäure an.
Ethanol: C₂H₆O · –OH (Hydroxylgruppe)
Ethanal: C₂H₄O · –CHO (Aldehydgruppe)
Ethansäure: C₂H₄O₂ · –COOH (Carboxylgruppe)
Oxidationsreihe: Alkohol → Aldehyd → CarbonsäureWeiter auf w-hoelzel.de
← Chemie – 9. Klasse → Chemie – Kursstufe
📚 Verwandte Kursstufen-Themen: Cycloalkane & Aromaten · Gleichgewichtsreaktionen (Estergleichgewicht) · Naturstoffe I (Kohlenhydrate, Ester) · Naturstoffe II (Aminosäuren, Enzyme)
-
3.1 Ethin (Acetylen)
3.1 Ethin (Acetylen)
3.1.1 Eigenschaften
a) physikalische Eigenschaften
- farbloses Gas (geruchslos)
- leichter als Luft
- Smp.: -80,8°C
- Sdp.: - 84°C (Sublimation)
b) chemische
- brennt mit stark leuchtender und rußender Flamme
- entfärbt Bromwasser
- bildet mit Luft ein explosives Gemisch
- zerfällt unter Druck explosionsartig (⇨ nicht in Druckflaschen)
3.1.2 FormelermittlungVerbrennungsprodukte: H₂O, CO₂ (und bei unvollständiger Verbrennung C)
Molare Masse: M(Ethin) = 26 g/mol
Ermittel aus der molaren Masse die Summen- und die Strukturformel:
{slider title="Lösung" open="false" class="icon"}
Summenformel: C₂H₂
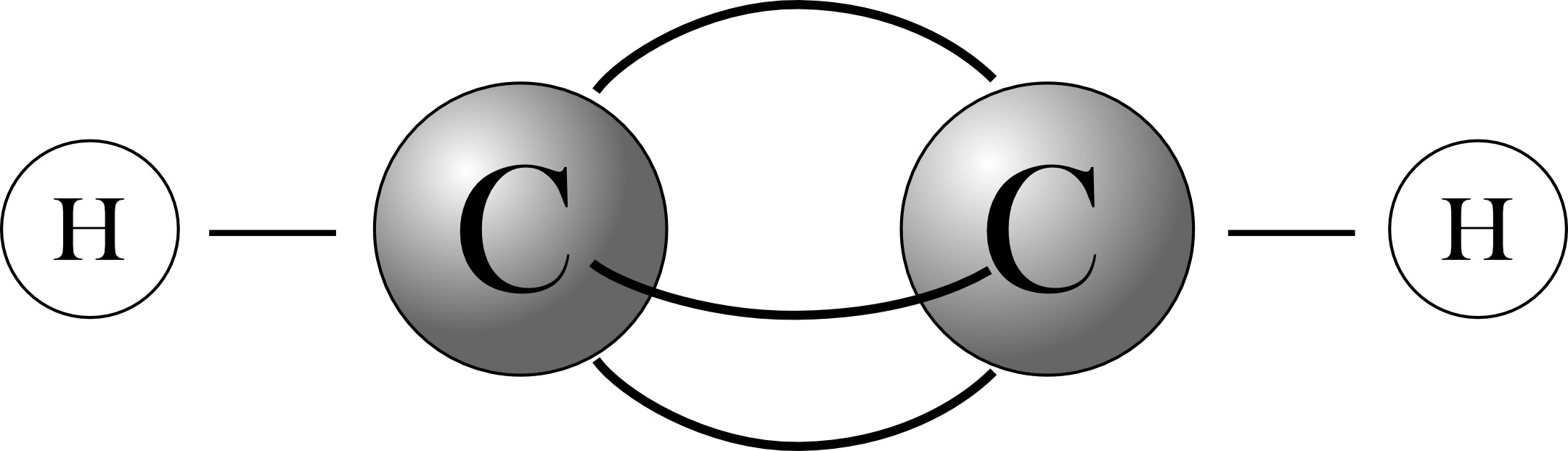
Strukturformel:
(linear; Bindungswinkel 180°)Bindungslänge noch geringer als bei der Doppelbindung (C=C: 134 pm; C=-C: 120 pm)
Ballmodell:3 „Bananenbindungen“, alle 4 Atome sind linear angeordnet.
{/sliders}
-
3.2 Reaktionstyp bei Alkinen
3.2 Reaktionstyp bei Alkinen
Wie bei Doppelbindungen ⇨ Additionsreaktionen
a) Addition von Halogene
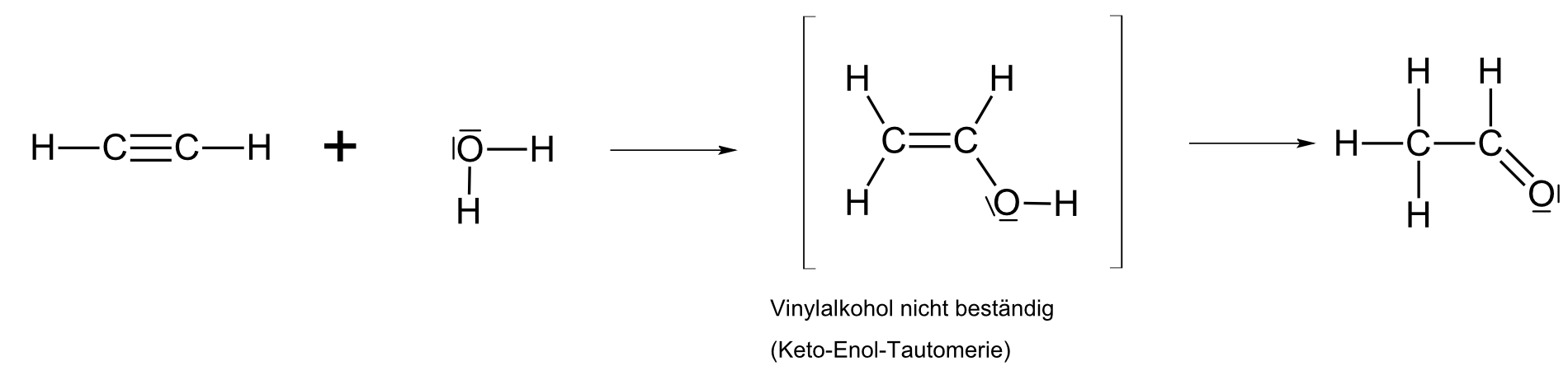
b) mit Wasser
Es gibt viele weitere Reaktionen, die technisch genutzt werden.
Überungsaufgaben
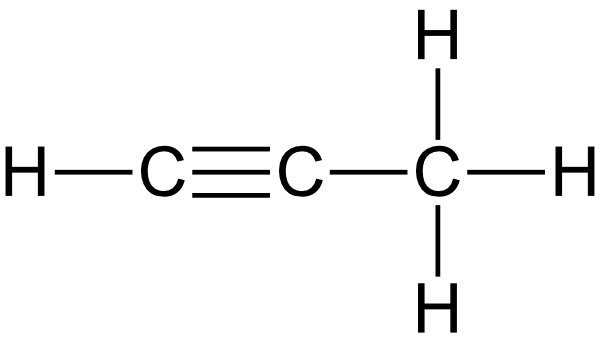
1. Gib alle möglichen Strukturformeln von Propin und Butin an (nur eine Mehrfachbindung).{slider title="Lösung" open="false" class="icon"}
Propin:
Butin:
2-Butin oder But-2-in
1-Butin oder But-1-in
{/sliders}
2. Formuliere die Reaktionsgleichungen für
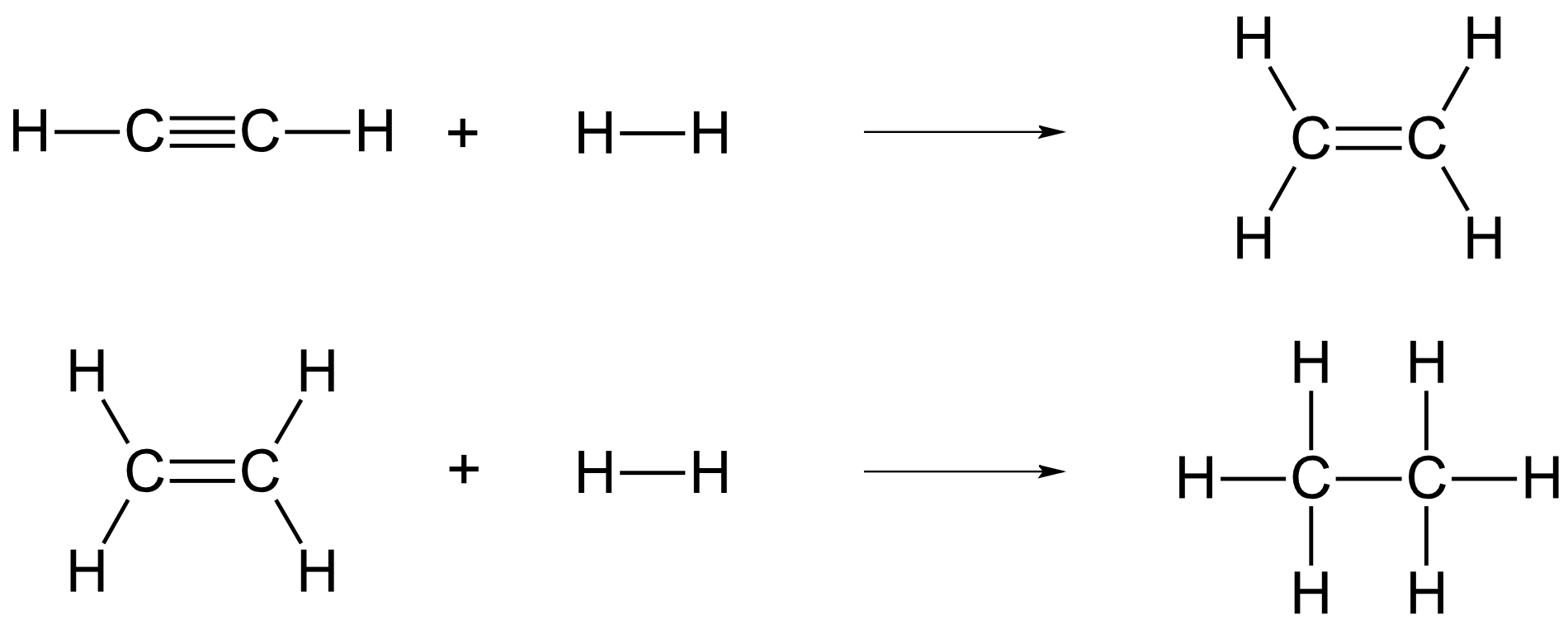
a) die Reaktion von Ethin zu Ethen und dann zu Ethan;
{slider title="Lösung" open="false" class="icon"}
{/sliders}
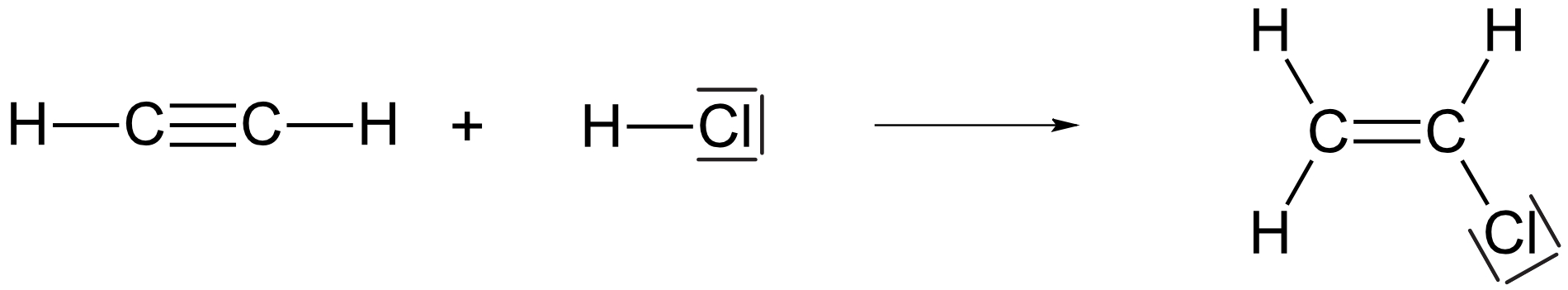
b) die Herstellung von Chlorethen aus Ethin.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
3. Bei Alkenen findet man die cis-trans-Isomerie. Gibt es das auch bei Alkinen?
{slider title="Lösung" open="false" class="icon"}
Nein, da an den beiden C-Atomen der C-C-Dreifachbindung sich nur je ein Atom/Atomgruppe befindet und der Bindungswinkel 180° beträgt. Es gibt somit keine "gegenüberliegende" Seite.
{/sliders}
4. Ethin wird heute vorwiegend durch unvollständige Verbrennung von Methan hergestellt. Formuliere die Reaktionsgleichung als Summenformel.{slider title="Lösung" open="false" class="icon"}
4 CH₄ (g) + 3 O₂ (g) → 2 C₂H₂ (g) + 6 H₂O (g)
{/sliders}