Atombau/Valenzelektronen
-
2.6 Das Periodensystem der Elemente (PSE) und die Atommodelle
Was du auf dieser Seite lernst
Das Periodensystem der Elemente (PSE) ordnet alle bekannten Elemente nach ihrer Ordnungszahl und gibt dir auf einen Blick Auskunft über Atommasse, Elektronenkonfiguration, Schalen und Valenzelektronen. Du lernst, wie das PSE aufgebaut ist, was Gruppen und Perioden bedeuten und wie du Valenzelektronen ablesen kannst.
Grundlagen aus der 9. Klasse
Um das PSE zu verstehen, solltest du Protonen, Elektronen und Neutronen sowie Elektronenschalen kennen: → 2.3 Rutherford-Modell · → 2.4 Bohr-Schalenmodell · → 2.5 Kugelwolkenmodell
Das Periodensystem der Elemente (PSE)
Periodensystem – Nur Hauptgruppenelemente
↑ Zum Vergrößern klicken · Farben: Alkalimetalle Erdalkalimetalle Metalloide Nichtmetalle Halogene Edelgase
Das Periodensystem der Elemente ist eine große Hilfe, um Voraussagen bezüglich chemischer Reaktionen zu treffen und Eigenschaften zu benennen. Man muss es nicht auswendig lernen – wichtig ist, es lesen zu können.
Ursprünglich wurden die Elemente nach steigender Atommasse geordnet. Heute erfolgt die Anordnung nach der Ordnungszahl (= Kernladungszahl = Anzahl der Protonen) und nach periodisch wiederkehrenden Ähnlichkeiten in den Eigenschaften.
Ordnungsprinzipien
- Reihenfolge: Die Elemente sind nach steigender Ordnungszahl (Anzahl der Protonen = Anzahl der Elektronen) angeordnet.
- Periode (= Zeile): Die Periodennummer gibt die Anzahl der Elektronenschalen an.
Beispiel: H, He → 1 Schale · Li…Ne → 2 Schalen · Na…Ar → 3 Schalen - Gruppe (= Spalte): Elemente mit gleicher Anzahl an Außenelektronen (Valenzelektronen) stehen in einer Gruppe.
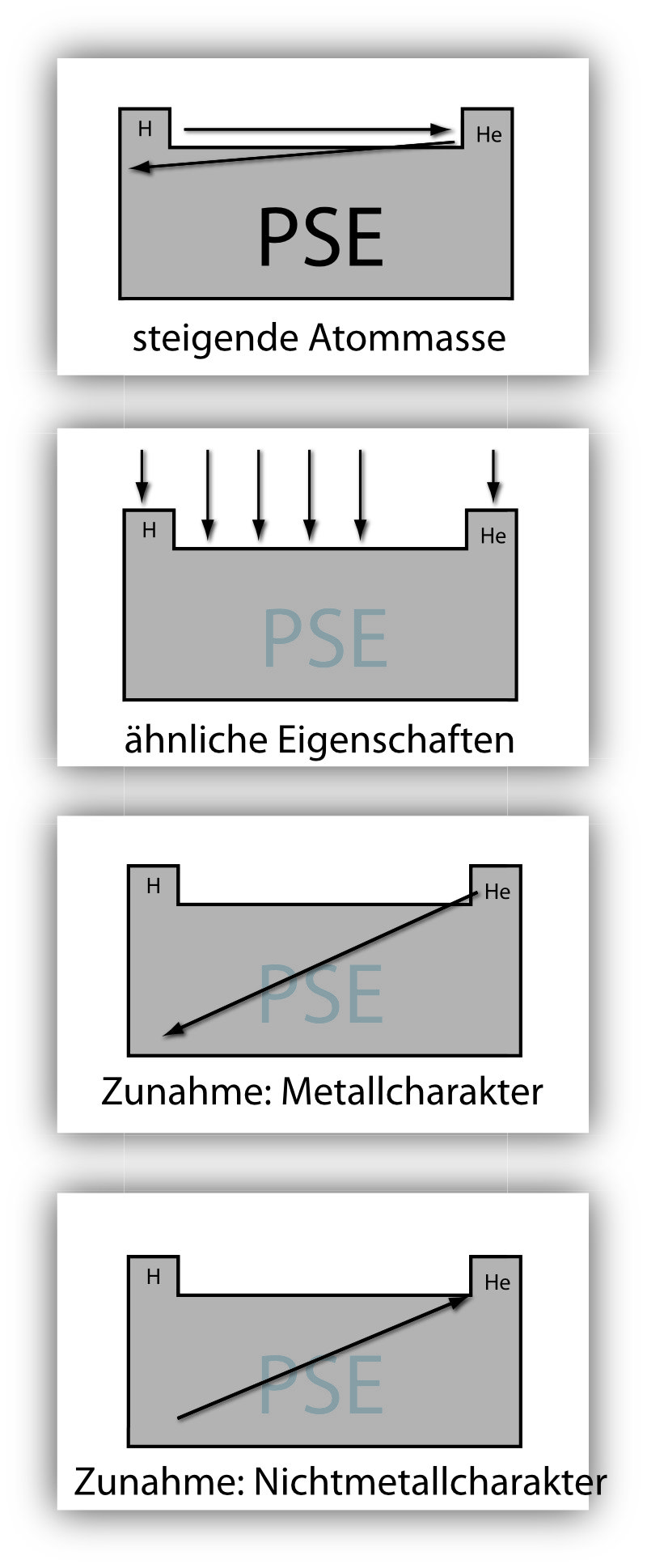
↑ PSE-Symbol-Erklärung – zum Vergrößern klicken
Bedeutung des PSE
- Voraussage damals unbekannter Elemente (z. B. Germanium – von Mendeleev 1871 vorausgesagt, 1886 entdeckt).
- Ablesen von physikalischen und chemischen Eigenschaften aus der Stellung im PSE.
- Das Kurzperiodensystem enthält nur die Hauptgruppenelemente.
Was bedeuten die Felder eines PSE-Eintrags?
Klicke auf ein farbiges Feld der Elementbox, um zu erfahren, was es bedeutet. Beispiel: Aluminium (Al, Z = 13)
26,981538[Ne]3s²3p¹13 Al6611,5 24676,0Aluminium← Klicke auf ein Feld der Elementbox
🟠 Relative Atommasse (oben) Die relative Atommasse (in u, früher: atomare Masseneinheit) gibt an, wie schwer ein Atom im Verhältnis zu 1/12 des Kohlenstoff-12-Atoms ist. Bei Aluminium: 26,98 u. Sie ist kein ganzzahliger Wert, weil verschiedene Isotope des Elements in der Natur vorkommen und gemittelt werden.⬜ Elektronenkonfiguration Die Elektronenkonfiguration [Ne]3s²3p¹ zeigt, auf welchen Orbitalen die Elektronen des Atoms verteilt sind. [Ne] bedeutet: die Konfiguration des Edelgases Neon ist bereits vollständig besetzt. Dann kommen noch 3s² (2 Elektronen im s-Orbital der 3. Schale) und 3p¹ (1 Elektron im p-Orbital). Das ist Kursstufen-Wissen – in Klasse 9 reicht die Schalen-Angabe.🟢 Elementsymbol und Ordnungszahl Das Elementsymbol (hier: Al) besteht aus 1–2 Buchstaben: 1. Buchstabe immer großgeschrieben, 2. Buchstabe immer klein. Die kleine Zahl links oben (hier: 13) ist die Ordnungszahl (= Kernladungszahl = Anzahl der Protonen = Anzahl der Elektronen im neutralen Atom).🔵 Schmelz-/Siedepunkt und weitere Daten Die vier Zahlen im mittleren Bereich geben (je nach PSE) an:
661 = Schmelzpunkt in °C · 2467 = Siedepunkt in °C
1,5 = Elektronegativität (EN) nach Pauling · 6,0 = weitere Eigenschaft (EN-Skala oder Ionisierungsenergie – je nach PSE-Version). Diese Werte sind für Klasse 9 noch weniger wichtig.🔵 Elementname Der vollständige Name des Elements (hier: Aluminium). Im PSE steht er meist unten. Die Valenzelektronen (Außenelektronen) kannst du aus der Hauptgruppe ablesen: Aluminium steht in der 3. Hauptgruppe → hat 3 Valenzelektronen.Elementarteilchen aus dem PSE ablesen
Mit Hilfe des PSE können wir sehr schnell die Anzahl der einzelnen Elementarteilchen bestimmen. Wichtig ist dabei: Im PSE sind die Elemente immer so notiert, dass sie elektrisch neutral sind.
Beispiel: Natrium 23₁₁Na
Größe Ableitung aus PSE Wert für Na Kernladungszahl (Z) = Ordnungszahl = Anzahl der Protonen = Anzahl der Elektronen 11 Nukleonenzahl (A) = Anzahl der Protonen + Anzahl der Neutronen 23 Neutronen = Nukleonenzahl − Kernladungszahl = 23 − 11 12 Merke: Da das Atom elektrisch neutral ist → Anzahl Protonen (11+) = Anzahl Elektronen (11−) → Ladung = 0
⚠️ Die Nukleonenzahl im PSE ist ein gerundeter Wert (relative Atommasse). Für exakte Berechnungen wird der ganzzahlige Wert des häufigsten Isotops verwendet.Übungen: Elementarteilchen aus dem PSE ablesen
Überlege zunächst selbst, dann klappe die Lösung auf.
Afg. 1 Nenne die Anzahl der Elektronen von Kohlenstoff (C).
Lösung: C hat die Ordnungszahl 6 → 6 Elektronen (= 6 Protonen, da elektrisch neutral).Afg. 2 Nenne die Anzahl der Protonen von Brom (Br).
Lösung: Br hat die Ordnungszahl 35 → 35 Protonen.Afg. 3 Nenne die Anzahl der Neutronen von Schwefel (S, Nukleonenzahl 32).
Lösung: S: Ordnungszahl = 16 (Protonen), Nukleonenzahl ≈ 32 → Neutronen = 32 − 16 = 16 Neutronen.Afg. 4 Wie groß ist die Masse von einem Bor-Atom (B)?
Lösung: Die relative Atommasse von B beträgt ca. 10,81 u (aus dem PSE ablesbar).Afg. 5 Nenne das Symbol und die Anzahl der Protonen von Gallium.
Lösung: Symbol: Ga · Ordnungszahl: 31 Protonen.Perioden = Anzahl der Elektronenschalen
Niels Bohr zeigte, dass sich die Elektronen auf unterschiedliche Energieniveaus (= „Schalen") verteilen. Diese Anzahl der Schalen findest du auch im PSE wieder – nämlich in der Angabe der Zeile (= Reihe = Periode).
H, He → Periode 1 → 1 Schale (K-Schale)Li … Ne → Periode 2 → 2 Schalen (K, L)Na … Ar → Periode 3 → 3 Schalen (K, L, M)Rb, Sr … → Periode 5 → 5 Schalen🔑 Merke: Die Periodennummer im PSE = die Anzahl der besetzten Elektronenschalen des Atoms.
Übungen: Perioden und Elektronenschalen
Afg. 1 Nenne alle Elemente, die nur 1 Energieniveau/Schale besitzen.
Lösung: H (Wasserstoff) und He (Helium) – beide stehen in Periode 1 → 1 Schale (K-Schale).Afg. 2 Wie viele „Schalen" besitzt Phosphor (P)?
Lösung: P steht in Periode 3 → 3 Schalen (K, L, M-Schale).Afg. 3 Wie viele Energieniveaus besitzt Xenon (Xe)?
Lösung: Xe steht in Periode 5 → 5 Energieniveaus.Afg. 4 Wie viele Elektronenschalen besitzt Sauerstoff (O)?
Lösung: O steht in Periode 2 → 2 Schalen (K- und L-Schale).Haupt- und Nebengruppenelemente
Im PSE unterscheidet man zwei Typen von Elementen:
Hauptgruppenelemente (grün)
Die Elemente der 1., 2. und 13.–18. Gruppe. Sie unterscheiden sich stärker voneinander. Ihre Anzahl an Valenzelektronen ist direkt aus der Hauptgruppennummer ablesbar. Im Kurzperiodensystem sind nur Hauptgruppenelemente enthalten.
Nebengruppenelemente (grau)
Die Elemente der 3.–12. Gruppe (Übergangsmetalle). Sie besitzen entweder 1 oder 2 Außenelektronen und sind sich chemisch recht ähnlich. Auf den folgenden Seiten werden sie zunächst „weggeschnitten", um mehr Platz zu haben.
Hauptgruppen-Namen: I. HG: Alkalimetalle · II. HG: Erdalkalimetalle · III. HG: Borgruppe · IV. HG: Kohlenstoffgruppe · V. HG: Stickstoffgruppe · VI. HG: Chalkogene (Erzbildner) · VII. HG: Halogene (Salzbildner) · VIII. HG: Edelgase
⚠️ Metallischer vs. nichtmetallischer Charakter: Metallischer Charakter nimmt nach links unten zu · Nichtmetallischer Charakter nimmt nach rechts oben zu · Halbmetalle stehen diagonal dazwischen.
Valenzelektronen und Hauptgruppennummer
Innerhalb einer Hauptgruppe stehen häufig chemisch sich ähnelnde Elemente. Für die chemischen Eigenschaften sind vor allem die Außenelektronen (= Valenzelektronen) verantwortlich.
Die Hauptgruppennummer (gelb unterlegt im PSE) gibt die Anzahl der Valenzelektronen wieder. „Chemie ist die Physik der Valenzelektronen!"
1. HauptgruppeH, Li, Na, K, Rb, Cs, Fr1Valenzelektron2. HauptgruppeBe, Mg, Ca, Sr, Ba, Ra2Valenzelektronen3. HauptgruppeB, Al, Ga, In, Tl3Valenzelektronen7. HauptgruppeF, Cl, Br, I, At7Valenzelektronen8. HauptgruppeHe, Ne, Ar, Kr, Xe, Rn8Valenzelektronen (Edelgase)🔑 Merke: H ist in der 1. HG → 1 Valenzelektron · O ist in der 6. HG (VIA) → 6 Außenelektronen · Edelgase haben 8 Valenzelektronen (He: 2) → besonders stabil (→ Edelgasregel)
Übungen: Valenzelektronen und Hauptgruppenelemente
Für diese Übungen benötigst du das PSE. Bei Klassenarbeiten (und im Abitur) darf es verwendet werden.
Afg. 1 Wie viele Außenelektronen besitzt Rubidium (Rb)?
Lösung: Rb steht in der 1. Hauptgruppe → 1 Außenelektron.Afg. 2 Wie viele Valenzelektronen hat Stickstoff (N)?
Lösung: N steht in der 5. Hauptgruppe (VA) → 5 Valenzelektronen.Afg. 3 Wie viele Valenzelektronen hat Aluminium (Al)?
Lösung: Al steht in der 3. Hauptgruppe → 3 Valenzelektronen.Afg. 4 Wie viele Außenelektronen besitzt die 4. Hauptgruppe?
Lösung: Alle Elemente der 4. HG (C, Si, Ge, Sn, Pb, Fl) haben 4 Außenelektronen.Afg. 5 Wie viele Außenelektronen besitzt Calcium (Ca)?
Lösung: Ca steht in der 2. Hauptgruppe → 2 Außenelektronen.Afg. 6 Wie viele Valenzelektronen hat Chlor (Cl)?
Lösung: Cl steht in der 7. Hauptgruppe (VIIA / Halogene) → 7 Valenzelektronen.Afg. 7 Wie viele Valenzelektronen hat Helium (He)?
Lösung: He ist ein Edelgas (8. HG) – aber eine Ausnahme: es hat nur 2 Valenzelektronen (K-Schale voll mit 2e).Afg. 8 Wie viele Außenelektronen besitzt die 8. Hauptgruppe (Edelgase)?
Lösung: Alle Edelgase (außer He) haben 8 Außenelektronen → vollständig besetzte Außenschale → besonders stabil → kaum Reaktionen.📥 PSE zum Downloaden: Periodensysteme (PSE) herunterladen → (Bei Klassenarbeiten und im Abitur darf das PSE verwendet werden.)
Auf einen Blick – die wichtigsten Aussagen
Ordnungszahl
Die Ordnungszahl = Kernladungszahl = Anzahl der Protonen = Anzahl der Elektronen (neutral).
Periode
Die Periodennummer = Anzahl der besetzten Elektronenschalen (Energieniveaus).
Hauptgruppe
Die Hauptgruppennummer = Anzahl der Valenzelektronen (Außenelektronen). Entscheidet über chemische Eigenschaften.
Nukleonenzahl
Nukleonenzahl = Protonen + Neutronen. Neutronen = Nukleonenzahl − Ordnungszahl.
Häufige Fragen – PSE und Atombau
Wie lese ich die Ordnungszahl, Atommasse und Valenzelektronen aus dem PSE ab?
Die Ordnungszahl steht oben links beim Elementsymbol (= Anzahl der Protonen). Die relative Atommasse steht meist oben im Feld. Die Valenzelektronen (Außenelektronen) entsprechen direkt der Hauptgruppennummer. Beispiel: Chlor (Cl) steht in der 7. Hauptgruppe → 7 Valenzelektronen, Ordnungszahl 17 → 17 Protonen, 17 Elektronen.
Was ist der Unterschied zwischen Gruppe und Periode im PSE?
Eine Periode ist eine waagerechte Zeile. Die Periodennummer gibt an, wie viele Elektronenschalen das Atom hat. Eine Gruppe (= Spalte) fasst Elemente mit gleicher Anzahl an Valenzelektronen zusammen – sie haben daher ähnliche chemische Eigenschaften. Beispiel: Alle Alkalimetalle (1. HG) haben 1 Valenzelektron und reagieren ähnlich mit Wasser.
Was sind Valenzelektronen und warum sind sie wichtig?
Valenzelektronen (= Außenelektronen) befinden sich auf der äußersten besetzten Elektronenschale. Sie sind entscheidend für alle chemischen Reaktionen, weil Atome bevorzugt ihre äußere Schale vollständig besetzen wollen (→ Edelgasregel). Die Anzahl der Valenzelektronen ist direkt aus der Hauptgruppennummer ablesbar.
Wie berechne ich die Anzahl der Neutronen eines Atoms?
Neutronen = Nukleonenzahl − Ordnungszahl (= Nukleonenzahl − Protonenzahl). Beispiel: Natrium ²³Na → Nukleonenzahl 23, Ordnungszahl 11 → 23 − 11 = 12 Neutronen. Achtung: Die im PSE angegebene Atommasse ist ein Mittelwert über alle Isotope – für die Neutronenberechnung nimmt man den gerundeten ganzzahligen Wert.
Was ist der Unterschied zwischen Haupt- und Nebengruppenelemente?
Hauptgruppenelemente stehen in Gruppe 1–2 und 13–18. Die Hauptgruppennummer entspricht direkt der Anzahl der Valenzelektronen. Nebengruppenelemente (Gruppen 3–12, Übergangsmetalle wie Eisen, Kupfer, Zink) haben meistens 1–2 Valenzelektronen. Im Kurzperiodensystem werden Nebengruppen oft weggelassen. → 2.7 Lewis-Formeln
Lernkarten – PSE und Atombau
Klicke auf eine Karte, um die Antwort zu sehen.
1Was gibt die Ordnungszahl im PSE an?
Ordnungszahl = Anzahl der Protonen = Anzahl der Elektronen (im neutralen Atom) = Kernladungszahl.
2Was sagt die Periode (Zeile) im PSE aus?
Die Periodennummer = Anzahl der besetzten Elektronenschalen (Energieniveaus) des Atoms.
3Wie viele Valenzelektronen hat Chlor? Wie liest du das ab?
Cl steht in der 7. Hauptgruppe → 7 Valenzelektronen. Hauptgruppennummer = Anzahl der Valenzelektronen.
4Wie berechnet man die Anzahl der Neutronen?
Neutronen = Nukleonenzahl − Ordnungszahl. Beispiel: Na ²³Na → 23 − 11 = 12 Neutronen.
5Wie viele Valenzelektronen haben Edelgase und warum sind sie so stabil?
Edelgase haben 8 Valenzelektronen (He: 2) → vollständig besetzte Außenschale → energetisch sehr stabil → kaum Reaktionen (→ Edelgasregel).
Weiter im Kapitel: Atombau und PSE
← 2.5 Kugelwolkenmodell → 2.7 Lewis-Formeln → 3. Edelgasregel
🔁 Grundlagen: Rutherford · Bohr-Schalenmodell · Kugelwolkenmodell · PSE herunterladen
-
2.7 Lewis – Formeln für Moleküle
Was du auf dieser Seite lernst
Die Lewis-Formel (= Valenzstrichformel) zeigt die Außenelektronen (Valenzelektronen) eines Atoms als Punkte und Striche. Du lernst die Regeln, zeichnest die Lewis-Formeln für alle Elemente der ersten drei Perioden und erkennst den Zusammenhang mit dem Periodensystem.
Grundlagen aus der 9. Klasse
Für Lewis-Formeln musst du die Valenzelektronen kennen: → 2.6 PSE und Valenzelektronen · → 2.5 Kugelwolkenmodell · → 3. Edelgasregel
2.7 Lewis-Formeln – Regeln zum Aufstellen
Teil I: Für einzelne Atome
Man zeichnet an jedes Atom die Außenelektronen (Valenzelektronen) als Punkte und Striche:
Regel 1 – Einfach besetztes Orbital (ein Elektron) → · Punkt
Regel 2 – Doppelt besetztes Orbital (Elektronenpaar) → – Strich
Regel 3 – Reihenfolge: Zunächst wird jede Seite des Symbols (oben, rechts, unten, links) einzeln belegt (Hund'sche Regel), bevor ein zweites Elektron dazukommt. Die Elektronen der inneren Schalen werden nicht gezeichnet.
Teil II: Für Moleküle
Für Moleküle gelten zusätzlich:
- Die Elementsymbole werden entsprechend ihrer Verknüpfung im Molekül angeordnet.
- Zwischen den Atomen werden so viele bindende Elektronenpaare gebildet, dass alle Atome die Edelgasregel erfüllen (→ Oktettregel).
- Dabei sind Einfach- und Mehrfachbindungen möglich.
- Bindende und nichtbindende Elektronenpaare werden durch einen Strich ersetzt.
🔗 Verbindung zum Kugelwolkenmodell: Einfach besetzte Kugelwolken (grün im KWM) = Punkt · · Doppelt besetzte Kugelwolken (rot im KWM) = Strich – . Damit direkt aus dem KWM ableitbar!Übung: Lewis-Formeln der ersten drei Perioden
Am einfachsten versteht man es, wenn man zunächst die ersten Elemente der Hauptgruppen zeichnet. Versuche die Lewis-Formeln für alle Elemente der ersten drei Perioden selbst – dann klappe die Lösung auf.
Ein PSE wäre recht hilfreich: → PSE herunterladen
· = 1 Elektron (einfach besetzt) – = 2 Elektronen (doppelt besetzt / Elektronenpaar) Blau = Punkt · Rot = Strich🖊 Interaktiv – Lewis-Formeln Perioden 1–3 → Versuche es erst selbst, dann Lösung einblenden📝 Aufgabe: Zeichne für die Elemente der ersten 3 Perioden (H bis Ar) alle Außenelektronen in der Lewis-Schreibweise (Punkte und Striche). Nutze die Regeln oben.
(Hinweis: Jede der 4 Seiten wird zuerst einfach besetzt, dann doppelt – analog zur Hundschen Regel.)Periode 1 – K-Schale· · H · ·Wasserstoff 1 VE · HG I· · He · ·Helium 2 VE · HG VIIIPeriode 2 – L-Schale· · Li · ·Lithium 1 VE · HG I· · Be · ·Beryllium 2 VE · HG II· · B · ·Bor 3 VE · HG III· · C · ·Kohlenstoff 4 VE · HG IV· · N – ·Stickstoff 5 VE · HG V· – O – ·Sauerstoff 6 VE · HG VI– – F – ·Fluor 7 VE · HG VII– – Ne – –Neon 8 VE · HG VIIIPeriode 3 – M-Schale· · Na · ·Natrium 1 VE · HG I· · Mg · ·Magnesium 2 VE · HG II· · Al · ·Aluminium 3 VE · HG III· · Si · ·Silicium 4 VE · HG IV· · P – ·Phosphor 5 VE · HG V· – S – ·Schwefel 6 VE · HG VI– – Cl – ·Chlor 7 VE · HG VII– – Ar – –Argon 8 VE · HG VIII✅ Muster: Blauer Punkt · = 1 Elektron (einfach besetzt) · Roter Strich – = Elektronenpaar (doppelt besetzt)
🔑 Zusammenhang PSE: Die Hauptgruppennummer = Anzahl der Valenzelektronen = Anzahl der Punkte/Striche insgesamt.Zusammenhang: Lewis-Formel und PSE
Die Lewis-Formel lässt sich direkt aus dem Periodensystem ableiten:
Hauptgruppennummer= Anzahl der Valenzelektronen = Anzahl der Punkte + 2 × Anzahl der Striche
Periode (Zeile)= Anzahl der Elektronenschalen. Nur die äußerste Schale wird in der Lewis-Formel gezeichnet.
Edelgase (HG VIII)8 Valenzelektronen = 4 Striche = vollständig besetzt = besonders stabil → Edelgasregel!
Übungsaufgaben – Lewis-Formeln
Afg. 1 Wie viele Punkte (·) und Striche (–) hat die Lewis-Formel von Sauerstoff (O)?
Lösung: O steht in der 6. Hauptgruppe → 6 Valenzelektronen. In der Lewis-Formel: 2 Punkte (oben und unten, einfach besetzt) + 2 Striche (rechts und links, doppelt besetzt) = 2 Punkte + 2 Striche. Probe: 2×1 + 2×2 = 6 Elektronen ✓Afg. 2 Schreibe die Lewis-Formel für Phosphor (P). Wie viele freie Elektronenpaare hat P?
Lösung: P steht in der 5. Hauptgruppe → 5 Valenzelektronen. Lewis-Formel: 3 Punkte (oben, unten, links) + 1 Strich (rechts) = 3 Punkte + 1 Strich. Freie Elektronenpaare: 1 Paar (der Strich rechts). 3 Elektronen sind für Bindungen verfügbar (P bildet in Molekülen oft 3 Bindungen).Afg. 3 Warum haben Edelgase (z. B. Ne, Ar) keine Punkte in der Lewis-Formel?
Lösung: Edelgase haben 8 Valenzelektronen (He: 2), alle als Paare. Alle 4 Positionen in der Lewis-Formel sind mit Strichen (–) besetzt → keine einzelnen Elektronen mehr. Diese vollständige Besetzung macht Edelgase so stabil (→ Edelgasregel).Afg. 4 Welches Element hat genau 2 Punkte und 2 Striche in der Lewis-Formel?
Lösung: 2 Punkte + 2 Striche = 2×1 + 2×2 = 6 Valenzelektronen → 6. Hauptgruppe. Das sind: O, S, Se, Te (Chalkogene). In unserer Tabelle: Sauerstoff (O) und Schwefel (S).Afg. 5 Zeichne die Lewis-Formel für Stickstoff (N) und erkläre, warum N 3 Bindungen eingehen kann.
Lösung: N (HG V) hat 5 Valenzelektronen → Lewis-Formel: 3 Punkte + 1 Strich. Die 3 einzelnen Elektronen (Punkte) können je mit einem Elektron eines anderen Atoms ein bindendes Elektronenpaar bilden → N geht 3 Bindungen ein (z. B. in NH₃, drei N–H-Bindungen). Das freie Elektronenpaar (Strich) bleibt als nichtbindendes Paar erhalten.
Auf einen Blick – die wichtigsten Aussagen
Punkt ·
Ein Punkt = 1 Elektron in einem einfach besetzten Orbital. Dieses Elektron ist für eine Bindung verfügbar.
Strich –
Ein Strich = 2 Elektronen (Elektronenpaar) in einem doppelt besetzten Orbital. Freies Paar – nicht bindend.
Hauptgruppe
Hauptgruppennummer = Anzahl der Valenzelektronen = Summe aller Punkte und Striche (×2) in der Lewis-Formel.
Edelgasregel
Edelgase: 4 Striche = 8 Elektronen = volle Außenschale. Alle anderen Elemente streben diesen Zustand durch Bindungen an.
Häufige Fragen – Lewis-Formeln
Was ist der Unterschied zwischen einem Punkt und einem Strich in der Lewis-Formel?
Ein Punkt (·) steht für ein einzelnes Elektron in einem einfach besetzten Orbital – dieses Elektron ist für eine chemische Bindung verfügbar. Ein Strich (–) steht für zwei Elektronen (ein Elektronenpaar) in einem doppelt besetzten Orbital – dieses Paar ist normalerweise nicht an Bindungen beteiligt (freies Elektronenpaar). Der Zusammenhang mit dem Kugelwolkenmodell: grüne Kugelwolke (einfach besetzt) → Punkt, rote Kugelwolke (doppelt besetzt) → Strich.
Wie leite ich die Lewis-Formel aus dem PSE ab?
Schritt 1: Hauptgruppennummer ablesen = Anzahl der Valenzelektronen. Schritt 2: Die ersten 4 Elektronen auf die 4 Positionen (oben, rechts, unten, links) je einzeln verteilen (Hund'sche Regel → Punkte). Schritt 3: Vom 5. bis 8. Elektron beginnt die Doppelbesetzung der schon belegten Positionen (Punkte werden zu Strichen).
Warum werden bei Lewis-Formeln nur die Valenzelektronen gezeichnet?
Nur die Elektronen der äußersten Schale (Valenzelektronen) nehmen an chemischen Reaktionen und Bindungen teil. Die Elektronen der inneren Schalen sind viel stärker an den Kern gebunden und stehen nicht für Bindungen zur Verfügung. Bei Kohlenstoff (Z=6) z. B.: 2 Elektronen der K-Schale werden nicht gezeichnet, nur die 4 Valenzelektronen der L-Schale.
Was besagt die Edelgasregel (Oktettregel) in Bezug auf Lewis-Formeln?
Die Edelgasregel besagt: Atome streben einen Zustand mit 8 Valenzelektronen an (Ausnahme: H und He mit 2). In der Lewis-Formel bedeutet das: ein Atom ist „zufrieden", wenn es 4 Striche in seiner Lewis-Formel hat (= 8 Elektronen). Einzelne Elektronen (Punkte) können dazu mit anderen Atomen geteilt werden → chemische Bindung. Mehr dazu: → 3. Edelgasregel
Wozu braucht man Lewis-Formeln?
Lewis-Formeln sind die Grundlage für das Verständnis chemischer Bindungen. Mit ihnen lässt sich vorhersagen: Wie viele Bindungen geht ein Atom ein? Welche Molekülstruktur entsteht? Wo sitzen freie Elektronenpaare (wichtig für die Molekülgeometrie, → VSEPR-Modell in der Kursstufe)? Außerdem zeigen sie direkt, welche Bindungspartner sich gegenseitig zur Edelgaskonfiguration vervollständigen.
Lernkarten – Lewis-Formeln
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeuten Punkte und Striche in einer Lewis-Formel?
· = 1 Elektron (einfach besetzt, für Bindungen verfügbar)
– = 2 Elektronen (Elektronenpaar, freies Paar)2Wie viele Punkte und Striche hat Stickstoff (N) in der Lewis-Formel?
N (HG V, 5 VE): 3 Punkte + 1 Strich. Die 3 Punkte stehen für mögliche Bindungen (z. B. 3 N–H-Bindungen in NH₃).
3Wie lautet die Lewis-Formel für ein Edelgas (z. B. Argon, Ar)?
Ar (HG VIII, 8 VE): 4 Striche, je einer oben, rechts, unten, links. Kein einziger Punkt → keine freien Elektronen für Bindungen → chemisch sehr stabil.
4Wie bestimme ich die Anzahl der Valenzelektronen aus dem PSE?
Hauptgruppennummer = Anzahl der Valenzelektronen. Beispiel: Cl steht in HG VII → 7 Valenzelektronen → Lewis-Formel: 3 Striche + 1 Punkt.
5Welchen Zusammenhang gibt es zwischen Lewis-Formel und Kugelwolkenmodell?
Grüne Kugelwolke (einfach besetzt, 1e) → Punkt ·
Rote Kugelwolke (doppelt besetzt, 2e) → Strich –
Die Lewis-Formel ist eine vereinfachte 2D-Darstellung der äußeren Kugelwolken.Weiter im Kapitel: Atombau und PSE
← 2.6 PSE und Atommodelle → 3. Edelgasregel → 4. Atombindung
🔁 Grundlagen: Kugelwolkenmodell · PSE · PSE herunterladen