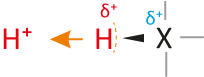
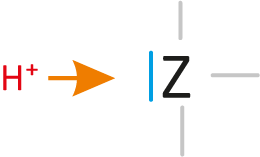
Brønsted
-
2.6 Phenole
2.6 Phenole = Hydroxybenzole
Vorkommen:
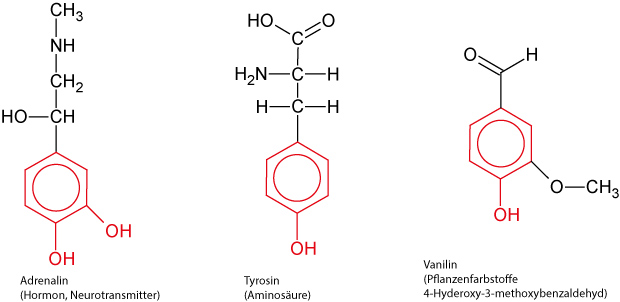
2.6.1 Monohydroxybenzol = Phenol
a) Physikalische Eigenschaften
- Smp.: 40,9; Sdp.: 181,9 °C
- In Wasser nur mäßig löslich (bildet bei ZT eine Emulsion)
- Starkes Zellgift, durch Haut resorbiert
b) Chemische Eigenschaften
- Oxidiert an Luft leicht ⇨ rötliche Färbung
- Karbolsäure“: 2 %ige Säure; Desinfektion
- Im Gegensatz zu Ethanol sauer:
1. Phenol als schwache Säure
pKS = 9,95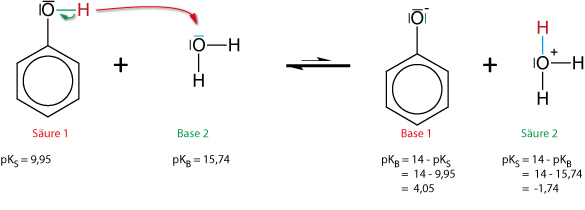
Grenzformeln des Phenolations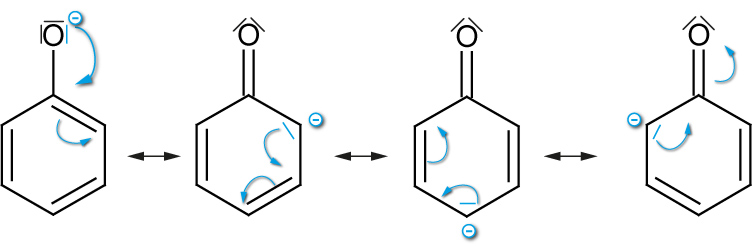
Phenol Ethanol Säurestärke höher niedriger Induktiver Effekt 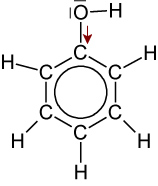
schwacher -I-Effekt ⇨ elektronenziehend
⇨ H⁺-Abgabe ist erleichtert
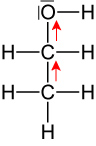
+I-Effekt ⇨ Elektro-nenschiebend
H⁺-Abgabe ist er-schwert.Anion: Mesomeriestabilisiert konjungierte Base (Phenolat): negative Ladung ist über den ganzen Ring delokalisiert ⇨ stabilisiert! Keine Stabilisierung durch Mesomerien Brønsted-Säure stärker schwächer Brønsted-Base schwächer stärker 2.6.3 Synthese
90% der Weltproduktion nach der Hock-Synthese
Wirtschaftliches Verfahren, da auch Aceton nutzbar ist.
siehe Heftaufschrieb
2.6.4 Verwendung
Herstellung von Kunststoffen (Polyamide, Phenoplasten, Phenolharzen und Polycarbonaten)
-
3 Protolyse-Reaktionen
Was du auf dieser Seite lernst
Chlorwasserstoff-Gas (HCl) reagiert mit Wasser zu Oxonium- und Chlorid-Ionen – das ist eine Protolyse-Reaktion nach Brønsted. Du lernst den Springbrunnenversuch zu erklären, Reaktionsgleichungen in Summenformel- und Lewis-Schreibweise aufzustellen und das Protolysen-Schema (Bergab-Reaktion) zu lesen und anzuwenden.
3 Protolyse-Reaktionen
3.1 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
Chlorwasserstoff: Summenformel HCl · polare Atombindung · Gas · stechender Geruch
Wasser: Summenformel H2O · polare Atombindung · Flüssigkeit · geruchslos✕Lewis-Formeln
H — Cl: Chlorwasserstoff H — O: Wasser | H 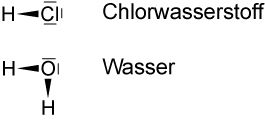
a) Versuch:
↑ Zum Vergrößern klicken
✕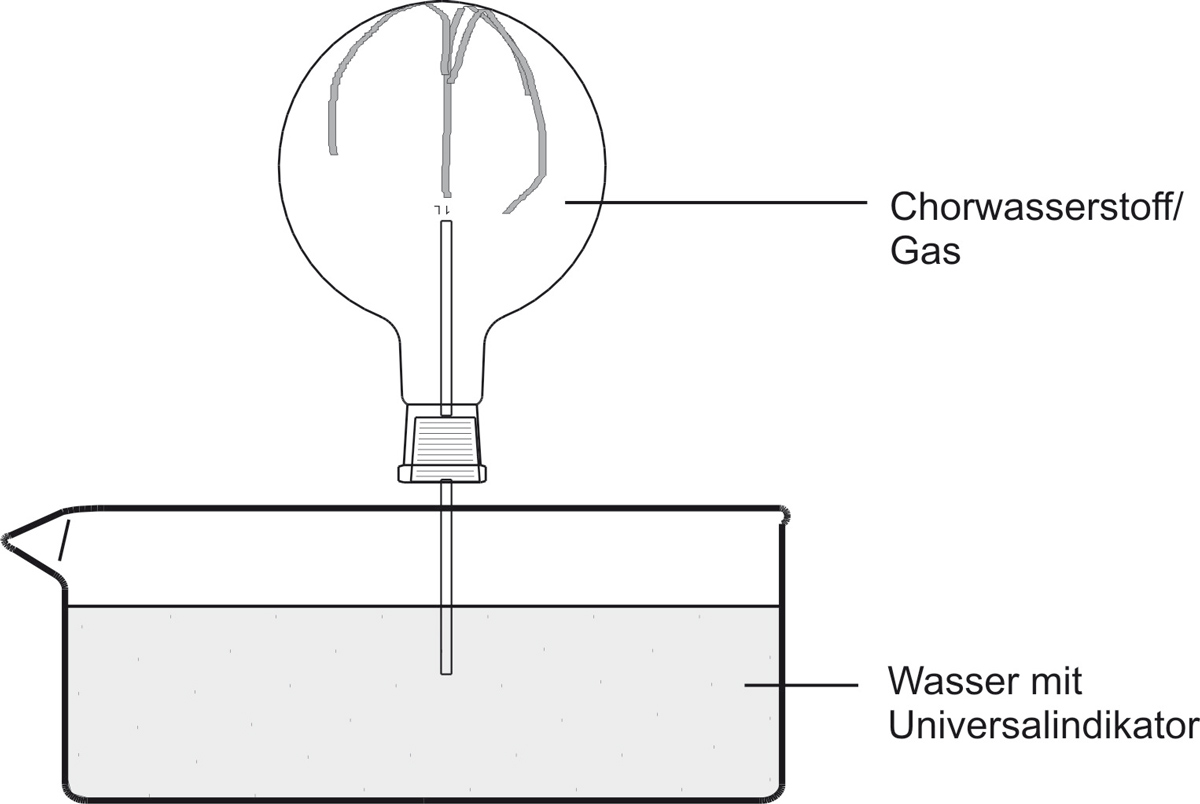
⚠️ Hinweis: Im Bild steht „Chorwasserstoff" – korrekte Schreibweise: Chlorwasserstoff.
b) Beobachtung:
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach rot/gelb um. Die rote wässrige Lösung ist geruchlos.c) Reaktionsgleichung – Struktur/Lewisformel:
Es gibt zwei mögliche Reaktionsgleichungen (wenn man zunächst die Säurestärke vernachlässigt). Welche zwei Reaktionsgleichungen sind das?
{slider title="Lösung" open="false" class="icon"}1. Möglichkeit – HCl als Säure, H2O als Base (korrekte Reaktion):
✕H2O(l) + HCl(g) ⟶ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
⇒ bildet zusammen: „Salzsäure"

2. Möglichkeit – H2O als Säure, HCl als Base:
↑ Zum Vergrößern klicken
✕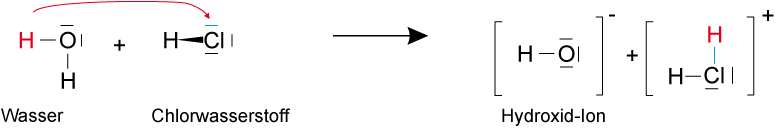
Chlorwasserstoff ist die stärkere Säure, Hydroxid-Ion (OH−) wäre eine sehr starke Base. Durch Elektrolyse wird die 1. Möglichkeit bestätigt: HCl wirkt als Säure.
{/sliders}Nachweis der gebildeten Ionen:
- Leitfähigkeitsmessung: Die Lösung leitet elektrischen Strom → Ionen sind vorhanden.
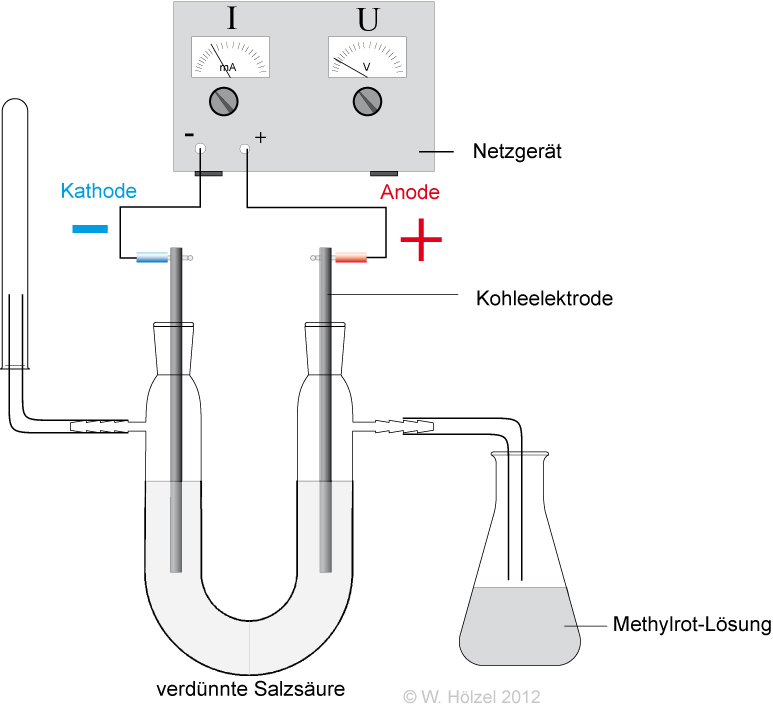
- Elektrolyse: An der Anode (Pluspol) entsteht Cl2-Gas → Chlorid-Ionen (Cl−) müssen vorliegen.
↑ Zum Vergrößern klicken
✕
- Indikator: Bromthymolblau färbt gelb → Oxonium-Ionen (H3O+) sind vorhanden.
Komplette Lösung:
{slider title="Lösung" open="false" class="icon"}Reaktionsgleichung (Lewis-Formel):
↑ Zum Vergrößern klicken
✕
Reaktionsgleichung (Summenformel):
✕H2O(l) + HCl(g) ⇌ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
„Salzsäure"

Verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen sowie Wassermolekule.
d) Protolysen-Schema:
↗ Originalbild des Protolysen-Schemas ansehen
✕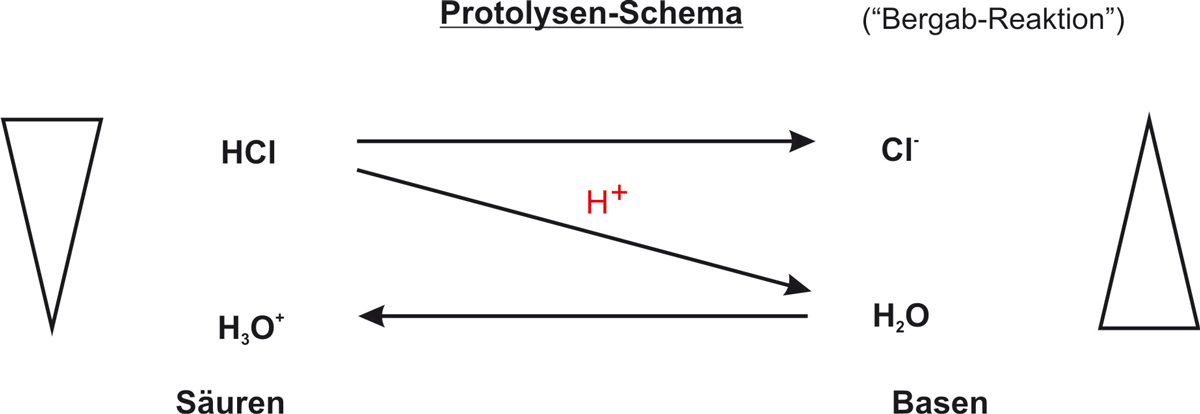 {/sliders}
{/sliders}
e) Erklärung:
Chlorwasserstoff-Gas reagiert mit Wasser zu Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Im Kolben entsteht durch das vollständige Auflösen ein Unterdruck. Die H3O+-Ionen färben den Universalindikator bzw. Bromthymolblau rot/gelb.Salzsäure = wässrige Lösung des Gases Chlorwasserstoff
Leitet man sehr viel HCl-Gas in Wasser ein, reagieren nicht mehr alle HCl-Moleküle mit H2O. Diese HCl-Moleküle liegen „gelöst" vor – es entsteht rauchende bzw. konzentrierte Salzsäure.
Leitfähigkeit Geruch Indikatorpapier Teilchen Verdünnte Salzsäure + − rot H2O, H3O+, Cl− Rauchende Salzsäure + + rot H2O, H3O+, Cl−, HCl
Auf einen Blick – die wichtigsten Aussagen
Protolyse (Brønsted)
Eine Protolyse ist die Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
Springbrunnen
HCl löst sich vollständig in H2O auf → Ionen bilden sich → Unterdruck entsteht → Atmosphärendruck drückt Wasser hoch.
Bergab-Reaktion
Das Proton wandert von der stärkeren Säure (HCl) zur stärkeren Base (H2O) – immer zur schwächeren Säure/Base hin.
Salzsäure
Salzsäure = wässrige Lösung von HCl. Enthält H3O+, Cl− und H2O; konzentriert zusätzlich gelöstes HCl.
Häufige Fragen – Protolyse-Reaktionen
Warum schießt das Wasser beim Springbrunnenversuch in den Kolben?
HCl-Gas reagiert sofort mit dem eingetretenen Wasser zu H3O+- und Cl−-Ionen. Dadurch sinkt der Gasdruck im Kolben stark. Der Atmosphärendruck drückt das Wasser durch das Glasrohr nach oben – der „Springbrunnen-Effekt". Die Indikatorfarbe zeigt: die Lösung ist sauer (H3O+-Ionen).
Was ist der Unterschied zwischen Chlorwasserstoff und Salzsäure?
Chlorwasserstoff (HCl) ist ein farbloses Gas mit stechendem Geruch. Salzsäure ist die wässrige Lösung dieses Gases: HCl löst sich in H2O und bildet dabei Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Verdünnte Salzsäure ist geruchlos, da kein HCl mehr als Gas vorliegt.
Was versteht man unter einer Protolyse nach Brønsted?
Nach Brønsted ist eine Säure ein Protonendonator (gibt H+ ab) und eine Base ein Protonenakzeptor (nimmt H+ auf). Eine Protolyse ist die Übertragung eines Protons. Das Protolysen-Schema zeigt: Die Reaktion läuft stets von der stärkeren Säure/Base zu den schwächeren Produkten – die sogenannte Bergab-Reaktion. Mehr dazu: Brønsted-Definition (Kl. 9).
Wie weist man Chlorid-Ionen in Salzsäure nach?
Durch Elektrolyse: An der Anode (Pluspol) entwickelt sich Chlorgas (Cl2), das durch Oxidation von Cl− entsteht – direkter Nachweis. Außerdem fällt bei Zugabe von Silbernitrat-Lösung (AgNO3) ein weißer Niederschlag aus Silberchlorid (AgCl) aus.
Was enthält rauchende Salzsäure im Vergleich zu verdünnter Salzsäure?
Verdünnte Salzsäure enthält nur H2O, H3O+ und Cl− – alles HCl hat mit Wasser reagiert. In konzentrierter (rauchender) Salzsäure ist so viel HCl gelöst, dass nicht mehr alle Moleküle mit H2O reagieren können. Sie liegen als undissoziiertes HCl vor → stechender Geruch, „Rauchen" an feuchter Luft. Mehr zur Konzentration: Konzentration von Lösungen (Kl. 9).
Lernkarten – Protolyse von Chlorwasserstoff
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Protolyse-Reaktion nach Brønsted?
Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
2Erkläre den Springbrunnenversuch mit HCl!
HCl löst sich schnell in H2O → Ionenbildung → Gasdruck sinkt → Atmosphärendruck drückt Wasser nach oben in den Kolben.
3Warum wirkt HCl als Säure und H2O als Base?
HCl ist die stärkere Säure. Im Protolysen-Schema reagiert immer die stärkere Säure mit der stärkeren Base (Bergab-Reaktion).
4Welche Teilchen enthält verdünnte vs. rauchende Salzsäure?
Verdünnt: H2O, H3O+, Cl−
Rauchend: zusätzlich gelöstes HCl → stechender Geruch5Berechne: Welche Masse HCl (M = 36,5 g/mol) steckt in 250 mL 0,2-mol/L-Salzsäure?
n = c · V = 0,2 mol/L · 0,25 L = 0,05 mol
m = n · M = 0,05 mol · 36,5 g/mol = 1,825 gWeiter im Kapitel Säure-Base-Reaktionen
→ 3.2 Chlorwasserstoff und Ammoniak → Brønsted-Definition → Stärke von Säuren und Basen
🔗 Verwandte Themen: pH-Wert und Oxonium-Ionen · Konzentration von Lösungen · Neutralisation
ⓘ Die verlinkten Seiten wurden nicht gegen die aktuelle Sitemap verifiziert – bitte vor dem Veröffentlichen prüfen.
-
4 Allgemeine Säure-Base-Definition nach Brønsted (1923)
4 Allgemeine Säure-Base-Definition nach Brønsted (1923)
a) Säuren...
... sind Teilchen, die Protonen abgeben können (= Protonendonator, „Protonenspender“).
Die Teilchen enthalten positivierte H-Atome (Die Bindung zum H-Atom muss polar sein):Wasserstoffatome bestehen nur aus Protonen und Elektronen. Eine Säure besitzt ein Wasserstoffatom, wobei das Elektron von dem Wasserstoffatom „stark“ angezogen wird. Kommt es zu einer Säure-Base-Reaktion (Protolyse), dann wird vereinfacht ausgedrückt nur das Proton des Wasserstoffatoms abgegeben. Das Elektron der Wasserstoffatoms bleibt beim Teilchen zurück (vgl. dazu alle vorher genannten Beispiele).
b) Basen...sind Teilchen, die Protonen aufnehmen können (= Protonenakzeptor, „Protonenräuber“). Die Teilchen enthalten mindestens ein freies Elektronenpaar.
Dieses freie Elektronenpaar „nimmt“ dann den positiven Wasserstoffkern (Proton) „auf“.
c) Übung
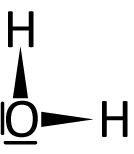
Im folgenden ist die Lewis-Formel (Strukturformel) von Wasser abgebildet. Gehört dieses Molekül zu einer Brønsted-Säure oder -Base? Schaut Euch dafür nochmals die Definitionen an.
{slider title="Lösung: Was ist Wasser? Eine Säure oder Base?" open="false" class="icon"}
Wasser kann (je nach Reaktionspartner) beides sein. Es kann ein Proton (H⁺) abgeben [es hat ja positivierte Wasserstoff-Atome], wie auch aufnehmen [es hat ja auch freie Elektronenpaare].
Dafür gibt es eine neue Bezeichnung: Wasser ist ein Ampholyt.
{/sliders}
c) Ampholyte
Ampholyte können sowohl als Säuren, wie auch als Basen reagieren. Sie müssen also freie Elektronenpaare (für die Funktion als Basen) wie auch positivierte Wasserstoff-Atome (Funktion als Säure) besitzen.
-
5 Stärke von Säuren und Basen
5 Stärke von Säuren und Basen - Säurestärke und Molekülstruktur
Hinweis 1: Das Kapitel stammt aus dem Oberstufenbereich. Ich halte es für das Verständnis für Säure-Base-Reaktionen wichtig, weil man sonst bei einer Reaktion mit zwei Ampholyten (z.B. Wasser und Ammoniak) gar nicht weiß, wer die Säure ist und wer als Base funktioniert.
Hinweis 2: Auch hier ist es von Vorteil, wenn man ein Periodensystem der Elemente zur Hand hat.
Brønsted-Theorie:
Säurestärke ist die Tendenz Protonen abzugeben.
Basenstärke Tendenz Protonen aufzunehmen.Bsp. HCl + H₂O → H₃O⁺ + Cl⁻
Säure 1 Base 2 Säure 2 Base 1Info: Supersäuren = Säuren die stärker als H₂SO₄ sind.
Je stärker die Säure desto schwächer die konjugierte (korrespondierende) Base.
5.1 Binäre Säuren.
Faktoren für Säurestärke von Bedeutung:
- Elektronegativität (innerhalb einer Periode)
- Atomgröße (innerhalb einer Gruppe)
a) innerhalb einer Periode (binäre H-Verbindungen)
Säurestärke nimmt mit der EN zu (Atomgrößenunterschiede sind „zu“ gering)
⇨ Elektronen werden stärker dem H-Atom entzogen ⇨ erleichterte Protonenabspaltung.Bsp.:
2. Periode:
Zunahme der EN: N < O < F
Zunahme der Säurestärke NH₃ < H₂O < HF
Gegenüber Wasser Base Säure
3. Periode
Zunahme der EN: P < S < Cl
Zunahme der Säurestärke PH₃ < H₂S < HCl
b) innerhalb einer Gruppe (binäre H-Verbindungen):
Säurestärke nimmt mit der Atomgröße zu (stärkere Auswirkung als Elektronegativität)
⇨ bei einem großen Atom ist die Valenzelektronenwolke auf einem größeren Raum verteilt ⇨ H⁺ ist weniger fest gebunden.H₂O < H₂S < H₂Se < H₂Te
HF < HCl < HBr < HI5.2 Oxosäuren
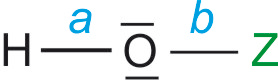
Sauerstoff hat in etwa die gleiche Größe
a) EN von Z ist entscheidend.
Je größer die EN von Z, desto stärker ist die Säure (-I-Effekt).HOI < HOBr < HOCl
hyopoiodige Säure hypobromige hypochlorige Säureb) An Z sind weitere O-Atome gebunden ⇨ stärkerer –I-Effekt (bzw. höhere Formalladung am Z. )
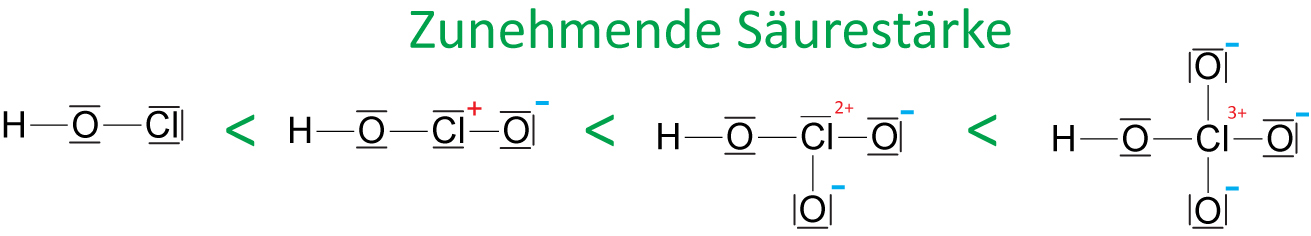
hypochlorige – chlorige – Chlor – Perchlorsäuren
⇨ Man kann Säurestärke abschätzen: Je mehr mehr O-Atome an das Z-Atom jedoch nicht an H-Atom gebunden sind, desto die Säure:
H-O-NO < H-O-NO₂
salpetrige Säure Salpetersäure
(H-O-)₂SO < (H-O-)₂SO₂
schweflige Säure Schwefelsäure -
5. Indikatoren
Was du auf dieser Seite lernst
Du lernst, wie Säure-Base-Indikatoren funktionieren und warum ihr Farbumschlag beim pKS-Wert der schwachen Indikatorsäure liegt. Mit der Henderson-Hasselbalch-Gleichung berechnest du das Konzentrationsverhältnis HIn/In⁻ und bestimmst die Farbe des Indikators bei beliebigem pH. Die Farbskalen der wichtigsten Indikatoren geben dir einen schnellen Überblick.
Grundlagen – Kursstufe Säure-Base
Indikatoren sind Anwendungen der Henderson-Hasselbalch-Gleichung, die du auf der → Zusammenfassungsseite 4.6 hergeleitet hast. Das Prinzip des kleinsten Zwanges (Le Chatelier) wurde in der → Gleichgewichtschemie eingeführt.
5. Indikatoren
In der Regel ist ein Säure-Base-Indikator eine schwache, farbige organische Säure, deren korrespondierende Base eine andere Farbe hat:
HIn + H2O ⇌ In⁻ + H3O+Indikator-
säure
(Farbe 1)korrespond.
Indikator-
base
(Farbe 2)Farbwechsel – Prinzip des kleinsten Zwanges
Das Gleichgewicht reagiert auf pH-Änderungen nach dem Prinzip von Le Chatelier:
Saure Lösung (niedriger pH)
Hohe H3O+-Konzentration drängt das GG nach links → Farbe 1 überwiegt
Basische Lösung (hoher pH)
Niedrige H3O+-Konzentration drängt das GG nach rechts → Farbe 2 überwiegt
Hinweis: Die Farben Rot/Blau sind im Tafelbild willkürlich gewählt. Andere Indikatoren ergeben andere Farben – z. B. Phenolphthalein: sauer/neutral = farblos, alkalisch = pink/magenta.
Berechnung: Henderson-Hasselbalch-Gleichung für Indikatoren
Mit der allgemeinen Henderson-Hasselbalch-Gleichung (→ Zusammenfassung 4.6.3) kann man für jeden pH-Wert berechnen, in welchem Verhältnis die Indikatorsäure HIn zur Indikatorbase In⁻ vorliegt:
↑ Zum Vergrößern klicken
✕
Merksatz: Der Indikator schlägt um, wenn c(In⁻) = c(HIn), also wenn lg(1) = 0 → pH = pKS(HIn). Der sichtbare Umschlagbereich liegt bei pKS ± 1, weil das Auge erst ab einem 10:1-Verhältnis eine einheitliche Farbe wahrnimmt.
Beispiel: Lackmus (pKS = 7, KS = 10−7)
✕Aufgabe a) Berechne das Konzentrationsverhältnis von HIn (rot) zu In⁻ (blau) bei pH = 5!
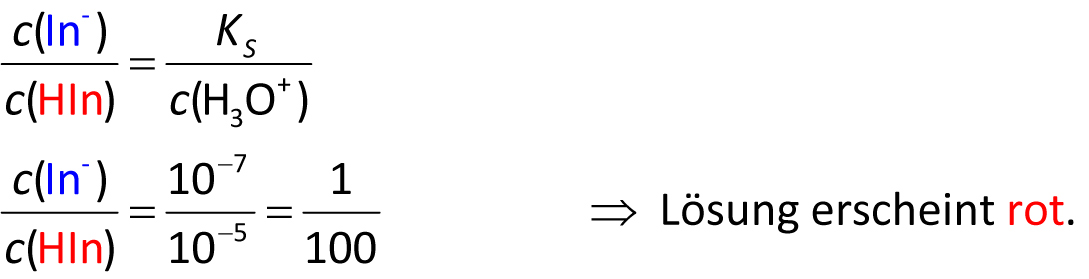 ✕
✕Aufgabe b) Welche Farbe hat der Lackmus-Indikator bei pH = 8?
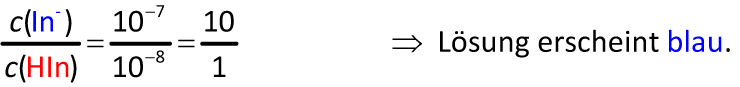
Aufgabe c) Welche Farbe liegt bei pH = 7 vor?
Bei pH = pKS = 7 gilt c(In⁻) = c(HIn) → beide Formen gleich konzentriert → Mischfarbe aus Rot und Blau = Purpur/Violett.
Das ist der Umschlagspunkt des Indikators.Der pH-Bereich, in dem die Farbe eines Indikators umschlägt, liegt demnach immer beim pKS-Wert der schwachen Säure HIn. Lackmus schlägt im Bereich pH ≈ pKS = 7 um (sichtbar zwischen pH 5 und pH 8).
Farbskalen wichtiger Indikatoren
Die Balken zeigen den Farbwechsel in Abhängigkeit vom pH-Wert (0–14). Der Umschlagbereich liegt stets bei pKS(HIn) ± 1. Das Auge nimmt eine einheitliche Farbe erst wahr, wenn ein Ion 10-fach überwiegt.
0 2 4 6 7 8 10 12 14Methylorange
Umschlag pH 3,1–4,4 · pKS ≈ 3,5● → ●Bromkresolgrün
Umschlag pH 3,8–5,4 · pKS ≈ 4,7● → ●Methylrot
Umschlag pH 4,4–6,2 · pKS ≈ 5,1● → ●Lackmus
Umschlag pH 5–8 · pKS ≈ 7● → ●Bromthymolblau (BTB)
Umschlag pH 6,0–7,6 · pKS ≈ 7,1● → ●Phenolphthalein
Umschlag pH 8,2–10 · pKS ≈ 9,4farbl. → ●sauer neutral basisch* Phenolphthalein: farblos unterhalb pH 8,2, pink/magenta im Bereich 8,2–10, ab pH 12 wieder farblos. Für die Säure-Base-Titration ist der Umschlag bei pH ≈ 9 besonders gut geeignet (Titration starker Säure mit starker Base). Mehr dazu: Säure-Base-Titration.
Auf einen Blick – die wichtigsten Aussagen
Indikator = schwache Säure
HIn und In⁻ haben verschiedene Farben. Das Gleichgewicht verschiebt sich mit dem pH.
Umschlagbereich
Umschlag bei pH = pKS(HIn). Sichtbarer Bereich: pKS ± 1.
Henderson-Hasselbalch
pH = pKS + lg(c(In⁻)/c(HIn))
→ bestimmt Farbverhältnis bei jedem pHIndikatorwahl
Indikator für Titration wählen, dessen pKS(HIn) nahe dem Äquivalenzpunkt liegt.
Häufige Fragen – Indikatoren
Warum zeigt ein Indikator verschiedene Farben bei verschiedenem pH?
Ein Indikator ist eine schwache organische Säure HIn, deren Säureform und Baseform unterschiedlich gefärbt sind. Ändert sich der pH, verschiebt sich nach Le Chatelier das Gleichgewicht HIn + H2O ⇌ In⁻ + H3O+: Bei niedrigem pH (viel H3O+) überwiegt HIn (Farbe 1), bei hohem pH überwiegt In⁻ (Farbe 2). Am Umschlagspunkt (pH = pKS) sind beide gleich konzentriert → Mischfarbe.
Welchen Indikator verwendet man für eine Titration?
Der pKS-Wert des Indikators sollte möglichst nahe am Äquivalenzpunkt der Titration liegen. Für die Titration einer starken Säure mit einer starken Base liegt der Äquivalenzpunkt bei pH = 7 → Lackmus oder Bromthymolblau (pKS ≈ 7) sind geeignet. Für schwache Säuren liegt der Äquivalenzpunkt im Basischen → Phenolphthalein (pKS ≈ 9,4) ist besser. Mehr dazu: Säure-Base-Titration.
Warum ist der Umschlagbereich immer pKS ± 1?
Das menschliche Auge nimmt eine Mischfarbe erst dann als eindeutige Farbe war, wenn eine Komponente 10-fach überwiegt (c(In⁻)/c(HIn) ≥ 10 oder ≤ 1/10). Nach der Henderson-Hasselbalch-Gleichung: pH = pKS + lg(10) = pKS + 1 bzw. pH = pKS − 1. Daraus folgt der sichtbare Umschlagbereich von pKS ± 1.
Warum ist Phenolphthalein im stark Basischen wieder farblos?
Phenolphthalein liegt in drei Formen vor: Bei pH < 8,2 als farblose Säureform, bei pH 8,2–10 als farbige chinoide Form (pink/magenta), und bei pH > 12 wird die chinoide Form durch weiteren OH⁻-Angriff in eine ebenfalls farblose Tri-Anion-Form umgewandelt. Dieses „Ausbleichen" im stark basischen Milieu ist für Titrationen zu beachten.
Wie berechnet man c(In⁻)/c(HIn) bei bekanntem pH?
Aus der Henderson-Hasselbalch-Gleichung umstellen: lg(c(In⁻)/c(HIn)) = pH − pKS, also c(In⁻)/c(HIn) = 10(pH − pKS). Beispiel Lackmus (pKS = 7) bei pH = 5: c(In⁻)/c(HIn) = 10(5−7) = 10−2 = 1/100 → 100-facher Überschuss HIn → Lösung erscheint rot. Mehr Formeln: Zusammenfassung 4.6.
Lernkarten – Indikatoren
Klicke auf eine Karte, um die Antwort zu sehen.
1Bei welchem pH-Wert schlägt ein Indikator um?
Am Umschlagspunkt gilt c(In⁻) = c(HIn).
→ pH = pKS(HIn)
Sichtbarer Bereich: pKS ± 12Was versteht man unter dem Umschlagbereich eines Indikators?
Der pH-Bereich, in dem das Auge den Farbwechsel wahrnimmt.
Liegt bei pKS ± 1, da das Auge erst bei 10:1-Verhältnis eine Reinfarbe sieht.3Wie lautet die Henderson-Hasselbalch-Gleichung für Indikatoren?
pH = pKS + lg(c(In⁻) / c(HIn))
Herleitung aus KS = c(H3O+)·c(In⁻)/c(HIn)4Warum ist Bromthymolblau für Neutraltitration gut geeignet?
pKS(BTB) ≈ 7,1 → Umschlagbereich pH 6–8.
Der Äquivalenzpunkt einer Stärkesäure-/Stärkebase-Titration liegt nahe pH 7 → BTB schlägt dort sicher um.5Rechenaufgabe: Welche Farbe hat Methylorange (pKS = 3,5) bei pH = 5?
c(In⁻)/c(HIn) = 10(5 − 3,5) = 101,5 ≈ 32
→ In⁻ überwiegt 32-fach → gelb (Baseform von Methylorange).Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← Zusammenfassung pH/pOH → Säure-Base-Titration
🔁 Grundlagen: Prinzip von Le Chatelier · Henderson-Hasselbalch-Gleichung (4.6.3)
📌 Weiterführend: Säure-Base-Titration · Pufferlösungen