Elektronen
-
1. Elementarteilchen – Proton, Neutron, Elektron
Was du auf dieser Seite lernst
Atome bestehen aus nur drei verschiedenen Bausteinen: Proton, Neutron und Elektron. Du lernst ihre Eigenschaften (Ladung, Masse, Ort im Atom) kennen, verstehst den Unterschied zwischen Ordnungszahl und Massenzahl und kannst die Gesamtladung eines Teilchens berechnen.
Grundlagen aus der 8. Klasse
Das Dalton-Modell (Atom als unteilbare Kugel) hast du bereits in der 8. Klasse kennengelernt: → Atommodell nach Dalton (Kl. 8)
Die drei Elementarteilchen – Bausteine der Atome
Atome bestehen aus genau drei verschiedenen Bausteinen. Fahre mit der Maus über die Kugeln (oder tippe sie an), um mehr zu erfahren:
ProtonDas Proton (p⁺):
Befindet sich im Atomkern
Ladung: +1
Relative Masse: 1 u (genau: 1,0073 u)NeutronDas Neutron (n⁰):
Befindet sich im Atomkern
Ladung: 0 (neutral)
Relative Masse: 1 u (genau: 1,0087 u)ElektronDas Elektron (e⁻):
Befindet sich in der Atomhülle
Ladung: −1
Relative Masse: ≈ 0 u (genau: 0,0005 u)↑ Mit der Maus über die Kugeln fahren (oder antippen)
Übersichtstabelle der Elementarteilchen
Teilchen Symbol Rel. Masse Ladung Ort im Atom Proton p⁺ 1 u +1 Atomkern Neutron n⁰ 1 u 0 Atomkern Elektron e⁻ ≈ 0 u −1 Atomhülle Ordnungszahl und Massenzahl
Die Ordnungszahl (auch: Kernladungszahl) gibt die Anzahl der Protonen im Atomkern an. Sie bestimmt die Stellung des Elements im Periodensystem. Im neutralen Atom gilt immer: Protonenzahl = Elektronenzahl.
Die Massenzahl ist die Summe aus Protonen und Neutronen:
Massenzahl = Anzahl der Protonen + Anzahl der Neutronen
Gesamtladung eines Teilchens berechnen
Die Gesamtladung ergibt sich durch einfaches Addieren aller Einzelladungen. Protonen (+1) und Elektronen (−1) werden gezählt, Neutronen (0) fallen dabei heraus.
Beispiel
Ein Teilchen besteht aus 3 Protonen, 3 Neutronen und 2 Elektronen. Wie groß ist die Ladung?
3 × (+1) = +3 (Protonen)
3 × ( 0) = 0 (Neutronen)
2 × (−1) = −2 (Elektronen)
+3 + 0 + (−2) = +1
→ Die Ladung ist 1+Teilchen-Modell
● Proton ● Neutron ● Elektron
Auf einen Blick – die wichtigsten Aussagen
PROTON
Im Atomkern, Ladung +1, Masse 1 u. Die Protonenzahl = Ordnungszahl = Stellung im PSE.
NEUTRON
Im Atomkern, Ladung 0, Masse 1 u. Beeinflusst die Masse, nicht die Ladung.
ELEKTRON
In der Atomhülle, Ladung −1, Masse ≈ 0 u. Bestimmt das chemische Verhalten.
NEUTRALES ATOM
Im neutralen Atom gilt immer: Protonen = Elektronen. Massenzahl = Protonen + Neutronen.
Häufige Fragen – Elementarteilchen
Aus welchen Teilchen besteht ein Atom?
Jedes Atom besteht aus drei Typen von Elementarteilchen: Protonen und Neutronen im Atomkern, Elektronen in der Atomhülle. Protonen sind positiv (+1), Neutronen neutral (0), Elektronen negativ (−1).
Was ist der Unterschied zwischen Ordnungszahl und Massenzahl?
Die Ordnungszahl gibt die Protonenzahl an und bestimmt die Position im Periodensystem. Die Massenzahl = Protonen + Neutronen und entspricht der ungefähren Atommasse in u. Beispiel Kohlenstoff (C): Ordnungszahl 6, Massenzahl 12 → 6 Protonen + 6 Neutronen.
Warum hat das Elektron eine vernachlässigbare Masse?
Die Elektronenmasse beträgt nur ca. 0,0005 u – etwa 1/1836 der Protonenmasse. In der Schulchemie wird sie als ≈ 0 u vereinfacht. Die Atommasse wird praktisch vollständig durch Protonen und Neutronen bestimmt.
Wie berechnet man die Ladung eines Ions?
Man addiert die Ladungen aller Elementarteilchen: Proton = +1, Elektron = −1, Neutron = 0. Ein Kation (positiv) entsteht durch Elektronenabgabe, ein Anion (negativ) durch Elektronenaufnahme. Beispiel: Na⁺ hat 11 Protonen und 10 Elektronen → Ladung = +1.
Was sind Isotope?
Isotope sind Atome desselben Elements mit gleicher Protonenzahl, aber unterschiedlicher Neutronenzahl (→ verschiedene Massenzahlen). Beispiel: ¹²C und ¹⁴C haben beide 6 Protonen, aber 6 bzw. 8 Neutronen. Chemisch verhalten sie sich identisch.
Lernkarten – Elementarteilchen
Klicke auf eine Karte, um die Antwort zu sehen.
1Nenne Symbol, Ladung, relative Masse und Aufenthaltsort des Protons.
Symbol: p⁺
Ladung: +1
Rel. Masse: 1 u
Ort: Atomkern2Nenne Symbol, Ladung, relative Masse und Aufenthaltsort des Neutrons.
Symbol: n⁰
Ladung: 0 (neutral)
Rel. Masse: 1 u
Ort: Atomkern3Nenne Symbol, Ladung, relative Masse und Aufenthaltsort des Elektrons.
Symbol: e⁻
Ladung: −1
Rel. Masse: ≈ 0 u
Ort: Atomhülle4Was ist die Ordnungszahl? Was sagt die Massenzahl aus?
Ordnungszahl = Protonenzahl (= Elektronenzahl im neutralen Atom); Stellung im PSE.
Massenzahl = Protonen + Neutronen5Schwefel (S, OZ = 16, MZ = 32): Wie viele Protonen, Neutronen und Elektronen? Welche relative Atommasse?
Protonen: 16
Neutronen: 32 − 16 = 16
Elektronen (neutral): 16
Rel. Atommasse: 16 + 16 = 32 u
Weiter im Kapitel – Vom Atombau bis ZMK
← Kapitelübersicht → Atommodelle: Demokrit und Dalton
🔁 Grundlagen: Atommodell nach Dalton (Kl. 8)
-
2.3 Rutherford: Kern-Hülle-Modell
Was du auf dieser Seite lernst
Atome bestehen aus einem winzigen, positiv geladenen Atomkern und einer negativ geladenen Elektronenhülle. Du lernst die drei Elementarteilchen (Proton, Neutron, Elektron) kennen, verstehst elektrische Anziehungs- und Abstoßungskräfte im Atom und lernst die chemische Schreibweise mit Nukleonenzahl, Kernladungszahl und Massenzahl.
Grundlagen aus der 8. Klasse
Das erste Atommodell hast du bereits in der 8. Klasse kennengelernt: → Atommodell nach Dalton – Kugelteilchenmodell
Elektrische Anziehungskräfte im Atom
Sehr vereinfacht können wir sagen, dass jede Anziehungskraft der Chemie auf der Anziehung zwischen positiver und negativer Ladung beruht.
Kurz: Plus + Minus ziehen sich an; gleiche Ladungen stoßen sich ab.
⚡ Anziehung und Abstoßung – ausprobieren!
Plus + Minus ziehen sich an. Gleiche Ladungen stoßen sich ab.+↔−+↔+−↔−Aufbau des Atoms: Atomkern und Elektronenhülle
Atome bestehen aus:
- einem sehr kleinen, positiv geladenen Kern
- einer negativen, kugelförmigen Elektronenhülle
- Elektronen, die sich mit hoher Geschwindigkeit um den Kern bewegen
Ein Atommodell, das zwischen Atomkern und Elektronenhülle unterscheidet, wird als Kern-Hülle-Modell bezeichnet.
Vereinfachtes Kern-Hülle-Modell eines Atoms (nicht maßstabsgerecht)
Größenverhältnis: Atomkern und Atomhülle
⚠️ Wichtig: Der Durchmesser der Atomhülle ist etwa 10 000-mal größer als der Durchmesser des Atomkerns. Die Hülle ist kein fester Bereich – es ist nur der Bereich, in dem sich die Elektronen aufhalten.
Wenn der Atomkern so groß wie eine Kirsche wäre, hätte das gesamte Atom einen Durchmesser von etwa einem Fußballfeld.
🔬 Wasserstoffatom – Maßstabsgetreues Modell1×Atom 10× 100× 1.000× 6.000× ProtonVollständiges Atom sichtbar. Das Proton ist maßstabsgerecht viel zu klein zum Sehen.2.3.1 Der Atomkern – Elementarteilchen und Schreibweise
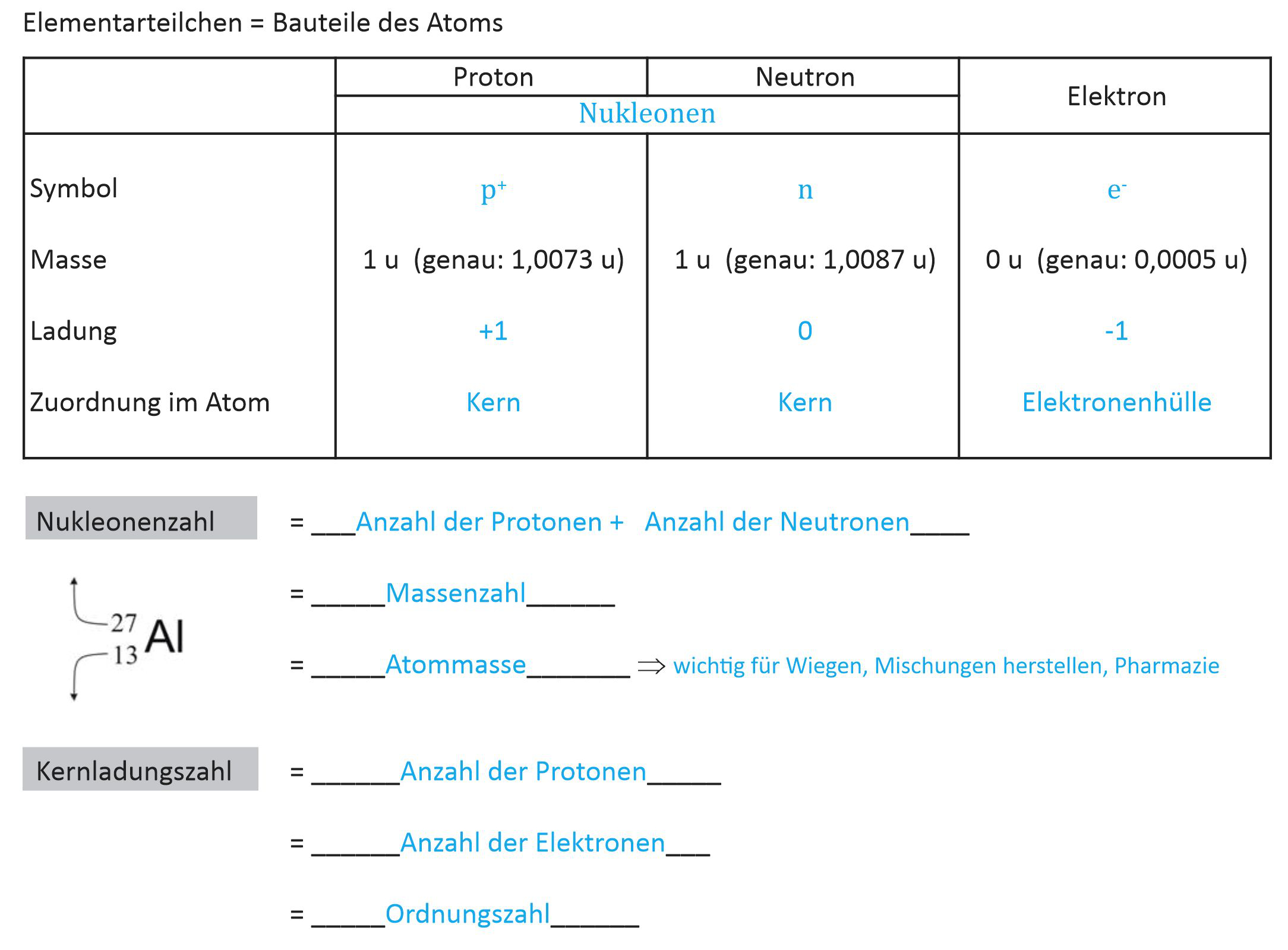
Die Teilchen, aus denen ein Atom besteht, bezeichnet man als Elementarteilchen: Protonen, Neutronen und Elektronen.
↑ Zum Vergrößern klicken
✕
Aus dem Tafelbild ergeben sich folgende Definitionen:
- Der Atomkern ist aus Protonen und Neutronen aufgebaut.
- Die Protonenzahl stimmt mit der Ordnungszahl eines Elements und der
Kernladungszahl überein.
Beispiel: Fluor = ₉F: 9 Protonen → Ordnungszahl = Kernladungszahl = 9, Elektronenanzahl = 9. - Nukleonenzahl = Anzahl der Protonen + Anzahl der Neutronen im Atomkern.
Beispiel: ¹⁹F: Nukleonenzahl = 19 → 9 Protonen und 10 Neutronen. - Massenzahl: Die Atommasse ist angenähert die Summe der Protonen- und Neutronenmasse. Die Masse der Elektronen ist außerordentlich klein.
Übungsaufgabe: Elementarteilchen
Kannst du die Tabelle selbst ausfüllen? Klicke dann auf „Lösung anzeigen".
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
Kern-Hülle-Modell
Atome bestehen aus einem winzigen, positiv geladenen Atomkern und einer negativ geladenen Elektronenhülle.
Elementarteilchen
Im Kern: Protonen (1 u, +1) und Neutronen (1 u, 0). In der Hülle: Elektronen (≈0 u, −1).
Nukleonenzahl
Nukleonenzahl = Anzahl Protonen + Anzahl Neutronen = Massenzahl. Die Kernladungszahl = Protonenzahl = Ordnungszahl.
Elektrische Kräfte
Ungleiche Ladungen ziehen sich an, gleiche stoßen sich ab. Protonen (+) und Elektronen (−) halten das Atom zusammen.
Häufige Fragen – Kern-Hülle-Modell und Elementarteilchen
Was sind Elementarteilchen und welche gibt es?
Elementarteilchen sind die Bausteine eines Atoms. Es gibt drei: Protonen (Masse 1 u, Ladung +1, im Kern), Neutronen (Masse 1 u, Ladung 0, im Kern) und Elektronen (Masse ≈ 0 u, Ladung −1, in der Elektronenhülle). Protonen und Neutronen heißen zusammen auch Nukleonen.
Was ist der Unterschied zwischen Kernladungszahl, Ordnungszahl und Massenzahl?
Die Kernladungszahl = Anzahl der Protonen im Kern = Ordnungszahl des Elements im Periodensystem. Die Massenzahl (= Nukleonenzahl) = Anzahl Protonen + Anzahl Neutronen. Beim Aluminium ²⁷₁₃Al: Kernladungszahl = Ordnungszahl = 13 (Protonen), Massenzahl = 27 (13 Protonen + 14 Neutronen).
Warum ist der Atomkern so viel kleiner als das Atom?
Der Durchmesser der Atomhülle beträgt etwa 10 000-mal den Durchmesser des Atomkerns. Der Kern enthält fast die gesamte Masse des Atoms, aber fast kein Volumen. Die Hülle ist kein festes Objekt – sie ist lediglich der Bereich, in dem sich die Elektronen aufhalten. Der übrige Teil des Atoms ist „leer".
Warum brechen nicht alle Protonen im Kern auseinander?
Auf sehr kurze Abstände wirkt die sogenannte starke Kernkraft (Kernbindungskraft), die stärker ist als die elektrische Abstoßung zwischen den positiv geladenen Protonen. Neutronen helfen dabei, diese Kraft zu vermitteln und den Kern zusammenzuhalten. Die starke Kernkraft ist Thema der Physik – in der Chemie arbeiten wir vereinfachend mit dem Kern-Hülle-Modell.
Welche Weiterentwicklung des Kern-Hülle-Modells gibt es?
Rutherford beschrieb erstmals den Aufbau aus Kern und Hülle. Niels Bohr erweiterte dieses Modell: Elektronen bewegen sich auf bestimmten Bahnen (Energiestufen, Schalen) um den Kern – man spricht vom Bohrschen Schalenmodell. Das modernste Modell für die Schule ist das Kugelwolkenmodell (KWM), das die Aufenthaltswahrscheinlichkeit der Elektronen beschreibt.
Lernkarten – Kern-Hülle-Modell und Elementarteilchen
Klicke auf eine Karte, um die Antwort zu sehen.
1Aus welchen drei Elementarteilchen besteht ein Atom? Nenne Symbol, Masse und Ladung.
Proton (p⁺, 1 u, +1) – im Kern
Neutron (n, 1 u, 0) – im Kern
Elektron (e⁻, ≈0 u, −1) – Elektronenhülle2Was ist die Kernladungszahl und womit stimmt sie überein?
Die Kernladungszahl = Anzahl der Protonen im Kern. Sie stimmt mit der Ordnungszahl im PSE und der Elektronenanzahl im neutralen Atom überein.
3Was passiert bei: +/−, +/+, −/−?
+ und − → Anziehung (ungleiche Ladungen)
+ und + → Abstoßung (gleiche Ladungen)
− und − → Abstoßung (gleiche Ladungen)4Was bedeuten die Zahlen in der Schreibweise ²⁷₁₃Al?
27 = Massenzahl (Nukleonenzahl) = Protonen + Neutronen
13 = Kernladungszahl = Ordnungszahl = Protonenzahl
Neutronen = 27 − 13 = 145Rechenaufgabe: ¹⁹₉F – wie viele Protonen, Neutronen und Elektronen?
Protonen = Kernladungszahl = 9
Neutronen = 19 − 9 = 10
Elektronen (neutral) = Protonenzahl = 9Weiter im Kapitel – Atombau bis ZMKs
← 2.2 Atommodelle: Demokrit und Dalton 2.4 Bohrsches Schalenmodell →
🔁 Grundlagen (Kl. 8): Atommodell nach Dalton – Kugelteilchenmodell
⏩ Weiterführend: 2.5 Das Kugelwolkenmodell (KWM) · PSE Teil I
-
2.4 Bohr – Schalenmodell der Elektronenhülle
Was du auf dieser Seite lernst
Niels Bohr erweiterte das Rutherford-Modell: Elektronen bewegen sich nicht beliebig, sondern nur auf bestimmten Bahnen (Energiestufen, Schalen) um den Kern. Du lernst Bohrs zwei Postulate kennen, verstehst die 2n²-Formel für die maximale Elektronenzahl pro Schale und erfährst, wie das Modell Lichtabsorption und -emission erklärt.
Grundlagen aus der 9. Klasse
Voraussetzung ist das Kern-Hülle-Modell von Rutherford: → 2.3 Rutherford: Kern-Hülle-Modell und Elementarteilchen
Niels Bohrs Schalenmodell
Niels Bohrs Modell beschreibt das Atom aus einem positiv geladenen Kern und negativ geladenen Elektronen, die auf ganz bestimmten konzentrischen Bahnen den Kern umkreisen (ähnlich wie die Planeten die Sonne umkreisen).
↑ Zum Vergrößern klicken – Zoom-Overlay aktiv
▶ 1. Postulat – Niels Bohr, 1913
Die Elektronen bewegen sich nur auf ganz bestimmten, genau definierten Bahnen (= Energiestufen, Energieschalen, Schalen) um den Atomkern.
Diese Bahnen heißen Schalen und werden von innen nach außen mit K, L, M, N, … bezeichnet. Je weiter die Schale vom Kern entfernt ist, desto höher ist die Energie der Elektronen auf ihr.
Energieniveaus und Elektronenschalen
Die Begriffe Schale und Energiestufe beschreiben dasselbe: den Bereich, in dem sich Elektronen mit einer bestimmten Energie bewegen. Elektronen auf der M-Schale besitzen eine höhere Energie als solche auf der L-Schale, da sie weiter vom Kern entfernt sind.
👆 Tipp: Die interaktive Übersicht direkt darunter zeigt die Schalenbesetzung für alle Elemente der 1.–3. Periode – hover einfach über ein Element im PSE!
2. Postulat – Maximale Elektronenzahl pro Schale
▶ 2. Postulat – Niels Bohr, 1913
Jede Schale kann maximal 2 · n² Elektronen aufnehmen.
n = Schalennummer (n = 1, 2, 3, 4, …)
Schale n 2 · n² Max. Elektronen K 1 2 · 1² = 2 2 L 2 2 · 2² = 8 8 M 3 2 · 3² = 18 18 N 4 2 · 4² = 32 32 Beispiel 1
Wie viele Elektronen kann die 1. Schale maximal aufnehmen?
Lösung 1
1. Schale → n = 1 | 2·n² = 2·1·1 = 2
Beispiel 2
Wie viele Elektronen kann die N-Schale maximal aufnehmen?
Lösung 2
N-Schale ist die 4. Schale → n = 4 | 2·n² = 2·4² = 32
⚠️ Wichtig: Das bedeutet nur, dass so viele Elektronen maximal in diese Schale passen. Natürlich können jederzeit weniger Elektronen vorhanden sein!
🧠 Verständnisüberprüfung
Elektronen welcher Schale besitzen eine höhere Energie – die der L-Schale oder die der M-Schale?
▶ Lösung anzeigen
Die Elektronen der M-Schale, da diese weiter vom Kern entfernt sind und damit eine höhere potenzielle Energie besitzen.
⚡ Energieniveaus vs. ElektronenschalenFahre mit der Maus über ein Element des Periodensystems!Wähle ein Element, um die Elektronenverteilung zu sehen.Quantentheorie: Absorption und Emission von Licht
Quantentheorie (Planck, Einstein):
Die kleinsten nicht mehr teilbaren Energiebeträge heißen Quanten.
Durch Energiezufuhr kann ein Elektron vom Grundzustand (= energieärmster Zustand) in einen angeregten Zustand gebracht werden.
Da das Elektron zwischen den Schalen nicht existieren kann, nimmt es nur solche Energiequanten auf, die der Energiedifferenz zwischen zwei Schalen entsprechen – zum Beispiel durch Absorption von Licht.
Der angeregte Zustand ist sehr instabil: Das Elektron springt nach ca. 10⁻⁸ s wieder in den Grundzustand zurück und gibt dabei die Anregungsenergie als Licht (Emission) wieder ab.
Absorption: Elektron springt in höhere Schale · Emission: Rücksprung mit Lichtabgabe (≈ 10⁻⁸ s)
Übungsaufgaben
Aufgabe 1: Aus welchen Elementarteilchen besteht der Atomkern und wie ist er geladen?
Der Atomkern besteht aus Protonen und Neutronen. Er ist positiv geladen, da Protonen die Ladung +1 tragen und Neutronen neutral sind. → Wiederholung: Elementarteilchen
Aufgabe 2: Wie verteilen sich die Elektronen laut Niels Bohr?
Die Elektronen bewegen sich auf ganz bestimmten Bahnen (Schalen / Energiestufen) um den Kern. Die innerste Schale (K) wird zuerst besetzt. Erst wenn sie voll ist, werden äußere Schalen gefüllt.
Aufgabe 3: Wie lautet die Formel für die maximale Elektronenzahl pro Schale?
Maximale Elektronenzahl pro Schale = 2 · n², wobei n die Schalennummer ist. Beispiele: K (n=1) → 2, L (n=2) → 8, M (n=3) → 18.
Aufgabe 4: Auf welche Schale verteilt sich ein Elektron als erstes?
Auf die K-Schale (innerste, energieärmste Schale). Elektronen besetzen immer zuerst die energieärmste verfügbare Schale.
Aufgabe 5: Wie viele Elektronen kann die L-Schale maximal besitzen?
L-Schale → n = 2 → 2 · n² = 2 · 4 = 8 Elektronen.
Aufgabe 6: Woraus besteht der Hauptteil (fast der ganze Raum) eines Atoms?
Fast der gesamte Raum eines Atoms besteht aus leerem Raum. Der winzige Kern enthält fast die gesamte Masse, nimmt aber nur einen verschwindend kleinen Teil des Atomvolumens ein. → Größenverhältnis Kern/Hülle
Auf einen Blick – die wichtigsten Aussagen
1. Postulat
Elektronen bewegen sich nur auf genau definierten Bahnen (Energiestufen / Schalen: K, L, M, N …) um den Kern.
2. Postulat
Maximale Elektronenzahl pro Schale: 2 · n² (K = 2, L = 8, M = 18, N = 32).
Energiestufen
Je weiter die Schale vom Kern, desto höher die Energie der Elektronen. M-Elektronen haben mehr Energie als L-Elektronen.
Absorption / Emission
Absorption: Elektron springt in höhere Schale. Emission: Rücksprung → Licht wird abgegeben (≈ 10⁻⁸ s).
Häufige Fragen – Bohrsches Schalenmodell
Was sind die Postulate von Niels Bohr?
1. Postulat: Elektronen bewegen sich nur auf bestimmten Bahnen (Schalen/Energiestufen) um den Kern – keine anderen Positionen möglich. 2. Postulat: Jede Schale fasst maximal 2·n² Elektronen (n = Schalennummer). Innerste Schale wird zuerst besetzt.
Was ist der Unterschied zwischen Schale und Energiestufe?
Beides bezeichnet dasselbe: den Bereich, in dem sich Elektronen mit einer bestimmten Energie aufhalten. „Schale" betont den räumlichen Aspekt (kreisförmige Bahn), „Energiestufe" betont den energetischen Aspekt. In der Chemie werden beide Begriffe synonym verwendet. Die Schalen sind von innen nach außen K, L, M, N … benannt.
Wie viele Elektronen passen maximal in die K-, L- und M-Schale?
K-Schale (n=1): 2·1² = 2 Elektronen. L-Schale (n=2): 2·2² = 8 Elektronen. M-Schale (n=3): 2·3² = 18 Elektronen. Wichtig: Das sind Maximalwerte – es können immer weniger Elektronen vorhanden sein.
Wie erklärt das Bohr-Modell die Entstehung von Licht?
Elektronen können Lichtenergie (Photonen) absorbieren und dadurch in eine höhere Schale springen (angeregter Zustand). Da dieser Zustand instabil ist, springen sie nach ca. 10⁻⁸ s zurück in den Grundzustand und geben dabei ein Lichtquant (Photon) ab – das ist die Emission von Licht. Die Farbe des emittierten Lichts hängt von der Energiedifferenz zwischen den Schalen ab.
Wo liegen die Grenzen des Bohrschen Schalenmodells?
Das Bohr-Modell funktioniert nur exakt für Wasserstoff (1 Elektron). Bei mehreren Elektronen liefert es nur Näherungen. Außerdem widerspricht die Vorstellung einer genau definierten Kreisbahn der Quantenmechanik (Heisenbergsche Unschärferelation). Das modernere Kugelwolkenmodell (KWM) löst diese Probleme durch Aufenthaltswahrscheinlichkeiten statt fester Bahnen.
Lernkarten – Bohrsches Schalenmodell
Klicke auf eine Karte, um die Antwort zu sehen.
1Nenne Bohrs 1. Postulat in einem Satz.
Elektronen bewegen sich nur auf ganz bestimmten, genau definierten Bahnen (= Energiestufen / Schalen) um den Atomkern.
2Wie lautet die Formel für die max. Elektronen pro Schale? Was bedeutet n?
Max. Elektronen = 2 · n²
n = Schalennummer (K=1, L=2, M=3, N=4)3Was passiert bei der Absorption von Licht?
Das Elektron nimmt ein Lichtquant (Photon) auf und springt von einer niedrigeren in eine höhere Schale (Grundzustand → angeregter Zustand).
4Warum senden Atome Licht aus? Was ist Emission?
Der angeregte Zustand ist instabil: Das Elektron springt zurück in den Grundzustand und gibt die Energiedifferenz als Licht (Photon) ab – das ist Emission.
5Rechenaufgabe: Wie viele Elektronen passen maximal in die M-Schale?
M-Schale → n = 3
2 · n² = 2 · 3² = 2 · 9 = 18 ElektronenWeiter im Kapitel – Atombau bis ZMKs
← 2.3 Rutherford: Kern-Hülle-Modell 2.5 Kugelwolkenmodell →
⏩ Weiterführend: 2.6 PSE und die Atommodelle · 2.5 Kugelwolkenmodell (KWM)
-
2.5 Das Kugelwolkenmodell, KWM
Was du auf dieser Seite lernst
Das Kugelwolkenmodell (KWM) ist eine Weiterentwicklung des Bohr-Modells: Statt fester Elektronenbahnen gibt es nur noch Wahrscheinlichkeitsbereiche – sogenannte Kugelwolken. Du lernst, wie diese dargestellt werden, was das Pauli-Prinzip und die Regel von Hund besagen, und wie das KWM für die ersten 10 Elemente aussieht.
Grundlagen aus der 9. Klasse
Das KWM baut direkt auf dem Bohr-Schalenmodell auf: → 2.4 Bohr-Schalenmodell · → 2.3 Rutherford-Kern-Hülle-Modell
Das Kugelwolkenmodell – eine Weiterentwicklung des Bohr-Modells
Das Bohrsche Atommodell kann schon viel erklären; allerdings gibt es ein weiteres Atommodell, in dem die Elektronen in bestimmten gedachten Aufenthaltswahrscheinlichkeitsräumen betrachtet werden. Das sind keine echten Räume, sondern Bereiche, in denen sich mit hoher Wahrscheinlichkeit gerade ein Elektron – maximal zwei – aufhält. Es könnte sich auch gerade außerhalb dieses Bereichs bewegen, allerdings mit geringerer Wahrscheinlichkeit.
So einfach, wie Niels Bohr sich das vorgestellt hatte, war es allerdings nicht mit der Verteilung der Elektronen innerhalb einer Schale. Es gibt bestimmte Bereiche, in denen sich die Elektronen mit größerer Wahrscheinlichkeit aufhalten – sogenannte Kugelwolken.
🖱️ Interaktives Diagramm → Klicke auf einen Bereich für eine Erläuterung · Mobilgerät: TippenVergleich: Schalenmodell vs. Kugelwolkenmodell am Beispiel Sauerstoff (Z = 8)
Kugelwolke einfach besetzt (1 Elektron) Kugelwolke doppelt besetzt (2 Elektronen) Elektron🔴 Atomkern (Schalenmodell) Der Kern des Sauerstoffs trägt die Ladung 8+ (8 Protonen). Im Schalenmodell nach Bohr umkreisen die Elektronen den Kern auf festen Bahnen – wie Planeten die Sonne. Im Kugelwolkenmodell bleibt der Kern unverändert, aber die Elektronen befinden sich nicht mehr auf Bahnen, sondern in Wahrscheinlichkeitsbereichen.⚪ K-Schale (Schalenmodell) Die K-Schale ist die innerste Elektronenschale. Beim Sauerstoff enthält sie 2 Elektronen. Im Kugelwolkenmodell entspricht ihr eine einzige rote Kugelwolke direkt am Kern (doppelt besetzt). Die K-Schale fasst maximal 2 Elektronen (→ Pauli-Prinzip).⚪ L-Schale (Schalenmodell) Die L-Schale ist die zweite Elektronenschale. Beim Sauerstoff enthält sie 6 Elektronen, gleichmäßig auf der Kreisbahn verteilt. Im Kugelwolkenmodell werden diese 6 Elektronen auf 4 Kugelwolken verteilt: 2 doppelt besetzte (rot) und 2 einfach besetzte (grün).🔴 Atomkern (Kugelwolkenmodell) Auch im Kugelwolkenmodell bleibt der Atomkern mit der Ladung 8+ unveränderter Mittelpunkt. Die Kugelwolken sind um ihn herum angeordnet. Je näher eine Kugelwolke am Kern liegt, desto energieärmer ist sie (K-Schale < L-Schale).● Kugelwolke der K-Schale (doppelt besetzt) Die Kugelwolke der K-Schale liegt direkt am Kern und ist rot = doppelt besetzt – sie enthält beide K-Elektronen (2e). In der K-Schale gibt es nur eine einzige Kugelwolke. Maximal 2 Elektronen passen hinein (→ Pauli-Prinzip).● Kugelwolke der L-Schale – einfach besetzt Grüne Kugelwolken sind einfach besetzt – sie enthalten genau 1 Elektron. Beim Sauerstoff gibt es in der L-Schale 2 einfach besetzte Kugelwolken. Dies folgt aus der Regel von Hund: Energiegleiche Kugelwolken werden zuerst einzeln besetzt.● Kugelwolke der L-Schale – doppelt besetzt Rote Kugelwolken sind doppelt besetzt – sie enthalten 2 Elektronen. Beim Sauerstoff gibt es in der L-Schale 2 doppelt besetzte Kugelwolken. Die Doppelbesetzung tritt erst auf, wenn alle energiegleichen Kugelwolken mindestens 1 Elektron haben (→ Regel von Hund).💡 Nochmals klicken schließt die Erläuterung.
Das Kugelwolkenmodell ähnelt einem Tetraeder
Das Kugelwolkenmodell ist ein stark vereinfachtes Orbitalmodell. Da die Elektronen sich in bestimmten Bereichen aufhalten, den sogenannten Orbitalen, sind diese negativ geladen und stoßen sich somit ab. Um den größtmöglichen Abstand zu erhalten, ergeben diese vier Kugelwolken eine Art Tetraeder. Das soll die folgende Animation eines Sauerstoffmodells zeigen.
Vereinfachte Darstellung der Kugelwolken
Da die räumliche Anordnung der Kugelwolken (Tetraeder-Struktur, 109,47°-Winkel) schwer darstellbar ist, wird im Unterricht eine vereinfachte, ebene Darstellung verwendet. Die Abbildung unten zeigt links die räumliche Ansicht und rechts die vereinfachte Darstellung. Beachte: Die räumliche Anordnung der Orbitale sieht in Wirklichkeit anders aus als die ebene Vereinfachung.
🖱️ Interaktives Diagramm – Vereinfachte Darstellung → Klicke auf eine Kugelwolke für eine ErläuterungSauerstoff (Z = 8): räumliche Darstellung (links) und vereinfachte Darstellung (rechts)
einfach besetztes Orbital (1 Elektron) doppelt besetztes Orbital (2 Elektronen) Elektron🔴 Atomkern (räumliche Darstellung) Der Kern des Sauerstoffs trägt die Ladung 8+. In der räumlichen Darstellung ist gut zu sehen, wie die vier L-Kugelwolken den Kern tetraedrisch umgeben – der Winkel zwischen je zwei Kugelwolken beträgt 109,47° (Tetraeder-Winkel). Dieser maximale Abstand entsteht, weil sich die negativ geladenen Kugelwolken gegenseitig abstoßen.● K-Schalen-Kugelwolke (räumlich, doppelt besetzt) Die kleine rote Kugelwolke direkt am Kern gehört zur K-Schale (1s²). Sie ist doppelt besetzt (2 Elektronen) und liegt energetisch am tiefsten. In der räumlichen Darstellung ist gut zu sehen, wie sie sich vom Kern kaum abhebt – sie ist sehr klein im Vergleich zu den L-Kugelwolken.● Einfach besetztes Orbital (räumlich, 1 Elektron) Grüne Kugelwolken enthalten jeweils 1 Elektron. Beim Sauerstoff gibt es zwei einfach besetzte Kugelwolken in der L-Schale. In der räumlichen Darstellung sieht man ihre tetraedrische Anordnung: Sie stehen im größtmöglichen Winkelabstand zu allen anderen Kugelwolken.● Doppelt besetztes Orbital (räumlich, 2 Elektronen) Rote Kugelwolken enthalten jeweils 2 Elektronen. Beim Sauerstoff gibt es zwei doppelt besetzte Kugelwolken in der L-Schale (2s² und 2px²). In der räumlichen Ansicht sind sie gut von den grünen einfach besetzten Kugelwolken zu unterscheiden.🔴 Atomkern (vereinfachte Darstellung) In der vereinfachten Darstellung liegt der Kern 8+ in der Mitte. Die vier L-Kugelwolken sind hier in einer ebenen Anordnung (oben, unten, links, rechts) dargestellt – in Wirklichkeit sind sie tetraedrisch (räumlich) angeordnet. Die vereinfachte Darstellung erleichtert das Zeichnen im Unterricht.● K-Schalen-Kugelwolke (vereinfacht, doppelt besetzt) Die kleine rote Kugelwolke um den Kern gehört zur K-Schale. Sie ist doppelt besetzt (2 Elektronen, 1s²). In der vereinfachten Darstellung wird sie als kleiner Kreis direkt am Kern gezeigt – wie in der räumlichen Darstellung auch.● Einfach besetztes Orbital (vereinfacht, 1 Elektron) Grüne Kugelwolken = einfach besetzt (1 Elektron). In der vereinfachten Darstellung sind sie oben und links gezeichnet. Achtung: Diese ebene Anordnung ist eine Vereinfachung – räumlich stehen alle vier L-Kugelwolken im Tetraeder-Winkel (109,47°) zueinander!● Doppelt besetztes Orbital (vereinfacht, 2 Elektronen) Rote Kugelwolken = doppelt besetzt (2 Elektronen). In der vereinfachten Darstellung sind sie unten und rechts gezeichnet. Diese Anordnung zeigt die Besetzungsunterschiede (grün vs. rot) auf einen Blick – auch wenn die räumliche Realität eine tetraedrische Anordnung ist.💡 Nochmals klicken schließt die Erläuterung.
2.5.1 Feinstruktur der Elektronenhülle
Im Kugelwolkenmodell gelten drei grundlegende Prinzipien, die erklären, wie Elektronen auf die Kugelwolken verteilt werden:
1. Heisenbergsche Unschärferelation (1927)
Es ist nicht möglich, gleichzeitig den Ort, die Geschwindigkeit und die Bewegungsrichtung eines Elektrons anzugeben. Daher lassen sich für Elektronen der Atomhülle keine festen Bahnen, sondern nur Aufenthaltsbereiche angeben.
2. Pauli-Prinzip
In einer „Kugelwolke" können sich maximal 2 Elektronen aufhalten, die sich in einer bestimmten Eigenschaft (Spin) voneinander unterscheiden.
3. Regel von Hund
Energiegleiche Kugelwolken werden zunächst einzeln mit Elektronen besetzt, bevor eine Doppelbesetzung erfolgt.
Das Kugelwolkenmodell ist ein vereinfachtes Orbitalmodell und gilt nur für Hauptgruppenelemente.
🖱️ Interaktiv – Pauli-Prinzip → Finde den Fehler im rechten Modell und klicke darauf🔍 Aufgabe: Das rechte Modell zeigt eine Verletzung des Pauli-Prinzips. Finde das falsche Orbital und klicke darauf! (Tipp: Eines der Orbitale hat zu viele Elektronen.)✅ Dieses Orbital ist korrekt besetzt Dieses Orbital enthält maximal 2 Elektronen – das entspricht dem Pauli-Prinzip. Suche weiter: Das falsche Orbital befindet sich im rechten Modell (falsch, nach Pauli-Prinzip).✅ Dieses Orbital ist korrekt besetzt Auch dieses Orbital im rechten Modell ist korrekt (max. 2 Elektronen). Der Fehler liegt woanders – schau dir alle Orbitale des rechten Modells genau an!🎉 Du hast den Fehler gefunden! Dieses Orbital enthält 3 Elektronen – das ist nach dem Pauli-Prinzip unmöglich!
Pauli-Prinzip: In einer Kugelwolke (= Orbital) können sich maximal 2 Elektronen aufhalten. Diese müssen sich außerdem in ihrer Quanteneigenschaft (dem Spin) voneinander unterscheiden (+½ und −½). Ein drittes Elektron wird vom Orbital „abgewiesen" – es muss in ein anderes Orbital wechseln.💡 Klicke nochmals auf ein Orbital, um die Erläuterung zu schließen.
🖱️ Interaktiv – Hundsche Regel → Finde den Fehler im rechten Modell und klicke darauf🔍 Aufgabe: Das rechte Modell zeigt eine Verletzung der Regel von Hund. Finde das falsch besetzte Orbital und klicke darauf! (Tipp: Energiegleiche Orbitale sollten zuerst einzeln besetzt werden.)✅ Dieses Orbital ist korrekt besetzt – Regel von Hund eingehalten Im linken Modell sind die Orbitale korrekt nach der Regel von Hund besetzt: Energiegleiche Orbitale werden zunächst einzeln mit Elektronen besetzt, bevor eine Doppelbesetzung stattfindet. Das Suchergebnis liegt im rechten Modell – klicke dort auf ein Orbital!🎉 Du hast den Fehler gefunden! Im rechten Modell sind alle Orbitale doppelt besetzt (rot) – obwohl noch ein viertes Orbital leer wäre. Das verstößt gegen die Regel von Hund!
Regel von Hund: Energiegleiche Orbitale (z. B. die drei 2p-Orbitale der L-Schale) werden zunächst einzeln mit einem Elektron besetzt, bevor ein zweites Elektron hinzukommt. Grund: Zwei Elektronen im selben Orbital stoßen sich durch ihre negative Ladung stärker ab – es ist energetisch günstiger, wenn sie verschiedene Orbitale besetzen.💡 Klicke nochmals, um die Erläuterung zu schließen.
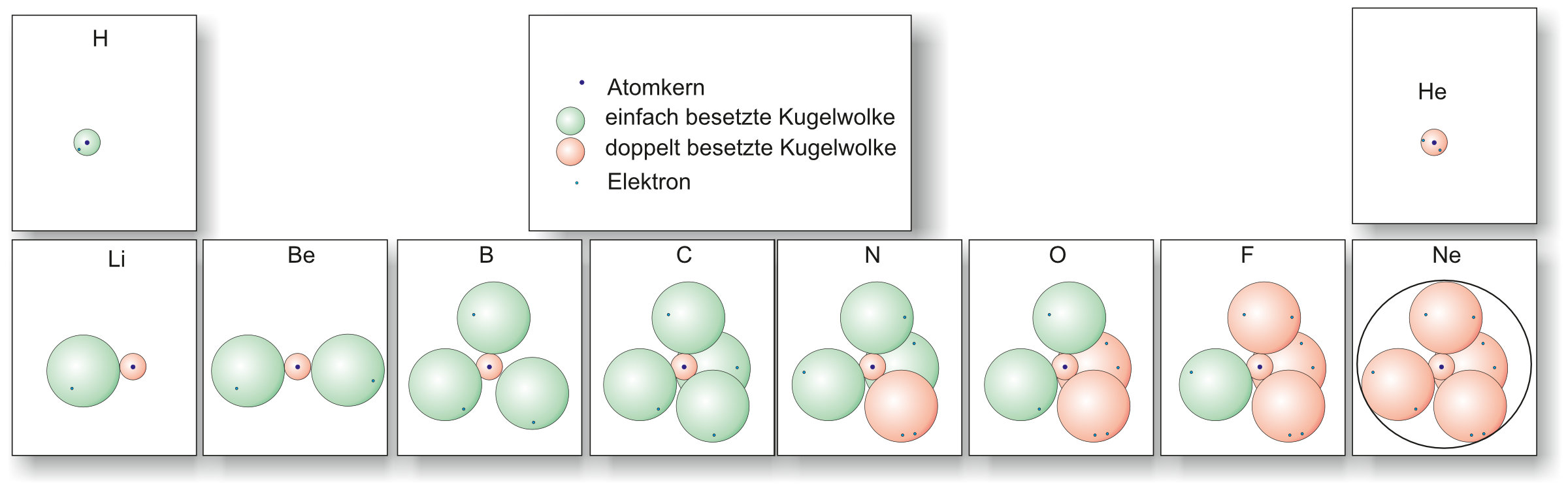
Das KWM der ersten 10 Elemente
Durch Pauli-Prinzip und Regel von Hund ergeben sich folgende Kugelwolkenmodelle für die ersten 10 Elemente. Grün = einfach besetzt · Rot = doppelt besetzt:
↑ Zum Vergrößern klicken
Auf einen Blick – die wichtigsten Aussagen
Kugelwolke
Eine Kugelwolke ist ein Bereich, in dem sich ein Elektron mit ~90 % Wahrscheinlichkeit aufhält. Kein fester Körper – nur ein Wahrscheinlichkeitsbereich.
Pauli-Prinzip
Max. 2 Elektronen pro Kugelwolke, mit entgegengesetztem Spin. Ein drittes Elektron ist ausgeschlossen.
Regel von Hund
Energiegleiche Kugelwolken erst einzeln besetzen, dann doppelt. Gilt für alle Kugelwolken einer Schale.
Farb-Code
Grün = 1 Elektron (einfach besetzt). Rot = 2 Elektronen (doppelt besetzt). Gilt für alle KWM-Darstellungen.
Häufige Fragen – Kugelwolkenmodell
Was ist der Unterschied zwischen dem Bohr-Modell und dem Kugelwolkenmodell?
Im Bohr-Modell bewegen sich Elektronen auf festen Kreisbahnen (Schalen). Das Kugelwolkenmodell ersetzt diese durch Wahrscheinlichkeitsbereiche: Man kann nur angeben, in welchem Bereich sich ein Elektron mit ca. 90 % Wahrscheinlichkeit aufhält – nicht wo es sich genau befindet. → 2.4 Bohr-Schalenmodell
Was ist eine Kugelwolke?
Eine Kugelwolke ist der kugelförmige Bereich, in dem sich ein Elektron mit einer Wahrscheinlichkeit von ca. 90 % aufhält. Wichtig: Kugelwolken sind keine festen Körper, sondern nur Wahrscheinlichkeitsbereiche! In der Kursstufe werden Kugelwolken auch als Orbitale bezeichnet und nach Typ (s, p, d) unterschieden.
Was besagt das Pauli-Prinzip?
Das Pauli-Prinzip (Wolfgang Pauli, 1925): In einer Kugelwolke können sich maximal 2 Elektronen aufhalten, die sich in ihrem Spin (+½ und −½) unterscheiden müssen. Merkhilfe: Die Kugelwolke ist wie ein Zimmer mit 2 Plätzen – beide Bewohner müssen verschieden sein.
Was besagt die Regel von Hund?
Die Regel von Hund (Friedrich Hund, 1925): Energiegleiche Kugelwolken einer Schale werden zunächst einzeln besetzt, bevor eine Doppelbesetzung stattfindet. Grund: Zwei Elektronen in derselben Kugelwolke stoßen sich stärker ab. Merkhilfe: Wie in einem Bus – erst wenn jede Doppelbank einen Fahrgast hat, setzt sich jemand dazu.
Für welche Elemente gilt das Kugelwolkenmodell?
Das vereinfachte Kugelwolkenmodell gilt für Hauptgruppenelemente. Für H bis Ne (Perioden 1 und 2) ist die Darstellung vollständig. Ab der dritten Periode kommen weitere Kugelwolkentypen hinzu. Bei Nebengruppenmetallen reicht das vereinfachte Modell nicht mehr aus. → 2.6 PSE und Atommodelle
Lernkarten – Kugelwolkenmodell
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Kugelwolke und wie unterscheidet sie sich von einer Elektronenbahn?
Kugelwolke = Wahrscheinlichkeitsbereich (~90 %), kein fester Weg. Bohr: Kreisbahn → KWM: kugelförmige Zone.
2Formuliere das Pauli-Prinzip in einem Satz.
In einer Kugelwolke können sich maximal 2 Elektronen aufhalten – sie unterscheiden sich im Spin.
3Formuliere die Regel von Hund mit einem Beispiel.
Energiegleiche Kugelwolken werden erst einzeln besetzt. Beispiel: N (Z=7) → alle drei L-Kugelwolken je 1e (2px¹ 2py¹ 2pz¹).
4Was bedeuten die Farben Grün und Rot in KWM-Darstellungen?
Grün = 1e (einfach besetzt) · Rot = 2e (doppelt besetzt).
5Wie viele Kugelwolken hat die K-Schale, wie viele die L-Schale?
K-Schale: 1 Kugelwolke (max. 2e). L-Schale: 4 Kugelwolken (max. 8e). Die 3 äußeren L-Kugelwolken sind energiegleich.
Weiter im Kapitel: Atombau und PSE
← 2.4 Bohr-Schalenmodell → 2.6 PSE und Atommodelle → 2.7 Lewis-Formeln
🔁 Grundlagen: Rutherford-Modell · Bohr-Schalenmodell · Periodensystem (PSE)
-
2.6 Das Periodensystem der Elemente (PSE) und die Atommodelle
Was du auf dieser Seite lernst
Das Periodensystem der Elemente (PSE) ordnet alle bekannten Elemente nach ihrer Ordnungszahl und gibt dir auf einen Blick Auskunft über Atommasse, Elektronenkonfiguration, Schalen und Valenzelektronen. Du lernst, wie das PSE aufgebaut ist, was Gruppen und Perioden bedeuten und wie du Valenzelektronen ablesen kannst.
Grundlagen aus der 9. Klasse
Um das PSE zu verstehen, solltest du Protonen, Elektronen und Neutronen sowie Elektronenschalen kennen: → 2.3 Rutherford-Modell · → 2.4 Bohr-Schalenmodell · → 2.5 Kugelwolkenmodell
Das Periodensystem der Elemente (PSE)
Periodensystem – Nur Hauptgruppenelemente
↑ Zum Vergrößern klicken · Farben: Alkalimetalle Erdalkalimetalle Metalloide Nichtmetalle Halogene Edelgase
Das Periodensystem der Elemente ist eine große Hilfe, um Voraussagen bezüglich chemischer Reaktionen zu treffen und Eigenschaften zu benennen. Man muss es nicht auswendig lernen – wichtig ist, es lesen zu können.
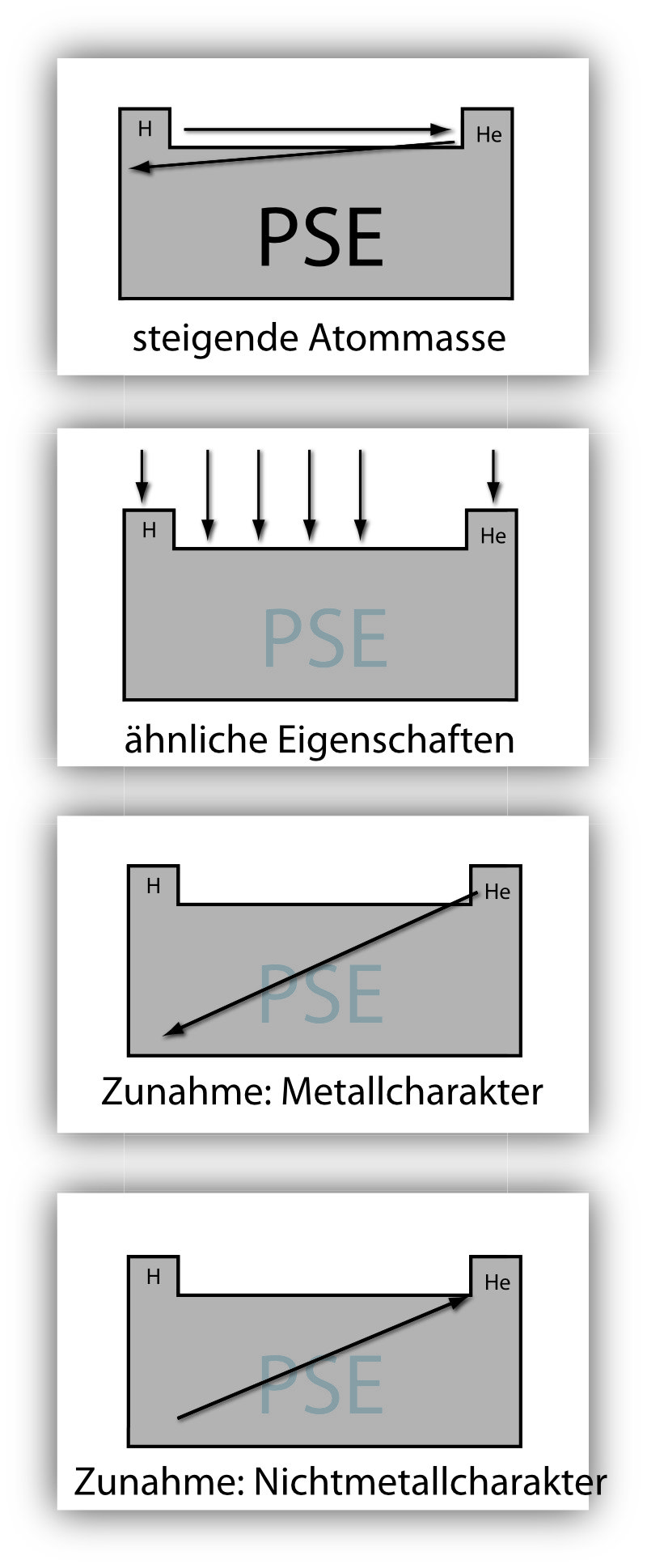
Ursprünglich wurden die Elemente nach steigender Atommasse geordnet. Heute erfolgt die Anordnung nach der Ordnungszahl (= Kernladungszahl = Anzahl der Protonen) und nach periodisch wiederkehrenden Ähnlichkeiten in den Eigenschaften.
Ordnungsprinzipien
- Reihenfolge: Die Elemente sind nach steigender Ordnungszahl (Anzahl der Protonen = Anzahl der Elektronen) angeordnet.
- Periode (= Zeile): Die Periodennummer gibt die Anzahl der Elektronenschalen an.
Beispiel: H, He → 1 Schale · Li…Ne → 2 Schalen · Na…Ar → 3 Schalen - Gruppe (= Spalte): Elemente mit gleicher Anzahl an Außenelektronen (Valenzelektronen) stehen in einer Gruppe.
↑ PSE-Symbol-Erklärung – zum Vergrößern klicken
Bedeutung des PSE
- Voraussage damals unbekannter Elemente (z. B. Germanium – von Mendeleev 1871 vorausgesagt, 1886 entdeckt).
- Ablesen von physikalischen und chemischen Eigenschaften aus der Stellung im PSE.
- Das Kurzperiodensystem enthält nur die Hauptgruppenelemente.
Was bedeuten die Felder eines PSE-Eintrags?
Klicke auf ein farbiges Feld der Elementbox, um zu erfahren, was es bedeutet. Beispiel: Aluminium (Al, Z = 13)
26,981538[Ne]3s²3p¹13 Al6611,5 24676,0Aluminium← Klicke auf ein Feld der Elementbox
🟠 Relative Atommasse (oben) Die relative Atommasse (in u, früher: atomare Masseneinheit) gibt an, wie schwer ein Atom im Verhältnis zu 1/12 des Kohlenstoff-12-Atoms ist. Bei Aluminium: 26,98 u. Sie ist kein ganzzahliger Wert, weil verschiedene Isotope des Elements in der Natur vorkommen und gemittelt werden.⬜ Elektronenkonfiguration Die Elektronenkonfiguration [Ne]3s²3p¹ zeigt, auf welchen Orbitalen die Elektronen des Atoms verteilt sind. [Ne] bedeutet: die Konfiguration des Edelgases Neon ist bereits vollständig besetzt. Dann kommen noch 3s² (2 Elektronen im s-Orbital der 3. Schale) und 3p¹ (1 Elektron im p-Orbital). Das ist Kursstufen-Wissen – in Klasse 9 reicht die Schalen-Angabe.🟢 Elementsymbol und Ordnungszahl Das Elementsymbol (hier: Al) besteht aus 1–2 Buchstaben: 1. Buchstabe immer großgeschrieben, 2. Buchstabe immer klein. Die kleine Zahl links oben (hier: 13) ist die Ordnungszahl (= Kernladungszahl = Anzahl der Protonen = Anzahl der Elektronen im neutralen Atom).🔵 Schmelz-/Siedepunkt und weitere Daten Die vier Zahlen im mittleren Bereich geben (je nach PSE) an:
661 = Schmelzpunkt in °C · 2467 = Siedepunkt in °C
1,5 = Elektronegativität (EN) nach Pauling · 6,0 = weitere Eigenschaft (EN-Skala oder Ionisierungsenergie – je nach PSE-Version). Diese Werte sind für Klasse 9 noch weniger wichtig.🔵 Elementname Der vollständige Name des Elements (hier: Aluminium). Im PSE steht er meist unten. Die Valenzelektronen (Außenelektronen) kannst du aus der Hauptgruppe ablesen: Aluminium steht in der 3. Hauptgruppe → hat 3 Valenzelektronen.Elementarteilchen aus dem PSE ablesen
Mit Hilfe des PSE können wir sehr schnell die Anzahl der einzelnen Elementarteilchen bestimmen. Wichtig ist dabei: Im PSE sind die Elemente immer so notiert, dass sie elektrisch neutral sind.
Beispiel: Natrium 23₁₁Na
Größe Ableitung aus PSE Wert für Na Kernladungszahl (Z) = Ordnungszahl = Anzahl der Protonen = Anzahl der Elektronen 11 Nukleonenzahl (A) = Anzahl der Protonen + Anzahl der Neutronen 23 Neutronen = Nukleonenzahl − Kernladungszahl = 23 − 11 12 Merke: Da das Atom elektrisch neutral ist → Anzahl Protonen (11+) = Anzahl Elektronen (11−) → Ladung = 0
⚠️ Die Nukleonenzahl im PSE ist ein gerundeter Wert (relative Atommasse). Für exakte Berechnungen wird der ganzzahlige Wert des häufigsten Isotops verwendet.Übungen: Elementarteilchen aus dem PSE ablesen
Überlege zunächst selbst, dann klappe die Lösung auf.
Afg. 1 Nenne die Anzahl der Elektronen von Kohlenstoff (C).
Lösung: C hat die Ordnungszahl 6 → 6 Elektronen (= 6 Protonen, da elektrisch neutral).Afg. 2 Nenne die Anzahl der Protonen von Brom (Br).
Lösung: Br hat die Ordnungszahl 35 → 35 Protonen.Afg. 3 Nenne die Anzahl der Neutronen von Schwefel (S, Nukleonenzahl 32).
Lösung: S: Ordnungszahl = 16 (Protonen), Nukleonenzahl ≈ 32 → Neutronen = 32 − 16 = 16 Neutronen.Afg. 4 Wie groß ist die Masse von einem Bor-Atom (B)?
Lösung: Die relative Atommasse von B beträgt ca. 10,81 u (aus dem PSE ablesbar).Afg. 5 Nenne das Symbol und die Anzahl der Protonen von Gallium.
Lösung: Symbol: Ga · Ordnungszahl: 31 Protonen.Perioden = Anzahl der Elektronenschalen
Niels Bohr zeigte, dass sich die Elektronen auf unterschiedliche Energieniveaus (= „Schalen") verteilen. Diese Anzahl der Schalen findest du auch im PSE wieder – nämlich in der Angabe der Zeile (= Reihe = Periode).
H, He → Periode 1 → 1 Schale (K-Schale)Li … Ne → Periode 2 → 2 Schalen (K, L)Na … Ar → Periode 3 → 3 Schalen (K, L, M)Rb, Sr … → Periode 5 → 5 Schalen🔑 Merke: Die Periodennummer im PSE = die Anzahl der besetzten Elektronenschalen des Atoms.
Übungen: Perioden und Elektronenschalen
Afg. 1 Nenne alle Elemente, die nur 1 Energieniveau/Schale besitzen.
Lösung: H (Wasserstoff) und He (Helium) – beide stehen in Periode 1 → 1 Schale (K-Schale).Afg. 2 Wie viele „Schalen" besitzt Phosphor (P)?
Lösung: P steht in Periode 3 → 3 Schalen (K, L, M-Schale).Afg. 3 Wie viele Energieniveaus besitzt Xenon (Xe)?
Lösung: Xe steht in Periode 5 → 5 Energieniveaus.Afg. 4 Wie viele Elektronenschalen besitzt Sauerstoff (O)?
Lösung: O steht in Periode 2 → 2 Schalen (K- und L-Schale).Haupt- und Nebengruppenelemente
Im PSE unterscheidet man zwei Typen von Elementen:
Hauptgruppenelemente (grün)
Die Elemente der 1., 2. und 13.–18. Gruppe. Sie unterscheiden sich stärker voneinander. Ihre Anzahl an Valenzelektronen ist direkt aus der Hauptgruppennummer ablesbar. Im Kurzperiodensystem sind nur Hauptgruppenelemente enthalten.
Nebengruppenelemente (grau)
Die Elemente der 3.–12. Gruppe (Übergangsmetalle). Sie besitzen entweder 1 oder 2 Außenelektronen und sind sich chemisch recht ähnlich. Auf den folgenden Seiten werden sie zunächst „weggeschnitten", um mehr Platz zu haben.
Hauptgruppen-Namen: I. HG: Alkalimetalle · II. HG: Erdalkalimetalle · III. HG: Borgruppe · IV. HG: Kohlenstoffgruppe · V. HG: Stickstoffgruppe · VI. HG: Chalkogene (Erzbildner) · VII. HG: Halogene (Salzbildner) · VIII. HG: Edelgase
⚠️ Metallischer vs. nichtmetallischer Charakter: Metallischer Charakter nimmt nach links unten zu · Nichtmetallischer Charakter nimmt nach rechts oben zu · Halbmetalle stehen diagonal dazwischen.
Valenzelektronen und Hauptgruppennummer
Innerhalb einer Hauptgruppe stehen häufig chemisch sich ähnelnde Elemente. Für die chemischen Eigenschaften sind vor allem die Außenelektronen (= Valenzelektronen) verantwortlich.
Die Hauptgruppennummer (gelb unterlegt im PSE) gibt die Anzahl der Valenzelektronen wieder. „Chemie ist die Physik der Valenzelektronen!"
1. HauptgruppeH, Li, Na, K, Rb, Cs, Fr1Valenzelektron2. HauptgruppeBe, Mg, Ca, Sr, Ba, Ra2Valenzelektronen3. HauptgruppeB, Al, Ga, In, Tl3Valenzelektronen7. HauptgruppeF, Cl, Br, I, At7Valenzelektronen8. HauptgruppeHe, Ne, Ar, Kr, Xe, Rn8Valenzelektronen (Edelgase)🔑 Merke: H ist in der 1. HG → 1 Valenzelektron · O ist in der 6. HG (VIA) → 6 Außenelektronen · Edelgase haben 8 Valenzelektronen (He: 2) → besonders stabil (→ Edelgasregel)
Übungen: Valenzelektronen und Hauptgruppenelemente
Für diese Übungen benötigst du das PSE. Bei Klassenarbeiten (und im Abitur) darf es verwendet werden.
Afg. 1 Wie viele Außenelektronen besitzt Rubidium (Rb)?
Lösung: Rb steht in der 1. Hauptgruppe → 1 Außenelektron.Afg. 2 Wie viele Valenzelektronen hat Stickstoff (N)?
Lösung: N steht in der 5. Hauptgruppe (VA) → 5 Valenzelektronen.Afg. 3 Wie viele Valenzelektronen hat Aluminium (Al)?
Lösung: Al steht in der 3. Hauptgruppe → 3 Valenzelektronen.Afg. 4 Wie viele Außenelektronen besitzt die 4. Hauptgruppe?
Lösung: Alle Elemente der 4. HG (C, Si, Ge, Sn, Pb, Fl) haben 4 Außenelektronen.Afg. 5 Wie viele Außenelektronen besitzt Calcium (Ca)?
Lösung: Ca steht in der 2. Hauptgruppe → 2 Außenelektronen.Afg. 6 Wie viele Valenzelektronen hat Chlor (Cl)?
Lösung: Cl steht in der 7. Hauptgruppe (VIIA / Halogene) → 7 Valenzelektronen.Afg. 7 Wie viele Valenzelektronen hat Helium (He)?
Lösung: He ist ein Edelgas (8. HG) – aber eine Ausnahme: es hat nur 2 Valenzelektronen (K-Schale voll mit 2e).Afg. 8 Wie viele Außenelektronen besitzt die 8. Hauptgruppe (Edelgase)?
Lösung: Alle Edelgase (außer He) haben 8 Außenelektronen → vollständig besetzte Außenschale → besonders stabil → kaum Reaktionen.📥 PSE zum Downloaden: Periodensysteme (PSE) herunterladen → (Bei Klassenarbeiten und im Abitur darf das PSE verwendet werden.)
Auf einen Blick – die wichtigsten Aussagen
Ordnungszahl
Die Ordnungszahl = Kernladungszahl = Anzahl der Protonen = Anzahl der Elektronen (neutral).
Periode
Die Periodennummer = Anzahl der besetzten Elektronenschalen (Energieniveaus).
Hauptgruppe
Die Hauptgruppennummer = Anzahl der Valenzelektronen (Außenelektronen). Entscheidet über chemische Eigenschaften.
Nukleonenzahl
Nukleonenzahl = Protonen + Neutronen. Neutronen = Nukleonenzahl − Ordnungszahl.
Häufige Fragen – PSE und Atombau
Wie lese ich die Ordnungszahl, Atommasse und Valenzelektronen aus dem PSE ab?
Die Ordnungszahl steht oben links beim Elementsymbol (= Anzahl der Protonen). Die relative Atommasse steht meist oben im Feld. Die Valenzelektronen (Außenelektronen) entsprechen direkt der Hauptgruppennummer. Beispiel: Chlor (Cl) steht in der 7. Hauptgruppe → 7 Valenzelektronen, Ordnungszahl 17 → 17 Protonen, 17 Elektronen.
Was ist der Unterschied zwischen Gruppe und Periode im PSE?
Eine Periode ist eine waagerechte Zeile. Die Periodennummer gibt an, wie viele Elektronenschalen das Atom hat. Eine Gruppe (= Spalte) fasst Elemente mit gleicher Anzahl an Valenzelektronen zusammen – sie haben daher ähnliche chemische Eigenschaften. Beispiel: Alle Alkalimetalle (1. HG) haben 1 Valenzelektron und reagieren ähnlich mit Wasser.
Was sind Valenzelektronen und warum sind sie wichtig?
Valenzelektronen (= Außenelektronen) befinden sich auf der äußersten besetzten Elektronenschale. Sie sind entscheidend für alle chemischen Reaktionen, weil Atome bevorzugt ihre äußere Schale vollständig besetzen wollen (→ Edelgasregel). Die Anzahl der Valenzelektronen ist direkt aus der Hauptgruppennummer ablesbar.
Wie berechne ich die Anzahl der Neutronen eines Atoms?
Neutronen = Nukleonenzahl − Ordnungszahl (= Nukleonenzahl − Protonenzahl). Beispiel: Natrium ²³Na → Nukleonenzahl 23, Ordnungszahl 11 → 23 − 11 = 12 Neutronen. Achtung: Die im PSE angegebene Atommasse ist ein Mittelwert über alle Isotope – für die Neutronenberechnung nimmt man den gerundeten ganzzahligen Wert.
Was ist der Unterschied zwischen Haupt- und Nebengruppenelemente?
Hauptgruppenelemente stehen in Gruppe 1–2 und 13–18. Die Hauptgruppennummer entspricht direkt der Anzahl der Valenzelektronen. Nebengruppenelemente (Gruppen 3–12, Übergangsmetalle wie Eisen, Kupfer, Zink) haben meistens 1–2 Valenzelektronen. Im Kurzperiodensystem werden Nebengruppen oft weggelassen. → 2.7 Lewis-Formeln
Lernkarten – PSE und Atombau
Klicke auf eine Karte, um die Antwort zu sehen.
1Was gibt die Ordnungszahl im PSE an?
Ordnungszahl = Anzahl der Protonen = Anzahl der Elektronen (im neutralen Atom) = Kernladungszahl.
2Was sagt die Periode (Zeile) im PSE aus?
Die Periodennummer = Anzahl der besetzten Elektronenschalen (Energieniveaus) des Atoms.
3Wie viele Valenzelektronen hat Chlor? Wie liest du das ab?
Cl steht in der 7. Hauptgruppe → 7 Valenzelektronen. Hauptgruppennummer = Anzahl der Valenzelektronen.
4Wie berechnet man die Anzahl der Neutronen?
Neutronen = Nukleonenzahl − Ordnungszahl. Beispiel: Na ²³Na → 23 − 11 = 12 Neutronen.
5Wie viele Valenzelektronen haben Edelgase und warum sind sie so stabil?
Edelgase haben 8 Valenzelektronen (He: 2) → vollständig besetzte Außenschale → energetisch sehr stabil → kaum Reaktionen (→ Edelgasregel).
Weiter im Kapitel: Atombau und PSE
← 2.5 Kugelwolkenmodell → 2.7 Lewis-Formeln → 3. Edelgasregel
🔁 Grundlagen: Rutherford · Bohr-Schalenmodell · Kugelwolkenmodell · PSE herunterladen
-
4.2 Atomradien
4.2 Atomradien
{slider title="Link zur interaktiven Übungsseite mit Bildern" open="false" class="icon"}
{/sliders}
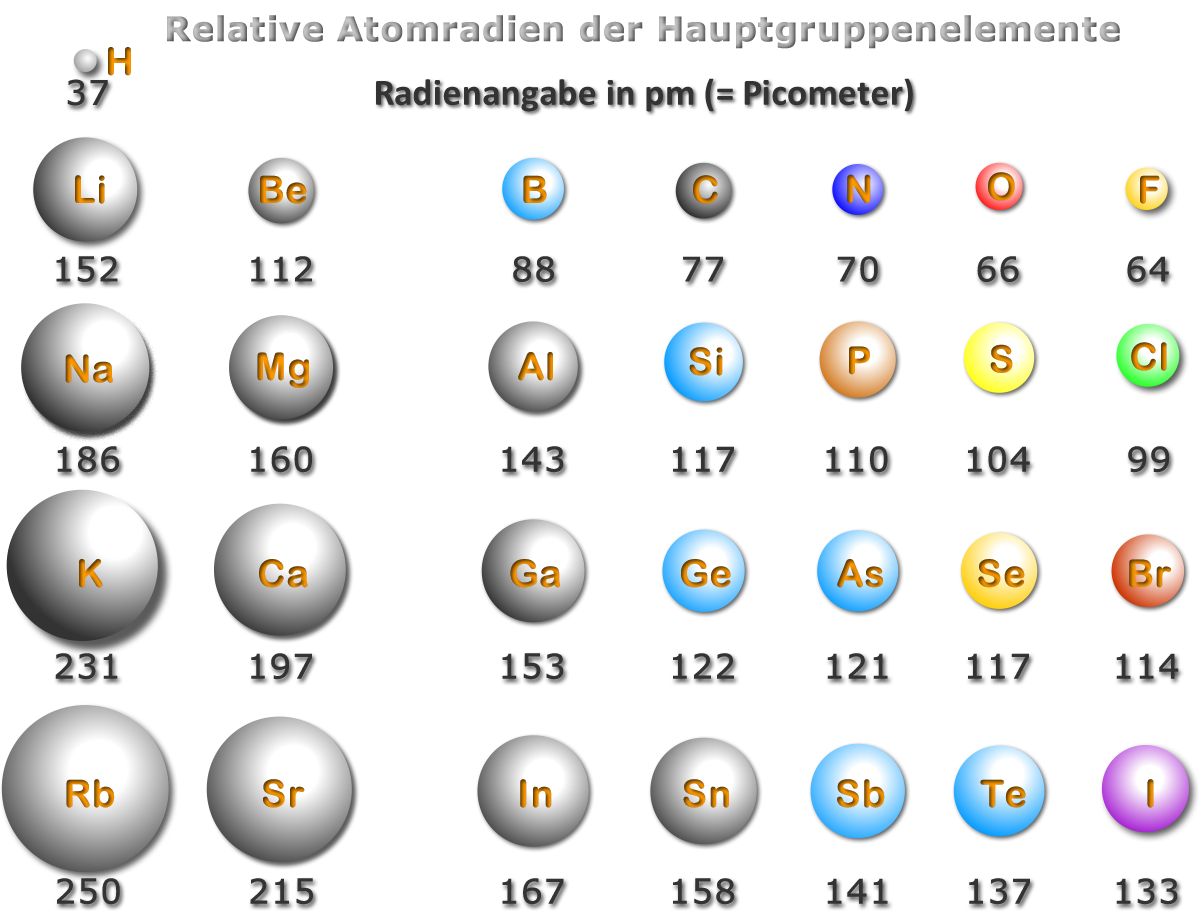
Folgende Abbildung zeigt, wie der Zusammenhang der Atomradien und das PSE ist.
Überlegt Euch die Erklärungen dafür, dass die Atomradien von oben nach unten und von rechts nach links zunehmen.
Innerhalb einer Hauptgruppe:
{slider title="Lösung" open="false" class="icon"}
Atomradien nehmen von oben nach unten zu, da die Anzahl der Schalen zunimmt.
{/sliders}
Innerhalb einer Periode:
{slider title="Lösung" open="false" class="icon"}
Atomradien nehmen von links nach rechts ab. Da die Anzahl der Protonen steigt, werden die Elektronen stärker vom Atomkern angezogen.
Diese Anziehung überwiegt die Abstoßung der Elektronen untereinander.{/sliders}