Elementarteilchen
-
1. Elementarteilchen – Proton, Neutron, Elektron
Was du auf dieser Seite lernst
Atome bestehen aus nur drei verschiedenen Bausteinen: Proton, Neutron und Elektron. Du lernst ihre Eigenschaften (Ladung, Masse, Ort im Atom) kennen, verstehst den Unterschied zwischen Ordnungszahl und Massenzahl und kannst die Gesamtladung eines Teilchens berechnen.
Grundlagen aus der 8. Klasse
Das Dalton-Modell (Atom als unteilbare Kugel) hast du bereits in der 8. Klasse kennengelernt: → Atommodell nach Dalton (Kl. 8)
Die drei Elementarteilchen – Bausteine der Atome
Atome bestehen aus genau drei verschiedenen Bausteinen. Fahre mit der Maus über die Kugeln (oder tippe sie an), um mehr zu erfahren:
ProtonDas Proton (p⁺):
Befindet sich im Atomkern
Ladung: +1
Relative Masse: 1 u (genau: 1,0073 u)NeutronDas Neutron (n⁰):
Befindet sich im Atomkern
Ladung: 0 (neutral)
Relative Masse: 1 u (genau: 1,0087 u)ElektronDas Elektron (e⁻):
Befindet sich in der Atomhülle
Ladung: −1
Relative Masse: ≈ 0 u (genau: 0,0005 u)↑ Mit der Maus über die Kugeln fahren (oder antippen)
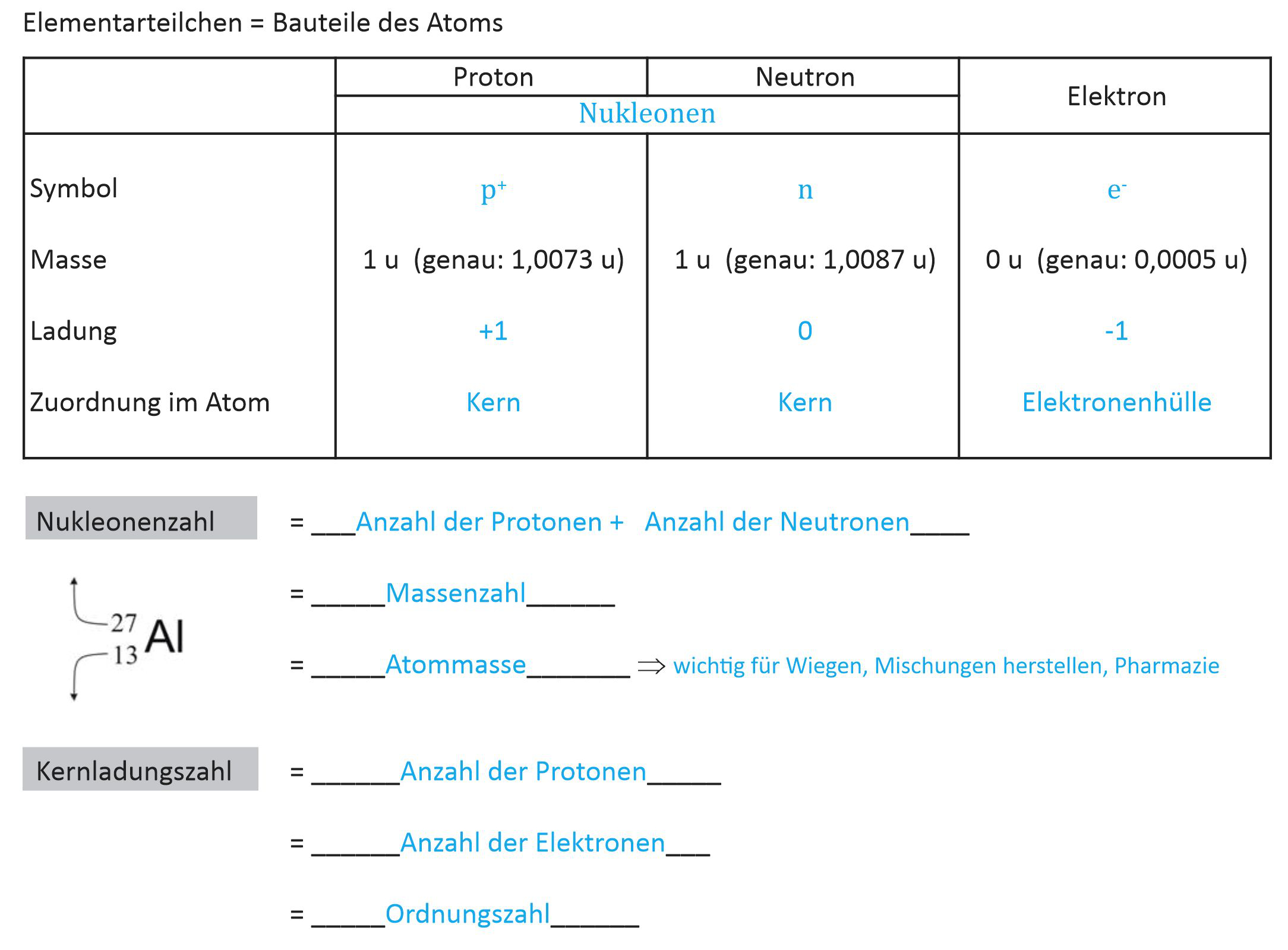
Übersichtstabelle der Elementarteilchen
Teilchen Symbol Rel. Masse Ladung Ort im Atom Proton p⁺ 1 u +1 Atomkern Neutron n⁰ 1 u 0 Atomkern Elektron e⁻ ≈ 0 u −1 Atomhülle Ordnungszahl und Massenzahl
Die Ordnungszahl (auch: Kernladungszahl) gibt die Anzahl der Protonen im Atomkern an. Sie bestimmt die Stellung des Elements im Periodensystem. Im neutralen Atom gilt immer: Protonenzahl = Elektronenzahl.
Die Massenzahl ist die Summe aus Protonen und Neutronen:
Massenzahl = Anzahl der Protonen + Anzahl der Neutronen
Gesamtladung eines Teilchens berechnen
Die Gesamtladung ergibt sich durch einfaches Addieren aller Einzelladungen. Protonen (+1) und Elektronen (−1) werden gezählt, Neutronen (0) fallen dabei heraus.
Beispiel
Ein Teilchen besteht aus 3 Protonen, 3 Neutronen und 2 Elektronen. Wie groß ist die Ladung?
3 × (+1) = +3 (Protonen)
3 × ( 0) = 0 (Neutronen)
2 × (−1) = −2 (Elektronen)
+3 + 0 + (−2) = +1
→ Die Ladung ist 1+Teilchen-Modell
● Proton ● Neutron ● Elektron
Auf einen Blick – die wichtigsten Aussagen
PROTON
Im Atomkern, Ladung +1, Masse 1 u. Die Protonenzahl = Ordnungszahl = Stellung im PSE.
NEUTRON
Im Atomkern, Ladung 0, Masse 1 u. Beeinflusst die Masse, nicht die Ladung.
ELEKTRON
In der Atomhülle, Ladung −1, Masse ≈ 0 u. Bestimmt das chemische Verhalten.
NEUTRALES ATOM
Im neutralen Atom gilt immer: Protonen = Elektronen. Massenzahl = Protonen + Neutronen.
Häufige Fragen – Elementarteilchen
Aus welchen Teilchen besteht ein Atom?
Jedes Atom besteht aus drei Typen von Elementarteilchen: Protonen und Neutronen im Atomkern, Elektronen in der Atomhülle. Protonen sind positiv (+1), Neutronen neutral (0), Elektronen negativ (−1).
Was ist der Unterschied zwischen Ordnungszahl und Massenzahl?
Die Ordnungszahl gibt die Protonenzahl an und bestimmt die Position im Periodensystem. Die Massenzahl = Protonen + Neutronen und entspricht der ungefähren Atommasse in u. Beispiel Kohlenstoff (C): Ordnungszahl 6, Massenzahl 12 → 6 Protonen + 6 Neutronen.
Warum hat das Elektron eine vernachlässigbare Masse?
Die Elektronenmasse beträgt nur ca. 0,0005 u – etwa 1/1836 der Protonenmasse. In der Schulchemie wird sie als ≈ 0 u vereinfacht. Die Atommasse wird praktisch vollständig durch Protonen und Neutronen bestimmt.
Wie berechnet man die Ladung eines Ions?
Man addiert die Ladungen aller Elementarteilchen: Proton = +1, Elektron = −1, Neutron = 0. Ein Kation (positiv) entsteht durch Elektronenabgabe, ein Anion (negativ) durch Elektronenaufnahme. Beispiel: Na⁺ hat 11 Protonen und 10 Elektronen → Ladung = +1.
Was sind Isotope?
Isotope sind Atome desselben Elements mit gleicher Protonenzahl, aber unterschiedlicher Neutronenzahl (→ verschiedene Massenzahlen). Beispiel: ¹²C und ¹⁴C haben beide 6 Protonen, aber 6 bzw. 8 Neutronen. Chemisch verhalten sie sich identisch.
Lernkarten – Elementarteilchen
Klicke auf eine Karte, um die Antwort zu sehen.
1Nenne Symbol, Ladung, relative Masse und Aufenthaltsort des Protons.
Symbol: p⁺
Ladung: +1
Rel. Masse: 1 u
Ort: Atomkern2Nenne Symbol, Ladung, relative Masse und Aufenthaltsort des Neutrons.
Symbol: n⁰
Ladung: 0 (neutral)
Rel. Masse: 1 u
Ort: Atomkern3Nenne Symbol, Ladung, relative Masse und Aufenthaltsort des Elektrons.
Symbol: e⁻
Ladung: −1
Rel. Masse: ≈ 0 u
Ort: Atomhülle4Was ist die Ordnungszahl? Was sagt die Massenzahl aus?
Ordnungszahl = Protonenzahl (= Elektronenzahl im neutralen Atom); Stellung im PSE.
Massenzahl = Protonen + Neutronen5Schwefel (S, OZ = 16, MZ = 32): Wie viele Protonen, Neutronen und Elektronen? Welche relative Atommasse?
Protonen: 16
Neutronen: 32 − 16 = 16
Elektronen (neutral): 16
Rel. Atommasse: 16 + 16 = 32 u
Weiter im Kapitel – Vom Atombau bis ZMK
← Kapitelübersicht → Atommodelle: Demokrit und Dalton
🔁 Grundlagen: Atommodell nach Dalton (Kl. 8)
-
2.3 Rutherford: Kern-Hülle-Modell
2.3 Rutherford: Kern-Hülle-Modell
Atome bestehen aus:
- sehr kleinen, positiv geladenen Kern
- negativekugelförmige Elektronenhülle
- die Elektronenbewegen sich mit hoher Geschwindigkeit um den Kern.
Ein Atommodell, das zwischen Atomkern und Elektronenhülle unterscheidet, wird als Kern-Hülle-Modell bezeichnet.
Die Teilchen, aus denen ein Atom besteht, bezeichnet man als Elementarteilchen (Protonen, Neutronen und Elektronen).
{slider title="Link zur Übungsseite" open="false" class="icon"}
⇒ Interaktive Übungsseiten zu Elementarteilchen und deren Anziehung oder Abstoßung.
{/sliders}
2.3.1 Der Atomkern
{slider title="Link zur Übungsseite" open="false" class="icon"}
⇒ Interaktive Übungsseiten zum Atomkern und Atomhülle
{/sliders}
- Der Atomkern ist aus Protonenund Neutronenaufgebaut.
- Die Protonenzahlstimmt mit der Ordnungszahleines Elements und der Kernladungszahl überein.
Bsp.: Fluor = ₉F: 9 Protonen: Ordnungszahl und Kernladungszahl = 9, Elektronenanzahl= 9. - Nukleonenzahl: Anzahl der Protonen+ Anzahl der Neutronen im Atomkern.
Bsp: Die Nukleonenzahl von Fluor ¹⁹F ist 19 ⇒ 9 Protonenund 10 Neutronen - Massenzahl
Die Atommasse ist angenähert die Summe der Protonen- und Neutronenmasse. Die Masse der Elektronenist außerordentlich klein. - Schreibweise
Na, alles verstanden? Hier gibt es einen Ausschnitt eines Übungsarbeitsblattes. Hinter dem Slider ist dann die Lösung:
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
2.4 Bohr – Schalenmodell der Elektronenhülle
2.4 Bohr – Schalenmodell der Elektronenhülle
{slider title="Link zur Übungsseite" open="false" class="icon"}
Link zur Übungsseiten zum Bohrsschen Schalenmodell (mit vielen Abbildung)
{/sliders}
a) Ionisierungsenergien eines Neon-Atoms
Man hat herausgefunden, dass wohl nicht alle Elektronen "gleich" in der Hülle "verteilt" sind. Mit Hilfe von einem Experiment, in dem man nach und nach alle Elektronen von einem Neon-Atom entfernt kann man es nachweisen.
{slider title="Experiment mit Ergebnissen zur Ionisierung eines Neon-Atoms" open="false" class="icon"}
Ionisierungsenergien eines Neon-Atoms [MJ/mol], also die Energie, die man benötigt um das Elektron zu entfernen. Durchnummeriert vom 1. Elektron bis zum 10. Elektron:
- e⁻ = 2,1 MJ/mol
- e⁻ = 3,9 MJ/mol
- e⁻ = 6,2 MJ/mol
- e⁻ = 9,4 MJ/mol
- e⁻ = 12,2 MJ/mol
- e⁻ = 15,2 MJ/mol
- e⁻ = 20,0MJ/mol
- e⁻ = 23,0 MJ/mol
- e⁻ = 115,0 MJ/mol
- e⁻ = 130,0 MJ/mol
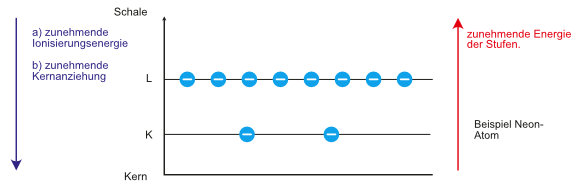
Beobachtung: Man benötigt immer mehr Energie, um das erste, zweite, dritte und die folgenden Elektronen vollständig abzutrennen.
Folgerung: Der verbleibende „Rumpf“ wird immer positiver und damit erfordert die Abrennung der folgenden Elektronen immer größere Energie.
Beobachtung: Man benötigt zur Abspaltung der beiden letzten Elektronen (z.B. im Vergleich zum drittletzten Elektron) besonders viel Energie.
Folgerung: Die Elektronen des Neons lassen sich in zwei Gruppen einteilen.
- Die zwei Elektronen mit großer Ionisierungsenergie sind im zeitlichen Mittel näher am Kern.
- Die acht Elektronen mit relativ kleinen Ionisierungsenergien sind im zeitlichen Mittel weiter vom Kern entfernt.
{/sliders}
b. Energiestufenschema (Neon-Atom)
Ein Neon-Atom könnte man mit der Elektronenverteilung wie folgt aufschreiben:
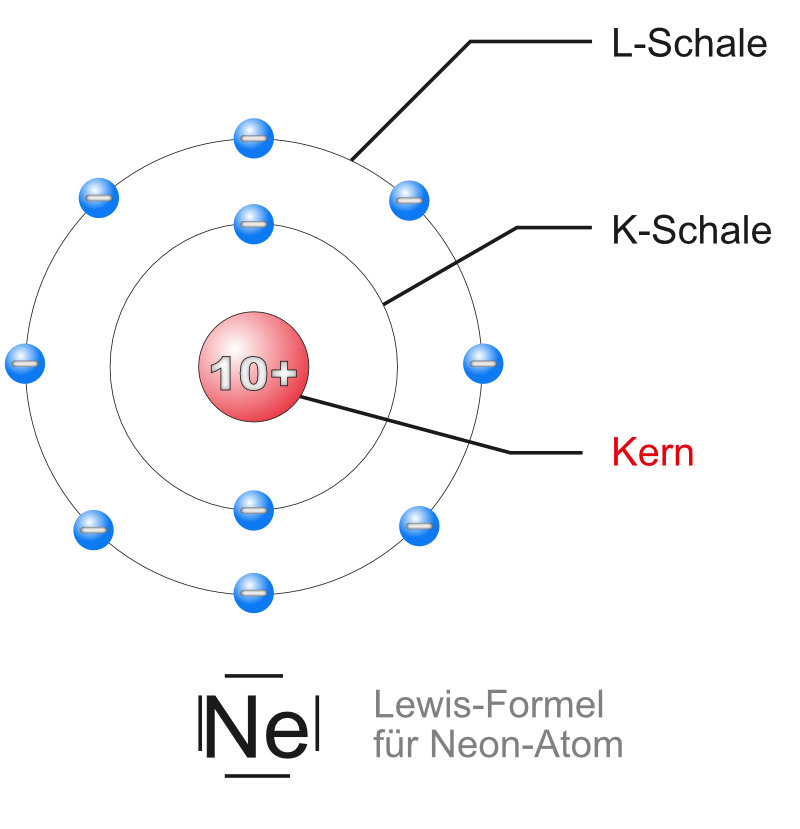
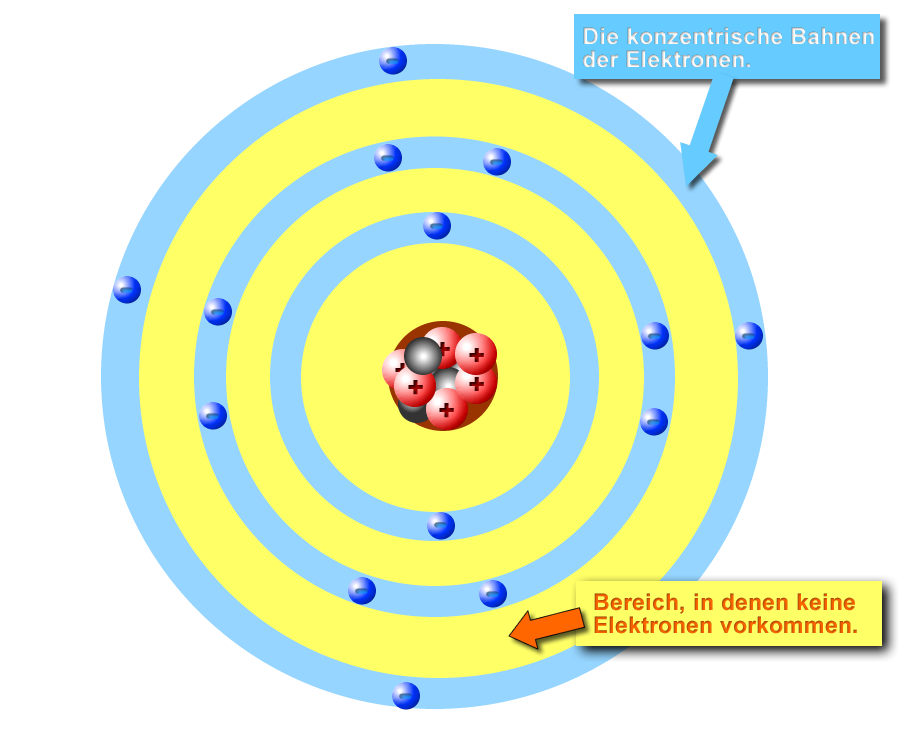
c. Schalenmodell (Neon-Atoms)
Die Energiestufen lassen sich als konzentrischen Kugelschalen um den Kern veranschaulichen. Man erhält damit ein „Schalenmodell“ des Neonatoms (mit Lewis-Formel). Hinweis: Der Kern ist zusammengefasst. Eigentlich müsste man dort 10 Protonen und 10 Neutronen zeichnen, aber das macht die Sache nicht anschaulicher. Deshalb nur ein "Kern" mit der Ladung.
Die Elektronen sind verteilt "auf" den Schalen dargestellt, die kugelförmig den Bereich der Elektronenangeben. In der inneren Schale sind es zwei Elektronen in der äußeren Schale acht.
Weitere Beispiele (Abbildungen aus der interaktiven Seite; ausführlichere Erklärungen siehe dort).
Schalenmodell eines Aluminium-Atoms
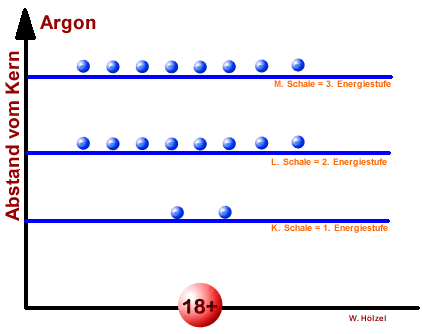
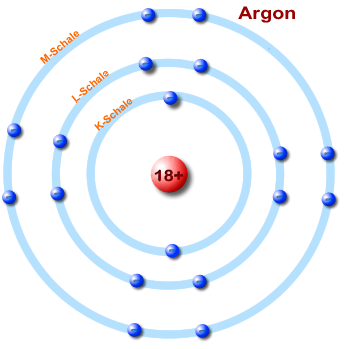
Vergleich - Energiestufen vers. Schalenmodell eines Argon-Atoms
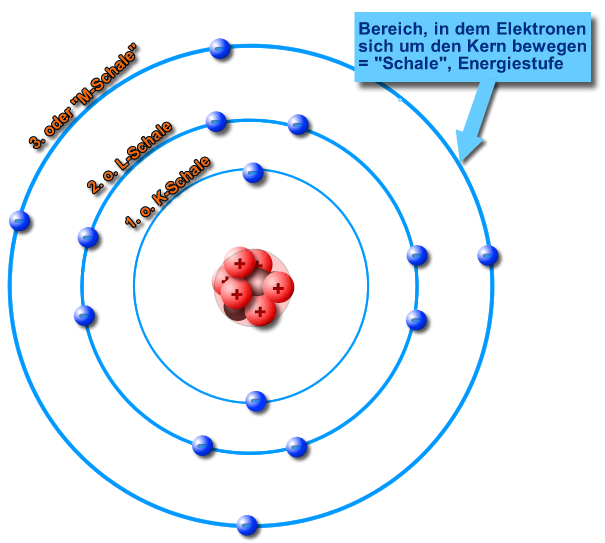
Atomschalen
d) Postulate (= Grundannahmen) von Niels Bohr:
1. Die Elektronen bewegen sich nur auf ganz bestimmten, genau definierten Bahnen (= Energiestufen, Energieschalen, Schalen) um den Atomkern. Die Elektronen bewegen sich nicht zwischen dieser Energiestufen.
2. Jede Schale kann maximal 2 n² Elektronen aufnehmen
n = Schalennummer
n = 1, 2, 3, 4,...
K, L, M, N,... Schale3. Für jede Bahn, auf der das Elektron den Atomkern umkreist, hat das Elektron eine bestimmte Energie. Auf der K-Schale (n = 1), die dem Atomkern am nächsten ist, kommt dem Elektron die geringste Energie zu.