Gleichgewichtsreaktionen
-
02 Gleichgewichte
Was du auf dieser Seite lernst
Konzentrierte Schwefelsäure ist hygroskopisch – sie nimmt begierig Wasser aus der Luft auf. Auf dieser Seite untersuchst du, wie sich dabei ein dynamisches Gleichgewicht einstellt, und lernst die zweistufige Protolyse der Schwefelsäure mit Wasser kennen.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säure-Base-Reaktionen und der Bronsted-Definition hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9)
2.1 Schwefelsäure – Wasserdampf – Gleichgewicht
a) konzentrierte Schwefelsäure (H2SO4)
- enthält Schwefelsäuremoleküle
- zeichnet einmal die Strukturformel(n) (unter Berücksichtigung, dass die Edelgas-Regel erfüllt sein muss):
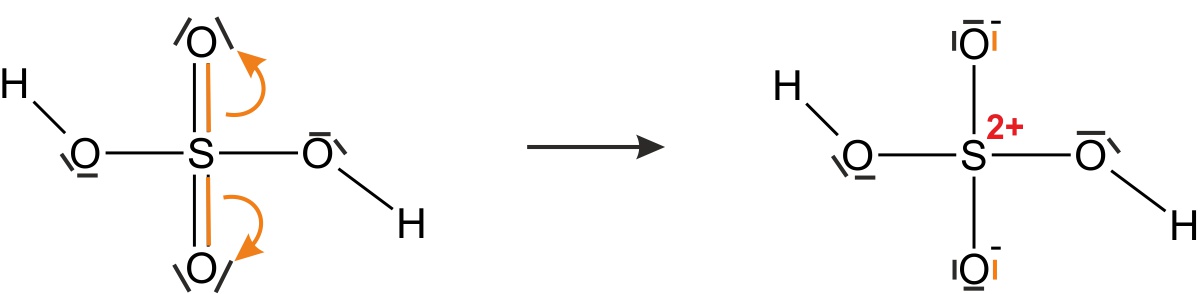
- Konzentrierte Schwefelsäure ist geruchlos.
- Siedetemperatur beträgt 300 °C.
- Konzentrierte Schwefelsäure reagiert heftig mit Wasser unter Ionenbildung (Protolyse-Reaktion).
Formuliert für die Reaktion der Schwefelsäure mit Wasser in zwei Stufen die Reaktionsgleichung in Summenformeln:
Lösung: Reaktionsgleichungen (zweistufige Protolyse)
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O → SO42− + H3O+b) Verdünnte Schwefelsäure
Verdünnte Schwefelsäure enthält folgende Ionen und Moleküle; nennt diese:Lösung: Bestandteile verdünnter Schwefelsäure
- H3O+ (Oxonium-Ion; früher Hydronium-Ion oder „Hydroxonium-Ion")
- HSO4− (Hydrogensulfat-Ion)
- SO42− (Sulfat-Ion; in geringer Konzentration)
- H2O (Wasser; in großer Menge vorhanden)
2.2 Langzeitversuch: Konzentrierte Schwefelsäure
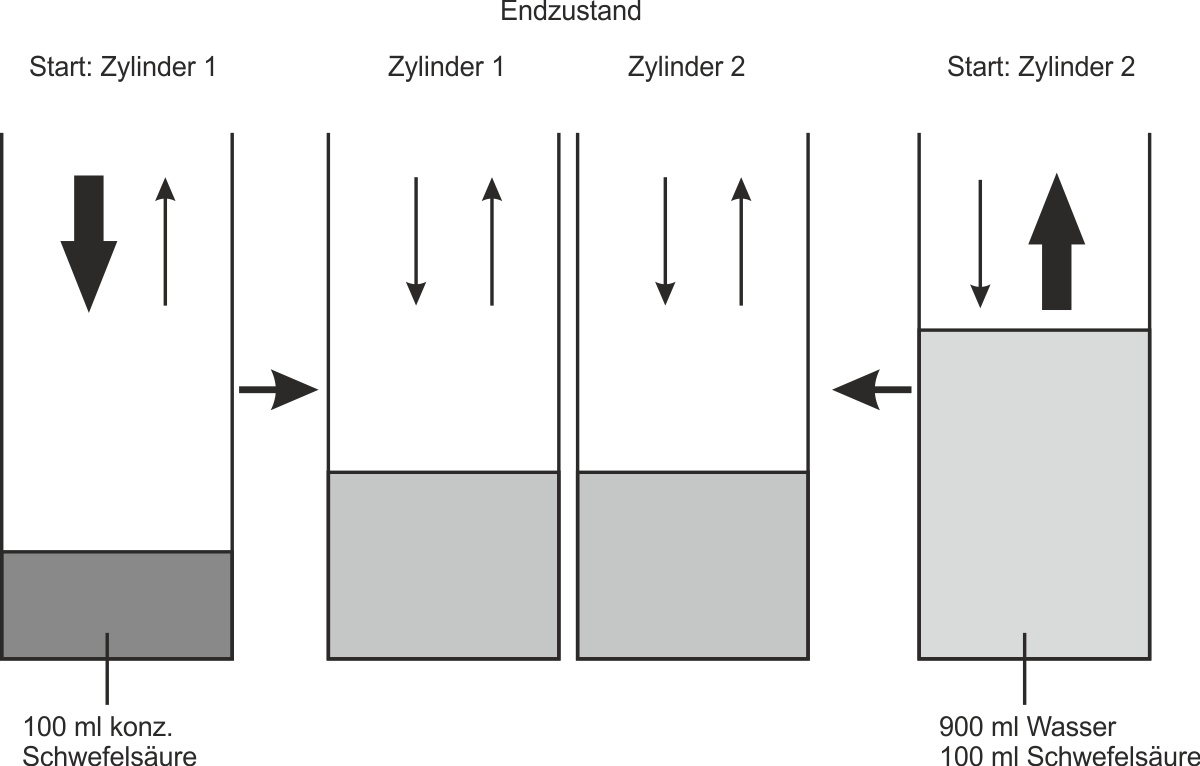
Versuchsdurchführung: In einen Zylinder 1 werden 100 ml konzentrierte Schwefelsäure gegeben. In einen Zylinder 2 werden zunächst 900 ml Wasser und dann vorsichtig 100 ml konzentrierte Schwefelsäure gegeben. Beide Zylinder werden mehrere Jahre offen im gleichen Zimmer stehengelassen.
↑ Zum Vergrößern klicken
✕
Versucht eine Deutung dieses Versuchs:
Lösung: Deutung des Langzeitversuchs
- Zylinder 1 (konz. H2SO4) nimmt mehr H2O-Moleküle aus der Umgebungsluft auf, als er abgibt.
- Zylinder 2 (verdünnte H2SO4) gibt mehr H2O-Moleküle an die Umgebungsluft ab, als er aufnimmt.
- Nach einigen Jahren hat sich ein Gleichgewichtszustand eingestellt: Pro Zeiteinheit werden gleich viele H2O-Moleküle an die Umgebung abgegeben wie H2O-Moleküle in die Lösung aufgenommen werden.
Auf einen Blick – die wichtigsten Aussagen
Hygroskopie
Konzentrierte H2SO4 ist hygroskopisch – sie zieht Wasser aus der Luft an. Je konzentrierter die Lösung, desto stärker diese Eigenschaft.
Dynamisches Gleichgewicht
Im Gleichgewicht sind Auf- und Abgabe von H2O-Molekülen gleich groß – es herrscht mikroskopische Aktivität bei makroskopischer Konstanz.
Zweistufige Protolyse
H2SO4 gibt in zwei Stufen je ein Proton ab. Im zweiten Schritt ist HSO4− eine schwächere Säure als H2SO4.
Siedepunkt 300 °C
Der hohe Siedepunkt von 300 °C erklärt sich durch starke zwischenmolekulare Kräfte (Wasserstoffbrücken und van-der-Waals-Kräfte).
Häufige Fragen – Schwefelsäure-Gleichgewicht
Was bedeutet „hygroskopisch" und warum ist konzentrierte Schwefelsäure so wassergierig?
Als hygroskopisch bezeichnet man Stoffe, die Wasser aus der Umgebungsluft aufnehmen. Konzentrierte H2SO4 reagiert heftig mit Wasser unter starker Wärmefreisetzung (Protolyse). Da diese Reaktion sehr exotherm ist, liegt das Gleichgewicht stark auf der Seite der Produkte – die Säure „zieht" Wassermoleküle regelrecht aus der Luft, bis sich ein dynamisches Gleichgewicht eingestellt hat.
Warum gibt verdünnte Schwefelsäure Wasser an die Luft ab, konzentrierte aber nicht?
Der entscheidende Faktor ist der Wasserdampfdruck der Lösung. Verdünnte Schwefelsäure hat einen höheren Wasserdampfdruck als die Umgebungsluft → H2O-Moleküle verdunsten. Konzentrierte H2SO4 hat dagegen einen sehr niedrigen Wasserdampfdruck → sie nimmt Wasser auf. Im Langzeitversuch gleichen sich beide Zylinder auf einen gemeinsamen Gleichgewichtszustand an. Mehr dazu auf der Seite Verschiebung des Gleichgewichts.
Was ist ein chemisches Gleichgewicht und woran erkennt man es?
Ein chemisches Gleichgewicht liegt vor, wenn Hin- und Rückreaktion gleich schnell ablaufen. Äußerlich scheint die Reaktion zum Stillstand gekommen zu sein (makroskopische Konstanz), auf molekularer Ebene laufen aber ständig beide Richtungen ab (dynamisches Gleichgewicht). Im Langzeitversuch erkennt man das Gleichgewicht daran, dass sich die Füllhöhen der Zylinder nicht mehr verändern. Weitere Merkmale findest du auf der Seite Merkmale eines chemischen Gleichgewichts.
Wie läuft die zweistufige Protolyse der Schwefelsäure mit Wasser ab?
H2SO4 ist eine zweiprotonige Säure und gibt ihre Protonen in zwei Schritten ab:
1. Stufe (vollständig):
H2SO4 + H2O → HSO4− + H3O+2. Stufe (unvollständig):
HSO4− + H2O ⇌ SO42− + H3O+Da HSO4− eine schwächere Säure ist, läuft die zweite Stufe nicht vollständig ab → daher enthält verdünnte Schwefelsäure sowohl SO42−- als auch HSO4−-Ionen. Die Grundlagen zur Protolyse hast du in der 9. Klasse kennengelernt: Bronsted-Definition (Kl. 9).
Warum darf man niemals Wasser zu konzentrierter Schwefelsäure geben?
Die Reaktion von konz. H2SO4 mit Wasser ist stark exotherm. Gibt man Wasser zu Säure, kann sich das Wasser an der Oberfläche spontan in Dampf verwandeln, was zu einem explosionsartigen Verspritzen der Säure führt. Richtig ist daher: immer Säure langsam in Wasser geben, nie umgekehrt! Die thermodynamischen Hintergründe (Reaktionsenthalpie) findest du in der Einheit Enthalpie H (Energetik).
Lernkarten – Schwefelsäure-Gleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeutet „hygroskopisch" und welcher bekannte Stoff zeigt diese Eigenschaft besonders stark?
Hygroskopisch = Wasser aus der Luft aufnehmend. Konzentrierte H2SO4 ist ein typisches Beispiel: Sie kann sogar organische Stoffe durch Wasserentzug verkohlen.
2Nenne die vier Teilchenarten, die in verdünnter Schwefelsäure vorhanden sind.
H3O+ (Oxonium-Ion) · HSO4− (Hydrogensulfat-Ion) · SO42− (Sulfat-Ion, wenig) · H2O (viele Wassermoleküle)
3Was passiert mit Zylinder 1 (konz. H2SO4) und Zylinder 2 (verd. H2SO4) im Langzeitversuch?
Zylinder 1 nimmt H2O auf → Füllstand steigt. Zylinder 2 gibt H2O ab → Füllstand sinkt. Nach Jahren: gleiche Konzentration → dynamisches Gleichgewicht.
4Schreibe die zweistufige Protolyse von H2SO4 mit Wasser auf.
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O ⇌ SO42− + H3O+
(Stufe 1 vollständig, Stufe 2 unvollständig)5Berechne die Stoffmenge H2SO4 in 100 ml konz. Schwefelsäure (ρ = 1,84 g/ml; w = 98 %; M = 98 g/mol).
m(Lösung) = 100 ml · 1,84 g/ml = 184 g
m(H2SO4) = 184 g · 0,98 = 180,3 g
n = 180,3 g ÷ 98 g/mol ≈ 1,84 molWeiter im Kapitel Gleichgewichtsreaktionen
← Calciumhydroxid-Gleichgewicht → Modellexperiment: Stechheberversuch
🔁 Verwandte Seiten: Merkmale eines chemischen Gleichgewichts · Prinzip von Le Chatelier · Brønsted-Definition (Kl. 9)
-
2.10 Verschiebung des Gleichgewichts
Was du auf dieser Seite lernst
Ein chemisches Gleichgewicht ist nicht unveränderlich: Konzentration, Temperatur und Druck können es verschieben. Du lernst an konkreten Beispielen – dem Eisenrhodanid-Gleichgewicht und dem Chlorethan-Versuch – wie und warum sich die Gleichgewichtslage ändert.
Grundlagen aus diesem Kapitel
Diese Seite baut auf den Grundlagen des chemischen Gleichgewichts auf: → Merkmale eines chemischen Gleichgewichts · → Kollisionsmodell · → Benzoesäure-Gleichgewicht
2.10 Verschiebung des Gleichgewichts
Die Lage des Gleichgewichts ergibt sich aus dem Zusammenwirken von Hinreaktion und Rückreaktion. Das Gleichgewicht verschiebt sich, wenn beide Reaktionen verschieden stark geändert werden.
Das ist häufig der Fall bei einer Änderung von
- Konzentration (Konzentration = Stoffmenge / Volumen)
- Temperatur
- Druck
2.10.1 Änderung der Konzentration und Temperatur
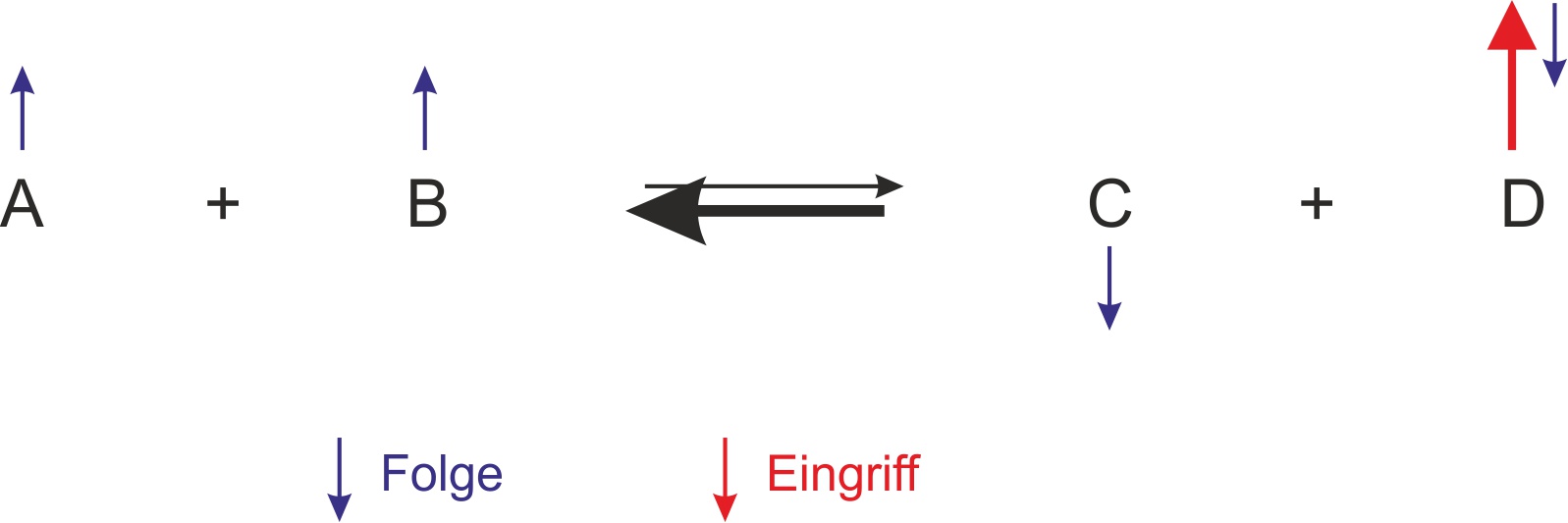
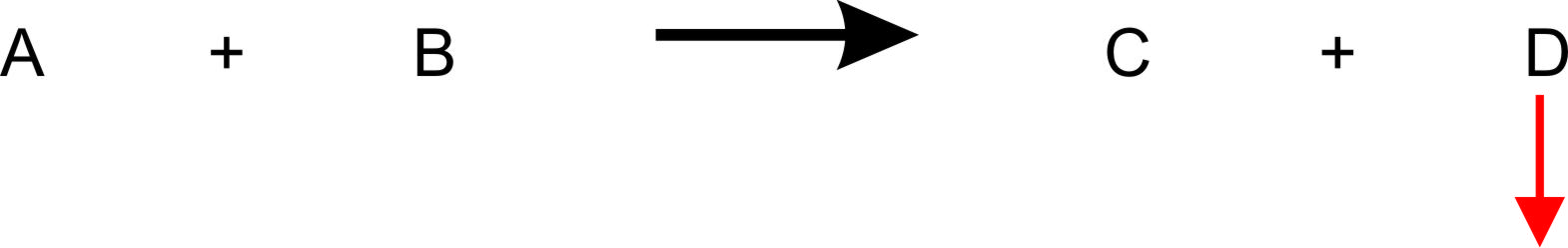
α) Einmaliger Zusatz von Stoff D
Es erfolgen mehr Rückreaktionen (Wichtig, das über das Kollisionsmodell zu verstehen: durch mehr Teilchen wird häufiger ein Zusammenstoß zwischen C und D erfolgen); dadurch stellt sich ein neues Gleichgewicht ein. Man sagt: „Das GG wird nach links verschoben."Roter Pfeil: Zugabe von Stoff D → Stoff D kollidiert häufiger mit C und reagiert. Dadurch werden es etwas weniger Stoffe C und D (blaue Pfeile auf der Produktseite); gleichzeitig entstehen etwas mehr Stoffe A und B. Bitte immer daran denken: Bei einem Gleichgewicht gibt es immer alle Stoffe – hier also A, B, C und D gleichzeitig! Man kann sich das schnell veranschaulichen, wenn man bei einer Reaktionsgleichung die Pfeile einzeichnet.
↑ Zum Vergrößern klicken
✕
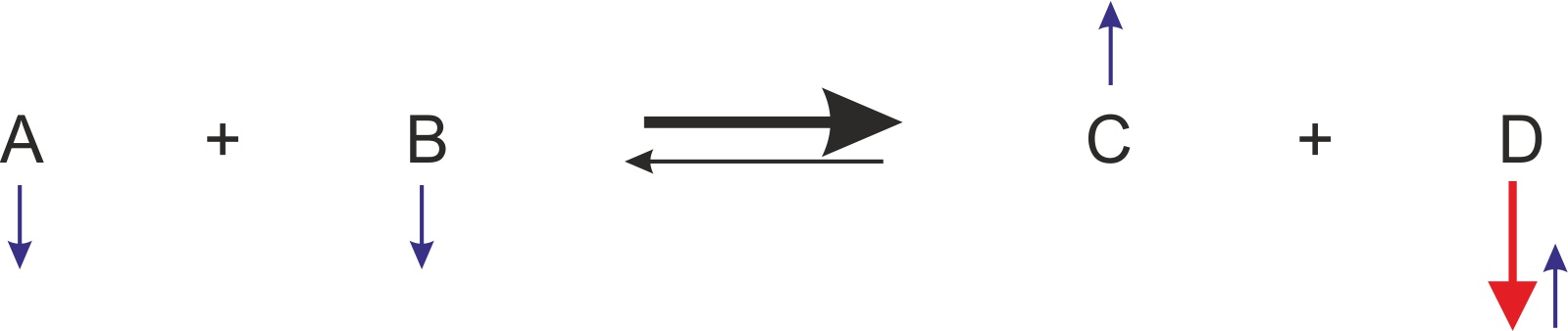
β) Einmalige Wegnahme von Stoff D
Jetzt seid ihr dran: Wie ändert sich das Gleichgewicht, wenn man einmalig den Stoff D wegnimmt? Macht eine analoge Reaktionsgleichung mit Pfeilen wie oben.
✕Lösung: Wegnahme von Stoff D
Es erfolgen mehr Hinreaktionen; dadurch stellt sich ein neues Gleichgewicht ein. Man sagt: „Das GG wird nach rechts verschoben."
↑ Zum Vergrößern klicken
γ) Dauernde Wegnahme von Stoff D (z. B. als Gas)
Wie ändert sich das Gleichgewicht bei dauerhafter Wegnahme, wenn der entstehende Stoff D permanent aus dem System verdampft?
✕Lösung: Dauernde Wegnahme – offenes System
In einem offenen System kann sich kein Gleichgewicht einstellen; die Reaktion läuft vollständig ab.
↑ Zum Vergrößern klicken
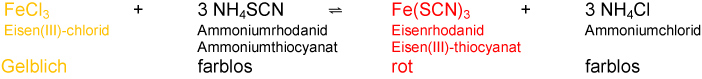
Eisenrhodanid-Gleichgewicht
Vergleich dazu Arbeitsblatt zum Experiment.
Vereinfachte Reaktionsgleichung:
↑ Zum Vergrößern klicken
✕
a) Das 1. Reagenzglas bleibt unverändert und dient zum Vergleich!
b) Ein Spatellöffel NH4Cl (Ammoniumchlorid) wird in Reagenzglas 2 gegeben.
Beobachtung: Die Lösung wird heller.Wie kann man das mithilfe der Verschiebung des Gleichgewichts deuten?
Lösung: Zugabe von NH₄Cl
Deutung: Das Gleichgewicht wird nach links verschoben. Die Konzentration des Produkts NH4Cl wird erhöht → mehr Rückreaktionen → weniger Fe(SCN)3 → Lösung entfärbt sich (wird heller).
c) Eine Spatelspitze FeCl3 (Eisenchlorid) wird in Reagenzglas 3 gegeben.
Nenne die mögliche Beobachtung und Deutung:
Lösung: Zugabe von FeCl₃
Beobachtung: Die Lösung wird dunkelrot.
Deutung: Das Gleichgewicht wird nach rechts verschoben. Die Konzentration des Edukts Fe3+ wird erhöht → mehr Hinreaktionen → mehr Fe(SCN)3 → Lösung wird dunkler.d) Ein Spatellöffel NH4SCN (Ammoniumrhodanid = Ammoniumthiocyanat) wird in Reagenzglas 4 gegeben.
Lösung: Zugabe von NH₄SCN
Beobachtung: Die Lösung wird dunkelrot.
Deutung: Das Gleichgewicht wird nach rechts verschoben. Die Konzentration des Edukts SCN− wird erhöht → mehr Hinreaktionen → mehr Fe(SCN)3.Ergebnis (Konzentration): Konzentrationserhöhung eines Reaktionspartners begünstigt die Reaktion, die diesen Stoff verbraucht.
e) Reagenzglas 5 wird in heißes Wasser gestellt.
Beobachtung: Die Lösung wird heller.
Lösung: Temperaturerhöhung (heißes Wasser)
Deutung: Das Gleichgewicht wird nach links verschoben. Temperaturerhöhung begünstigt die endotherme Reaktion (die Rückreaktion). Da ΔH < 0 für die Hinreaktion, ist die Rückreaktion endotherm → weniger Fe(SCN)3 → Lösung wird heller.
f) Reagenzglas 6 wird in Eiswasser gestellt.
Überlegt, was jetzt die Beobachtung sein könnte:
Lösung: Temperaturerniedrigung (Eiswasser)
Beobachtung: Die Lösung wird dunkler.
Deutung: Das Gleichgewicht wird nach rechts verschoben. Temperaturerniedrigung begünstigt die exotherme Reaktion (die Hinreaktion) → mehr Fe(SCN)3 → Lösung wird dunkler.Ergebnis (Temperatur):
• Temperaturerhöhung begünstigt die endotherme Reaktion.
• Temperaturerniedrigung begünstigt die exotherme Reaktion.b) Weiteres Beispiel
H2O (l) ⇌ H2O (g) ΔH = +41 kJ
flüssig gasförmigTemperaturerhöhung → mehr Wasser verdampft (endotherme Reaktion wird begünstigt).
2.10.2 Änderung des Drucks
a) Chlorethandampf – Chlorethanflüssigkeit (Kältespray; genau: Monochlorethan)
C2H5Cl (g) ⇌ C2H5Cl (l)
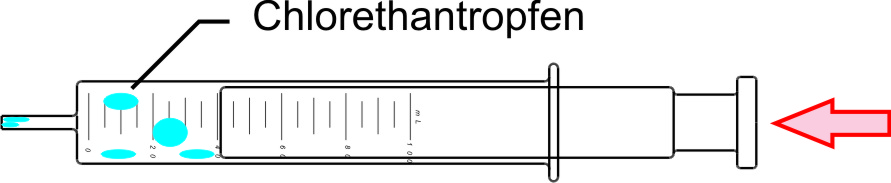
α) Bei Druckerhöhung bilden sich im Kolbenprober Chlorethantröpfchen:
↑ Zum Vergrößern klicken
✕
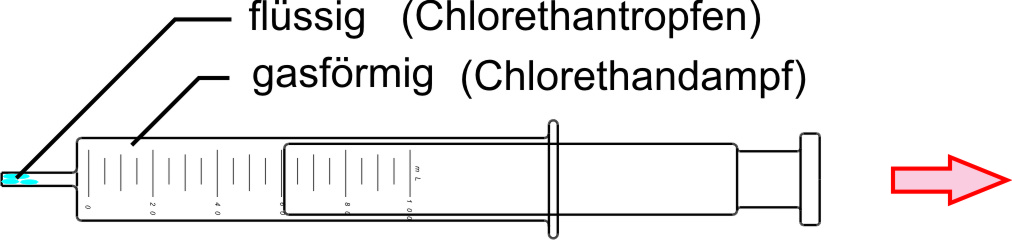
β) Bei Druckerniedrigung verschwinden die Chlorethantröpfchen wieder:
↑ Zum Vergrößern klicken
✕
Ergebnis (Druck): Druckerhöhung begünstigt die Reaktion mit Volumenabnahme.
b) Weiteres Beispiel
H2O (s) ⇌ H2O (l)
fest (solid) flüssig (liquid)Druckerhöhung verschiebt das Gleichgewicht nach rechts: Wasser wird flüssig.
Grund: Flüssiges Wasser hat eine größere Dichte (kleineres Volumen) als Eis – deshalb schwimmt Eis auf Wasser.FeCl3 + 3 NH4SCN ⇌ Fe(SCN)3 + 3 NH4Cl ΔH < 0
Auf einen Blick – die wichtigsten Aussagen
KONZENTRATION
Konzentrationserhöhung eines Stoffs begünstigt die Reaktion, die diesen Stoff verbraucht.
TEMPERATUR
Temperaturerhöhung begünstigt die endotherme, Kühlung die exotherme Reaktionsrichtung.
DRUCK
Druckerhöhung begünstigt die Reaktionsrichtung mit Volumenabnahme (weniger Gasteilchen).
OFFENES SYSTEM
Wird ein Produkt dauerhaft entfernt, kann sich kein Gleichgewicht einstellen – die Reaktion läuft vollständig ab.
Häufige Fragen – Verschiebung des Gleichgewichts
Was bedeutet es, dass ein Gleichgewicht „verschoben" wird?
Ein chemisches Gleichgewicht liegt vor, wenn Hin- und Rückreaktion gleich schnell ablaufen. Greift man von außen ein – z. B. durch Zugabe eines Stoffs – laufen beide Reaktionen vorübergehend unterschiedlich schnell. Bis sich ein neues Gleichgewicht einstellt, überwiegt eine der beiden Richtungen. Man sagt: Das Gleichgewicht wird nach links oder rechts verschoben. Mehr zu den Grundlagen: → Merkmale des chemischen Gleichgewichts.
Wie wirkt die Zugabe eines Reaktionspartners auf das Gleichgewicht?
Wird die Konzentration eines Stoffs erhöht, begünstigt das die Reaktionsrichtung, die diesen Stoff verbraucht. Erklärt wird das über das Kollisionsmodell: Mehr Teilchen bedeutet häufigere Zusammenstöße in der entsprechenden Reaktionsrichtung. Beispiel: Gibt man zum Eisenrhodanid-Gleichgewicht FeCl3 zu, steigt die Fe3+-Konzentration → das GG verschiebt sich nach rechts → Lösung wird dunkler.
Warum läuft eine Reaktion im offenen System vollständig ab?
Im offenen System werden Produkte permanent aus dem Reaktionsgemisch entfernt (z. B. durch Verdampfen). Dadurch kann die Rückreaktion nicht stattfinden – denn sie benötigt die Produkte als Edukte. Das Gleichgewicht wird so weit nach rechts verschoben, bis alle Edukte verbraucht sind. Dieses Prinzip ist z. B. in der Ammoniaksynthese technisch genutzt.
Warum verschiebt Erhitzen des Eisenrhodanid-Gleichgewichts die Lage nach links?
Die Hinreaktion des Eisenrhodanid-Gleichgewichts ist exotherm (ΔH < 0). Die Rückreaktion ist damit endotherm. Temperaturerhöhung begünstigt die endotherme Reaktionsrichtung – also die Rückreaktion. Infolgedessen zerfällt mehr Fe(SCN)3, und die rote Farbe verblasst. Umgekehrt: Kühlung (Eiswasser) begünstigt die exotherme Hinreaktion → Lösung wird dunkler.
Wie beeinflusst Druck ein Gleichgewicht zwischen Gasen?
Druckerhöhung begünstigt die Seite mit dem kleineren Volumen (weniger Gasteilchen). Beim Chlorethan-Gleichgewicht C2H5Cl (g) ⇌ C2H5Cl (l) bedeutet Druckerhöhung, dass mehr Dampf kondensiert (Flüssigkeit nimmt weniger Volumen ein). Bei Gasen mit unterschiedlicher Molzahl auf beiden Seiten (z. B. der Ammoniaksynthese: N2 + 3 H2 ⇌ 2 NH3) begünstigt Druck die Seite mit weniger Gasteilchen (hier die Produktseite mit 2 mol statt 4 mol).
Lernkarten – Verschiebung des Gleichgewichts
Klicke auf eine Karte, um die Antwort zu sehen.
1Was passiert beim einmaligen Zusatz von Stoff D zum Gleichgewicht A + B ⇌ C + D?
Das GG verschiebt sich nach links: Mehr Kollisionen zwischen C und D führen zu mehr Rückreaktionen. A und B nehmen zu, C und D (abzüglich Zugabe) nehmen ab.
2Was passiert, wenn ein Produkt im offenen System dauerhaft entfernt wird?
Die Rückreaktion kann nicht mehr stattfinden. Das GG wird so weit nach rechts verschoben, bis alle Edukte verbraucht sind – die Reaktion läuft vollständig ab.
3Das Eisenrhodanid-GG (ΔH < 0). Was beobachtet man beim Erwärmen – und warum?
Lösung wird heller: Temperaturerhöhung begünstigt die endotherme Rückreaktion → GG verschiebt sich nach links → weniger Fe(SCN)3.
4Was beobachtet man beim Druckerhöhen im Chlorethan-Kolbenprober – und warum?
Es entstehen Chlorethantröpfchen: Druckerhöhung begünstigt die Reaktionsrichtung mit Volumenabnahme → Gas kondensiert zu Flüssigkeit.
5Zusammenfassung: Nenne alle Maßnahmen, die das exotherme Eisenrhodanid-GG nach rechts verschieben, und erkläre jeweils warum.
① Fe³⁺ oder SCN⁻ zugeben (Edukt-Konzentration ↑) · ② NH₄Cl entfernen (Produkt-Konzentration ↓) · ③ Abkühlen (exotherme Hinreaktion wird begünstigt) – in allen Fällen: mehr Fe(SCN)3, Lösung wird dunkler.
Weiter im Kapitel Gleichgewichtsreaktionen
← 2.9 Benzoesäure-Gleichgewicht → 2.11 Prinzip von Le Chatelier
→ 2.12 Massenwirkungsgesetz → 2.15 Ammoniaksynthese
🔁 Grundlagen: Merkmale des chemischen GG · Kollisionsmodell
-
2.3 Modellexperiment - Stechheberversuch
Was du auf dieser Seite lernst
Der Stechheberversuch ist ein mechanisches Modell für chemische Gleichgewichte. Du erkennst, warum Hin- und Rückreaktion gleichzeitig ablaufen, warum beide Startbedingungen zum selben Gleichgewichtszustand führen – und wie sich das in Diagrammen zeigt.
Grundlagen aus diesem Kapitel
Den Begriff der umkehrbaren Reaktion hast du auf der vorherigen Seite kennengelernt: → Umkehrbare Reaktionen
2.3 Modellexperiment – Stechheberversuch
Vergleiche dazu auch das ausgeteilte Arbeitsblatt zum Experiment.
↑ Zum Vergrößern klicken
✕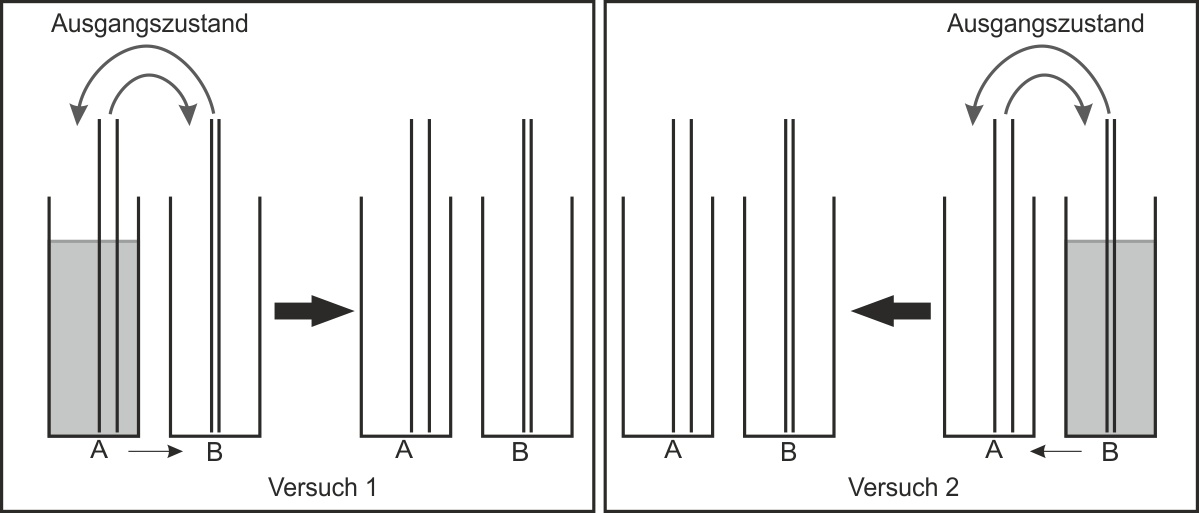
Versuch 1: Flüssigkeit gelangt von A nach B. Die reversible Reaktion setzt mit der „Hinreaktion" ein. Anschließend gelangt auch Flüssigkeit von B zurück nach A – es findet also auch eine „Rückreaktion" statt. Nach einiger Zeit sind die in den Rohren im gleichen Takt beförderten Flüssigkeitsportionen gleich groß geworden.
Wie könnten die Endzustände bei den Experimenten 1 und 2 aussehen?
✕Lösung: Endzustand Versuch 1 und 2
Versuch 1 und Versuch 2 führen zum gleichen Ergebnis – dem Gleichgewichtszustand. Unabhängig von der Startbedingung (ob die Flüssigkeit zunächst in A oder in B ist) stellt sich dieselbe Gleichgewichtsverteilung ein:
↑ Zum Vergrößern klicken
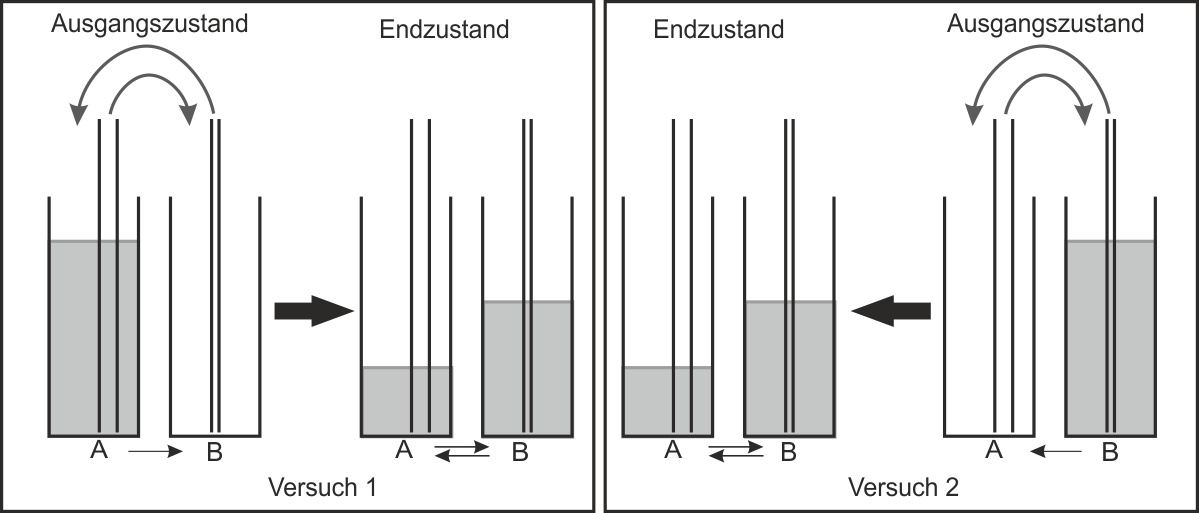
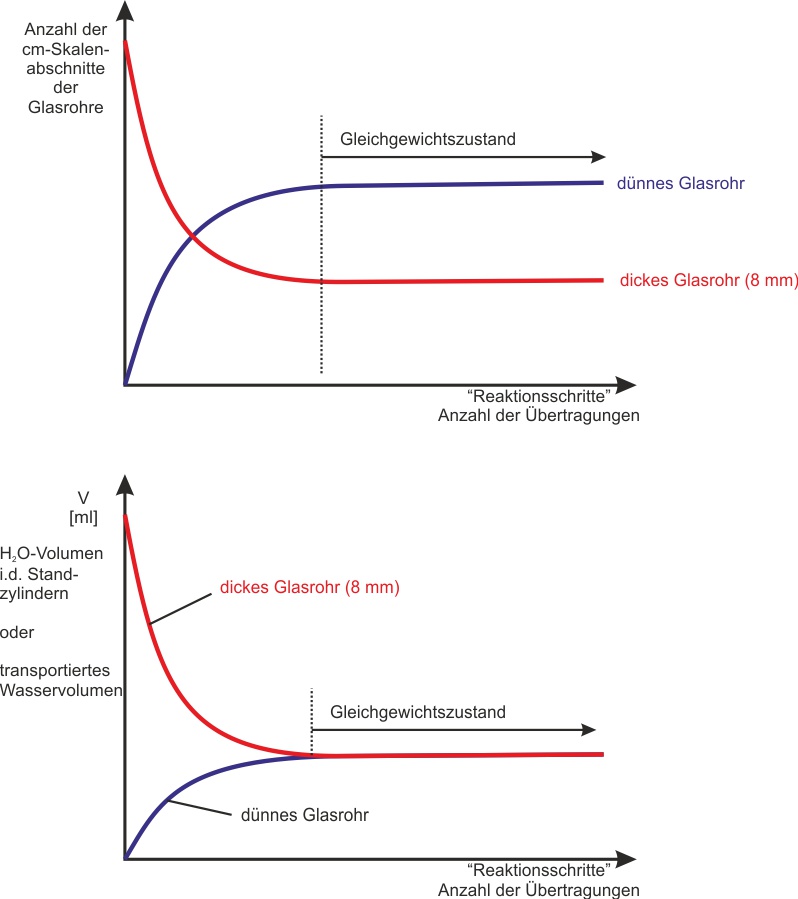
Was für ein Diagramm bekommt man, wenn man das Volumen in den Standzylindern gegen die Anzahl der Übertragungen aufträgt? Und wie sieht das Diagramm aus, wenn man das transportierte Volumen innerhalb der Glasrohre gegen die Zeit aufträgt?
✕
Auf einen Blick – die wichtigsten Aussagen
Gleiches Ergebnis
Versuch 1 und Versuch 2 führen zum selben Gleichgewichtszustand – unabhängig davon, von welcher Seite der Prozess startet.
Dynamisch
Im Gleichgewicht fließt noch immer Flüssigkeit in beide Richtungen – nur die transportierten Portionen sind gleich groß. Äußerlich: Stillstand. Innerlich: Aktivität.
Diagrammform
Die Kurven nähern sich asymptotisch einem konstanten Wert. Das gilt für das Volumen in den Zylindern ebenso wie für das transportierte Volumen in den Rohren.
Modellcharakter
Der Versuch ist eine mechanische Analogie. Die „Rohrdurchmesser" entsprechen den unterschiedlichen Reaktionsgeschwindigkeiten von Hin- und Rückreaktion.
Häufige Fragen – Stechheberversuch
Was zeigt der Stechheberversuch über chemische Gleichgewichte?
Der Stechheberversuch ist ein Modellexperiment: Zwei Standzylinder (A und B) sind über Glasrohre verbunden. Flüssigkeit wird abwechselnd von A nach B und von B nach A transportiert – analog zu Hin- und Rückreaktion. Nach einigen Schritten sind die transportierten Portionen gleich groß: Das Modell hat das dynamische Gleichgewicht erreicht. Die eigentlichen Merkmale eines chemischen Gleichgewichts findest du auf der Seite Merkmale eines chemischen Gleichgewichts.
Warum führen Versuch 1 und Versuch 2 zum gleichen Endzustand?
In Versuch 1 ist zu Beginn alles in A, in Versuch 2 alles in B. Trotzdem endet beides in derselben Gleichgewichtsverteilung. Das zeigt ein zentrales Merkmal chemischer Gleichgewichte: Der Gleichgewichtszustand ist unabhängig vom Startpunkt – er hängt nur von den Reaktionsbedingungen (Temperatur, Konzentration) ab, nicht davon, von welcher Seite man startet.
Was bedeutet „dynamisch" beim Gleichgewicht – ist da wirklich noch etwas in Bewegung?
Ja! Im Gleichgewicht hört der Transport nicht auf. Pro Schritt fließt weiterhin Flüssigkeit von A nach B und von B nach A – nur die Mengen sind gleich groß. Makroskopisch sieht es aus wie Stillstand (die Füllhöhen ändern sich nicht mehr), mikroskopisch ist das System aktiv. Deshalb: dynamisches Gleichgewicht, nicht statisches. Dasselbe Prinzip gilt für chemische Reaktionen: Hin- und Rückreaktion laufen gleichzeitig mit gleicher Geschwindigkeit ab.
Was zeigen die zwei Diagramme des Stechheberversuchs?
Diagramm 1 (oben): Anzahl der gefüllten cm-Skalenabschnitte in den Glasrohren. Das dünne Rohr (langsamere Reaktionsrichtung) startet niedrig und steigt; das dicke Rohr (schnellere Richtung) startet hoch und fällt. Beide Kurven nähern sich asymptotisch einem gemeinsamen Plateau – dem Gleichgewichtszustand.
Diagramm 2 (unten): Das transportierte Volumen pro Schritt. Das dicke Rohr transportiert anfangs viel, das dünne wenig. Im Gleichgewicht transportieren beide pro Schritt gleich viel – die Kurven treffen sich.
Welche Grenzen hat der Stechheberversuch als Modell für chemische Gleichgewichte?
Jedes Modell hat Grenzen. Beim Stechheberversuch sind das vor allem: Die Rohrdurchmesser sind fest – in echten Reaktionen können die Reaktionsgeschwindigkeiten durch Konzentration, Temperatur oder Katalysatoren verändert werden (siehe Prinzip von Le Chatelier). Außerdem ist der Stechheberversuch diskret (schrittweise), während chemische Reaktionen kontinuierlich ablaufen. Das Modell eignet sich gut zur Veranschaulichung des dynamischen Gleichgewichts, nicht aber zur quantitativen Beschreibung.
Lernkarten – Stechheberversuch
Klicke auf eine Karte, um die Antwort zu sehen.
1Wofür stehen im Stechheberversuch: die Standzylinder, die Glasrohre und der Flüssigkeitstransport?
Standzylinder A/B → Edukt- und Produktseite · Glasrohre → Reaktionswege (Hin- / Rückreaktion) · Flüssigkeitstransport → Stoffumsatz pro Zeiteinheit
2Warum führen Versuch 1 (Start: alles in A) und Versuch 2 (Start: alles in B) zum gleichen Gleichgewicht?
Der Gleichgewichtszustand hängt nur von den Bedingungen (Rohrdurchmesser = Geschwindigkeit) ab, nicht vom Startpunkt. Das gilt ebenso für chemische Gleichgewichte.
3Erkläre: Im Gleichgewicht des Stechheberversuchs bewegen sich die Füllhöhen nicht mehr – und trotzdem ist das Gleichgewicht „dynamisch". Wie passt das zusammen?
Makroskopisch: Füllhöhen konstant. Mikroskopisch: Flüssigkeit fließt weiterhin in beide Richtungen, aber in gleich großen Portionen. → dynamisch = gleichzeitig aktiv in beide Richtungen.
4Beschreibe die Form der Kurven im Diagramm „transportiertes Volumen gegen Reaktionsschritte".
Dickes Rohr: startet hoch, fällt exponentiell. Dünnes Rohr: startet niedrig, steigt. Beide nähern sich asymptotisch einem gemeinsamen Wert → Gleichgewichtszustand.
5Im GG-Zustand transportiert das dünne Rohr pro Schritt 2 ml. Das dicke Rohr hat doppelten Durchmesser. Wie viel ml transportiert es pro Schritt und wie viel insgesamt in 10 Schritten?
Im GG gilt: Transport Hin = Transport Rück. Dickes Rohr transportiert ebenfalls 2 ml pro Schritt. In 10 Schritten: 10 · 2 ml = 20 ml in jede Richtung.
Weiter im Kapitel Gleichgewichtsreaktionen
← Schwefelsäure-Gleichgewicht → Merkmale eines chemischen Gleichgewichts
🔁 Verwandte Seiten: Umkehrbare Reaktionen · Prinzip von Le Chatelier · Massenwirkungsgesetz
-
2.4 Merkmale eines chemischen Gleichgewichts
Was du auf dieser Seite lernst
Du lernst die drei zentralen Merkmale eines chemischen Gleichgewichts kennen und wiederholst den Systembegriff (offen / geschlossen / abgeschlossen). Diese Grundlagen brauchst du für alle weiteren Themen rund um Gleichgewichtsreaktionen.
Grundlagen aus diesem Kapitel
Das dynamische Gleichgewicht hast du am Modell des Stechheberversuchs kennengelernt: → Modellexperiment Stechheberversuch · Den Systembegriff aus der Energetik: → Thermodynamische Systeme (Energetik)
2.4 Merkmale eines chemischen Gleichgewichts
⚑ Merksatz – Chemisches Gleichgewicht
- Im abgeschlossenen System stellt sich das Gleichgewicht von beiden Seiten her ein.
- Im Gleichgewicht (Endzustand) erfolgen gleich viele Hin- wie Rückreaktionen pro Zeiteinheit.
- Im Gleichgewicht liegen meist nicht gleich viele Anfangs- wie Endstoffe vor.
Wiederholung: Systemtypen in der Chemie
Offenes System Geschlossenes System Abgeschlossenes System
(= isoliertes System)Austausch von … ✔ Energie
✔ Teilchen✔ Energie — Kein Austausch von … — ✘ Teilchen ✘ Energie
✘ TeilchenBesonderheit Gesamtenergie konstant
i. d. R. idealisiertes SystemBeispiele „Kochtopf"
Mensch„Dampfkochtopf"
Reagenzglas mit Stopfen„Thermoskanne"
Universum (idealisiert)ℹ Den Systembegriff aus der Perspektive der Thermodynamik findest du hier: Thermodynamische Systeme (Energetik)
Auf einen Blick – die wichtigsten Aussagen
Merkmal 1 – Startpunkt
Das Gleichgewicht stellt sich von beiden Seiten her ein – ob man mit Edukten, Produkten oder einem Gemisch startet, spielt keine Rolle.
Merkmal 2 – Dynamik
Im Gleichgewicht laufen Hin- und Rückreaktion mit gleicher Geschwindigkeit ab. Äußerlich: Stillstand. Innerlich: ständige Aktivität.
Merkmal 3 – Stoffmengen
Edukte und Produkte liegen im GG meist in ungleichen Mengen vor. Das Verhältnis beschreibt die Gleichgewichtskonstante Kc.
Voraussetzung
Ein stabiles Gleichgewicht kann sich nur in einem abgeschlossenen oder geschlossenen System einstellen – Teilchen dürfen nicht entweichen.
Häufige Fragen – Merkmale des chemischen Gleichgewichts
Was sind die drei wichtigsten Merkmale eines chemischen Gleichgewichts?
Ein chemisches Gleichgewicht ist durch drei Merkmale gekennzeichnet: (1) Es stellt sich von beiden Seiten ein – unabhängig vom Startpunkt. (2) Hin- und Rückreaktion laufen im Gleichgewicht gleich schnell ab (dynamisches Gleichgewicht). (3) Die Konzentrationen von Edukten und Produkten sind im Gleichgewicht konstant, aber i. d. R. verschieden.
Was bedeutet „das Gleichgewicht stellt sich von beiden Seiten ein"?
Ganz gleich, ob man mit reinen Edukten, reinen Produkten oder einem beliebigen Gemisch startet – das System strebt immer denselben Gleichgewichtszustand an (bei gleichen Bedingungen). Das zeigt der Stechheberversuch modellhaft: Versuch 1 (Start: alles in A) und Versuch 2 (Start: alles in B) enden im selben Endzustand.
Sind im Gleichgewicht immer gleich viele Edukte wie Produkte vorhanden?
Nein – das ist ein häufiges Missverständnis. Im Gleichgewicht sind die Konzentrationen konstant, aber nicht notwendigerweise gleich groß. Wie das Verhältnis aussieht, beschreibt die Gleichgewichtskonstante Kc. Liegt Kc ≫ 1, überwiegen die Produkte; liegt Kc ≪ 1, überwiegen die Edukte.
Warum braucht man ein abgeschlossenes (oder geschlossenes) System für ein Gleichgewicht?
Wenn Teilchen das System verlassen können (offenes System), kann sich kein stabiles Gleichgewicht einstellen – z. B. entweicht CO2 beim Erhitzen von CaCO3 im offenen Reagenzglas, und die Rückreaktion findet praktisch nicht statt. Im geschlossenen System (Stopfen drauf) bleibt das CO2 im System, die Rückreaktion läuft ab, und es stellt sich ein Gleichgewicht ein.
Was ist der Unterschied zwischen offenem, geschlossenem und abgeschlossenem System?
Offenes System: Austausch von Energie und Teilchen mit der Umgebung (z. B. Kochtopf ohne Deckel, lebender Organismus). Geschlossenes System: Nur Energieaustausch, keine Teilchen (z. B. Reagenzglas mit Stopfen, Dampfkochtopf). Abgeschlossenes System: Weder Energie- noch Teilchenaustausch (Thermoskanne, Universum – idealisiert). Alle drei Typen sind detailliert auf der Seite Thermodynamische Systeme (Energetik) beschrieben.
Lernkarten – Merkmale des chemischen Gleichgewichts
Klicke auf eine Karte, um die Antwort zu sehen.
1Nenne die drei Merkmale eines chemischen Gleichgewichts.
① Stellt sich von beiden Seiten ein · ② Hin- = Rückreaktion pro Zeiteinheit (dynamisch) · ③ Meist ungleiche Mengen von Edukten und Produkten
2Warum ist ein chemisches Gleichgewicht „dynamisch" und nicht „statisch"?
Weil Hin- und Rückreaktion weiterhin ablaufen – nur mit gleicher Geschwindigkeit. Makroskopisch: Konzentrationen konstant. Mikroskopisch: ständige Reaktionsaktivität.
3Ordne zu: Kochtopf (offen) · Reagenzglas mit Stopfen · Thermoskanne → welcher Systemtyp?
Kochtopf ohne Deckel → offenes System · Reagenzglas mit Stopfen → geschlossenes System · Thermoskanne → abgeschlossenes System
4Stimmt es, dass im GG immer [Edukt] = [Produkt] gilt? Begründe.
Nein. Im GG sind die Konzentrationen konstant, aber nicht notwendigerweise gleich. Das Verhältnis hängt von Kc ab: Kc ≫ 1 → Produkte überwiegen; Kc ≪ 1 → Edukte überwiegen.
5Für A ⇌ B gilt Kc = 4. Im Gleichgewicht beträgt [A] = 0,5 mol/L. Berechne [B].
Kc = [B] / [A]
[B] = Kc · [A]
[B] = 4 · 0,5 mol/L
[B] = 2,0 mol/LWeiter im Kapitel Gleichgewichtsreaktionen
← Stechheberversuch → Estergleichgewicht
🔁 Verwandte Seiten: Prinzip von Le Chatelier · Massenwirkungsgesetz · Thermodynamische Systeme (Energetik)
-
2.5 Estergleichgewicht
Was du auf dieser Seite lernst
Du lernst, wie Carbonsäuren und Alkohole in einer Kondensationsreaktion zu Estern und Wasser reagieren. Am Beispiel des Estergleichgewichts (Essigsäure + Ethanol) wird deutlich, dass sowohl Hin- als auch Rückreaktion zum gleichen Endzustand führen – ein klassisches Beispiel für ein chemisches Gleichgewicht.
Grundlagen aus der 10. Klasse
Die Grundlagen zu Carbonsäuren und Alkoholen hast du bereits in der 10. Klasse kennengelernt:
→ Essigsäure / Ethansäure (Kl. 10) · → Alkohole / Alkanole (Kl. 10)2.5 Estergleichgewicht
Allgemeine Reaktion
Carbonsäure + Alkohol ⇌ Ester + Wasser
Wer sich an die 10. Klasse erinnern kann, kann ja mal versuchen, die Reaktionsgleichung für Ethansäure und Ethanol zu formulieren.
Tipp 1: Es handelt sich um eine Kondensationsreaktion – zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (hier: Wasser).
Tipp 2: Es reagieren meist die funktionellen Gruppen miteinander und selten die Alkylgruppen.
Allgemeine Reaktionsgleichung (Summenformeln)
R–COOH + R'–OH ⇌ R–COO–R' + H2O
Carbonsäure + Alkohol ⇌ Ester + Wasser | Katalysator: H+ (z. B. konz. H2SO4)
✕Lösung: Reaktionsgleichung Ethansäure + Ethanol
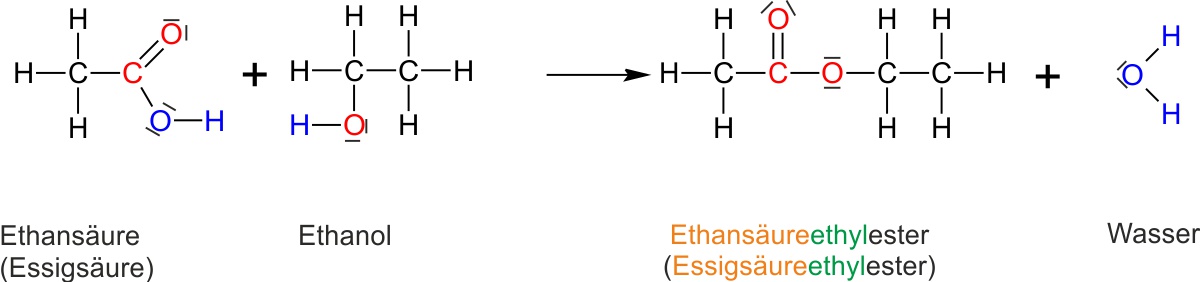
Mechanismus der Veresterung (säurekatalysiert)
Der Mechanismus der säurekatalysierten Veresterung verläuft in vier reversiblen Teilschritten. Der Katalysator (H+) wird am Ende wieder freigesetzt:
↑ Zum Vergrößern klicken
✕Die 4 Teilschritte in Kurzform
1. Protonierung der Carbonylfunktion der Carbonsäure → Carbokation
2. Nukleophiler Angriff des Alkohols (freies Elektronenpaar) → Oxoniumion
3. Protonenumlagerung → Wasserabspaltung → erneutes Carbokation
4. Protonenabspaltung (H+ wird regeneriert) → CarbonsäureesterAlle Teilschritte sind reversibel (⇌). Der H+-Katalysator beschleunigt die Reaktion, verschiebt aber das Gleichgewicht nicht.
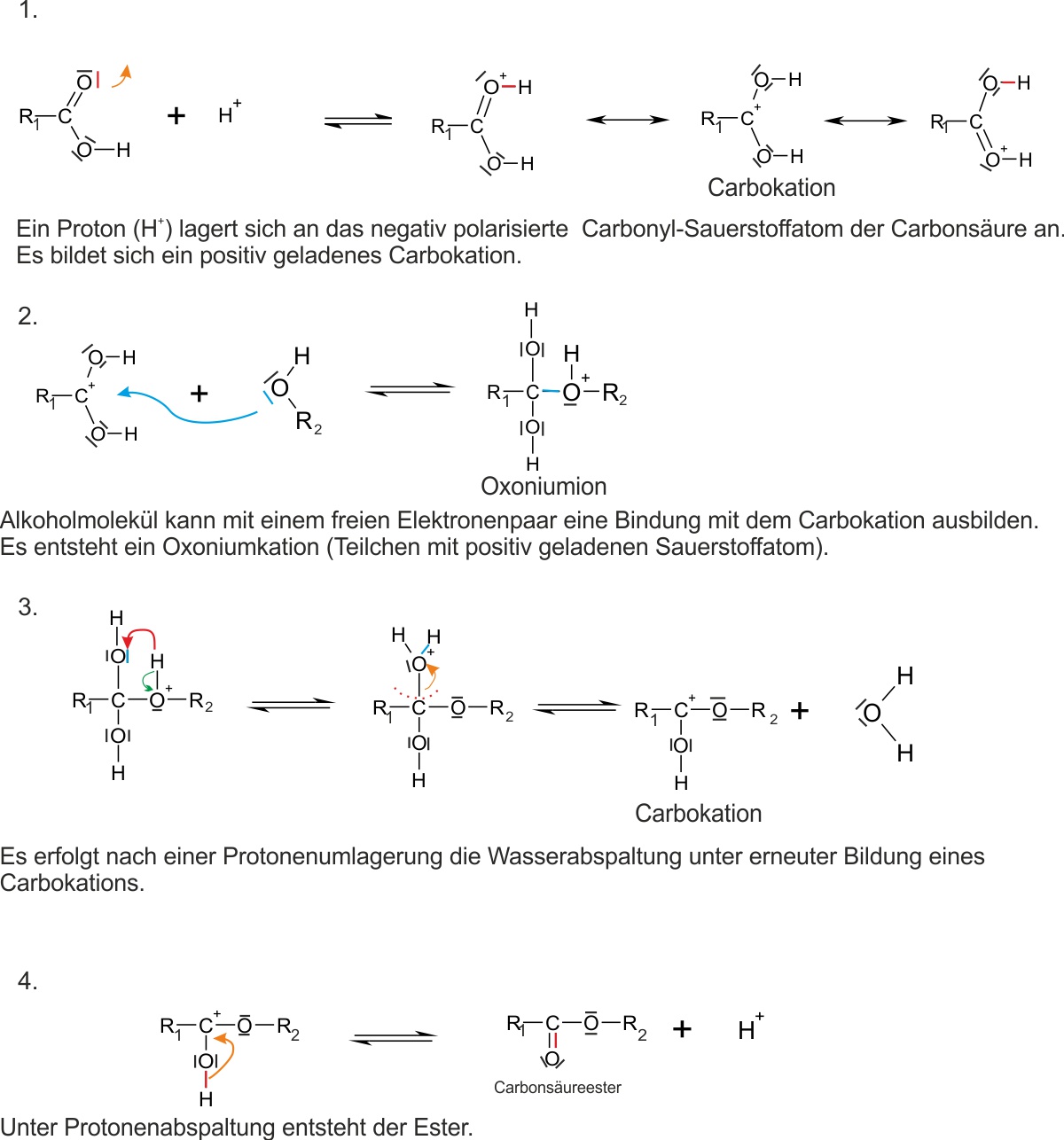
Das Estergleichgewicht – Nachweis durch zwei Versuchsansätze
Versuchsansatz 1 (Hinreaktion): Man gibt 1 mol Carbonsäure und 1 mol Alkohol zusammen.
Versuchsansatz 2 (Rückreaktion): Man gibt 1 mol Ester und 1 mol Wasser zusammen.Tipp: Was erwartest du?
Schau dir nochmals die Merkmale eines chemischen Gleichgewichts an. Ein echtes Gleichgewicht wird vom gleichen Endzustand aus erreicht – egal von welcher Seite man startet.
✕Lösung: Ergebnis des Experiments
Ergebnis: Man erhält in beiden Fällen denselben Endzustand.
↑ Zum Vergrößern klicken
Reaktionsgleichung und Mengenverhältnisse im Gleichgewicht
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
Zeitpunkt n(CH3COOH) n(C2H5OH) n(Ester) n(H2O) Anfang 1 (Hinreaktion) 1 mol 1 mol 0 mol 0 mol Gleichgewicht ⅓ mol ⅓ mol ⅔ mol ⅔ mol Anfang 2 (Rückreaktion) 0 mol 0 mol 1 mol 1 mol 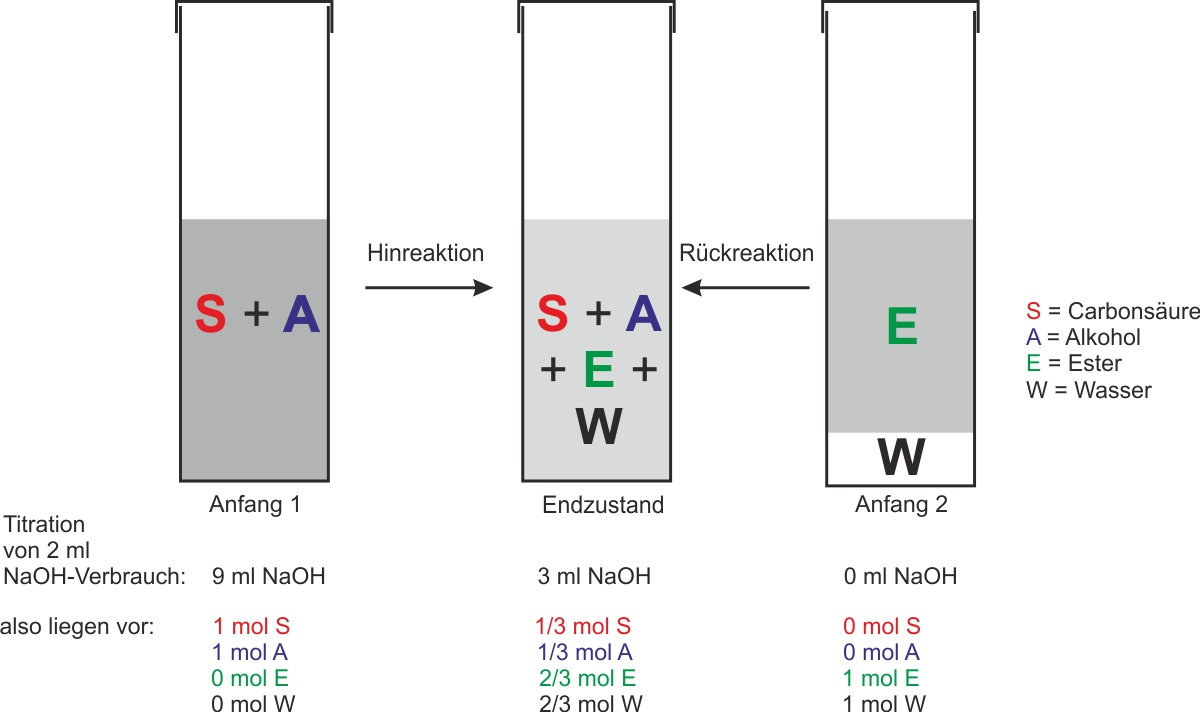
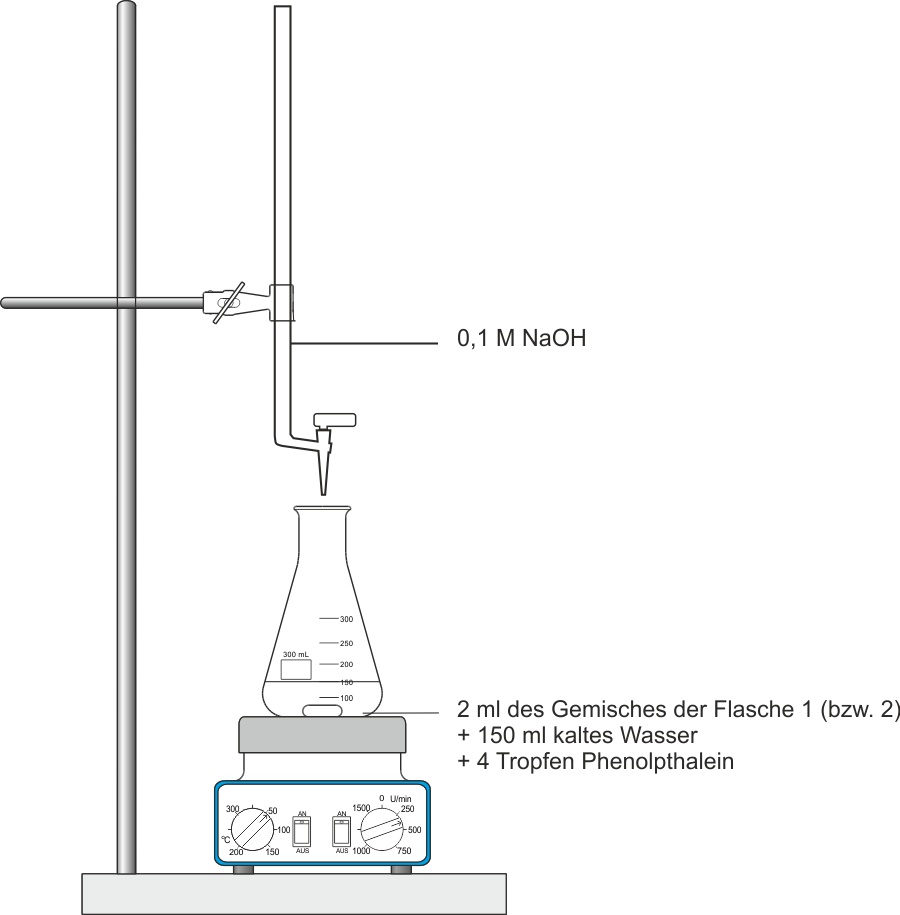
Quantitativer Nachweis: Titration der Carbonsäure
Man kann in beiden Versuchsansätzen die vorhandene Carbonsäuremenge durch quantitative Reaktion mit Natronlauge (Titration) messen.
Reaktionsgleichung der Titration (Summenformeln)
CH3COOH + NaOH → CH3COONa + H2O
Essigsäure reagiert vollständig und quantitativ mit NaOH. Mit 0,1 M NaOH und dem Verbrauch kann die Säuremenge berechnet werden: n(CH3COOH) = c(NaOH) · V(NaOH)
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
KONDENSATIONSREAKTION
Bei der Veresterung verbinden sich Carbonsäure und Alkohol unter Abspaltung von Wasser – typische Kondensationsreaktion.
MECHANISMUS
4 reversible Schritte: Protonierung → Carbokation → Oxoniumion → Wasserabspaltung → Ester. H+ ist Katalysator.
GLEICHGEWICHT
Hin- und Rückreaktion erreichen denselben Endzustand: ⅔ mol Ester + ⅔ mol Wasser (aus je 1 mol Edukt).
TITRATION
Der Gleichgewichtszustand lässt sich quantitativ nachweisen: Die Carbonsäuremenge wird durch Titration mit NaOH bestimmt.
Häufige Fragen – Estergleichgewicht
Was ist eine Kondensationsreaktion und warum ist die Veresterung eine solche?
Bei einer Kondensationsreaktion verbinden sich zwei Moleküle unter Abspaltung eines kleinen Moleküls – hier Wasser. Bei der Veresterung reagiert die Carboxylgruppe (–COOH) der Carbonsäure mit der Hydroxylgruppe (–OH) des Alkohols: Beide funktionellen Gruppen treten miteinander in Wechselwirkung, und als Nebenprodukt entsteht ein Wassermolekül. Mehr zur Carboxylgruppe findest du auf der Seite Funktionelle Gruppe der Monocarbonsäuren (Kl. 10).
Wie läuft der Mechanismus der säurekatalysierten Veresterung ab?
Der Mechanismus verläuft in vier reversiblen Schritten: (1) Ein Proton (H+) lagert sich an das Carbonyl-Sauerstoffatom der Carbonsäure – es entsteht ein Carbokation. (2) Ein freies Elektronenpaar des Alkohols greift das Carbokation an – es bildet sich ein Oxoniumkation. (3) Nach einer Protonenumlagerung wird Wasser abgespalten und erneut ein Carbokation gebildet. (4) Durch Protonenabspaltung entsteht der fertige Ester, und H+ wird regeneriert.
Warum führen Hin- und Rückreaktion zum gleichen Endzustand?
Weil es sich um ein echtes chemisches Gleichgewicht handelt. Das Gleichgewicht wird dynamisch erreicht: Hin- und Rückreaktion laufen gleichzeitig ab, bis ihre Geschwindigkeiten gleich groß sind. Egal ob man mit 1 mol Carbonsäure + 1 mol Alkohol (Hinreaktion) oder mit 1 mol Ester + 1 mol Wasser (Rückreaktion) startet – der Endzustand ist identisch: ca. ⅔ mol Ester und ⅔ mol Wasser liegen neben ⅓ mol Carbonsäure und ⅓ mol Alkohol vor. Mehr zu den Merkmalen eines Gleichgewichts: Merkmale eines chemischen Gleichgewichts.
Wie kann man das Estergleichgewicht zugunsten des Esters verschieben?
Nach dem Prinzip von Le Chatelier kann das Gleichgewicht verschoben werden, indem man:
• einen der Reaktionspartner im Überschuss einsetzt (z. B. mehr Alkohol),
• ein Produkt laufend entzieht (z. B. Wasser durch Destillation oder mit einem Trockenmittel entfernt).
Hinweis: Ein Katalysator (konz. H2SO4) beschleunigt lediglich die Gleichgewichtseinstellung – er verschiebt das Gleichgewicht nicht.
Mehr dazu: Prinzip von Le Chatelier.Wie wird das Estergleichgewicht experimentell nachgewiesen?
Man misst quantitativ die verbliebene Carbonsäuremenge durch Titration mit Natronlauge (NaOH) und dem Indikator Phenolphthalein. Aus dem NaOH-Verbrauch lässt sich n(Carbonsäure) berechnen: n = c(NaOH) · V(NaOH). Beim Gleichgewichtsansatz verbraucht man nur noch ⅓ des ursprünglichen NaOH-Verbrauchs, was zeigt, dass ⅔ der Essigsäure abreagiert haben. Mehr zur Säure-Base-Titration: Säure-Base-Titration (Kursstufe).
Lernkarten – Estergleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Kondensationsreaktion? Nenne ein Beispiel.
Zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (z. B. H2O). Beispiel: Veresterung – Carbonsäure + Alkohol → Ester + Wasser.
2Welche Zwischenstufen entstehen im Mechanismus der säurekatalysierten Veresterung?
1. Carbokation (nach Protonierung der Carbonsäure)
2. Oxoniumkation (nach Angriff des Alkohols)
3. erneutes Carbokation (nach Wasserabspaltung)
→ Ester + H+ (regeneriert)3Was beweist das Estergleichgewicht-Experiment mit zwei Ansätzen?
Beide Ansätze (1 mol S + 1 mol A bzw. 1 mol E + 1 mol W) führen zum gleichen Endzustand – Beweis für ein echtes dynamisches Gleichgewicht.
4Nenne zwei Maßnahmen, um das Estergleichgewicht auf die Esterseite zu verschieben.
1. Überschuss eines Reaktionspartners (z. B. mehr Alkohol)
2. Entzug eines Produkts (z. B. Wasser abdestillieren oder binden)
→ Prinzip von Le Chatelier
Nicht geeignet: Katalysator – beschleunigt nur, verschiebt nicht.5Beim GG-Ansatz (1 mol CH3COOH + 1 mol C2H5OH) verbraucht die Titration von 2 ml Probe 3 ml NaOH (0,1 M). Wie viel mol Essigsäure sind noch vorhanden, wenn der Gesamtansatz 50 ml beträgt?
n(NaOH) pro 2 ml Probe = 0,003 l · 0,1 mol/l = 3·10−4 mol
→ Hochrechnung auf 50 ml: n(CH3COOH) = 3·10−4 · 25 = 7,5·10−3 mol ≈ ⅓ der Ausgangsmenge (erwartet: ⅓ mol)Weiter im Kapitel Gleichgewichtsreaktionen
← Merkmale eines chemischen Gleichgewichts → Schreibweise und Kollisionsmodell
🔁 Grundlagen aus Klasse 10: Essigsäure / Ethansäure (Kl. 10) · Alkohole / Alkanole (Kl. 10) · Funktionelle Gruppe der Monocarbonsäuren (Kl. 10)
⬇️ Weiter im Kapitel: Prinzip von Le Chatelier · Massenwirkungsgesetz · Ammoniaksynthese
-
2.6 Schreibweise und 2.7 Kollisionsmodell
Was du auf dieser Seite lernst
Du lernst, wie man die Lage eines Gleichgewichts mit verschieden langen Pfeilen sichtbar macht. Das Kollisionsmodell erklärt, warum die Reaktionsgeschwindigkeit vom Produkt der Konzentrationen abhängt – und warum ein Katalysator zwar schneller zum Gleichgewicht führt, es aber nicht verschiebt.
Grundlagen aus diesem Kapitel
Die Merkmale des dynamischen Gleichgewichts: → Merkmale eines chemischen Gleichgewichts · Konkret am Beispiel des Estergleichgewichts: → Estergleichgewicht
2.6 Schreibweise für Gleichgewichtsreaktionen
Die Lage des Gleichgewichts lässt sich durch unterschiedlich lange Gleichgewichtspfeile visualisieren. Am Beispiel des Estergleichgewichts (S = Säure, A = Alkohol, E = Ester, W = Wasser):
↑ Zum Vergrößern klicken
✕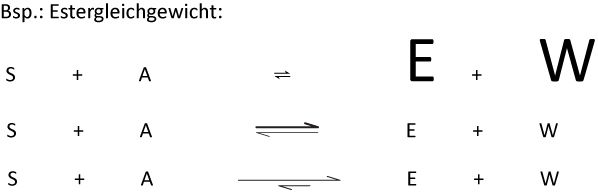
Merksatz – Pfeilnotation
- Gleich lange Pfeile (⇌): Gleichgewicht liegt in der Mitte – ähnlich viele Edukte wie Produkte.
- Längerer Pfeil nach rechts (⟹): Gleichgewicht liegt auf der Produktseite – Produkte überwiegen.
- Längerer Pfeil nach links (⟸): Gleichgewicht liegt auf der Eduktseite – Edukte überwiegen.
2.7 Kollisionsmodell und Reaktionsgeschwindigkeit
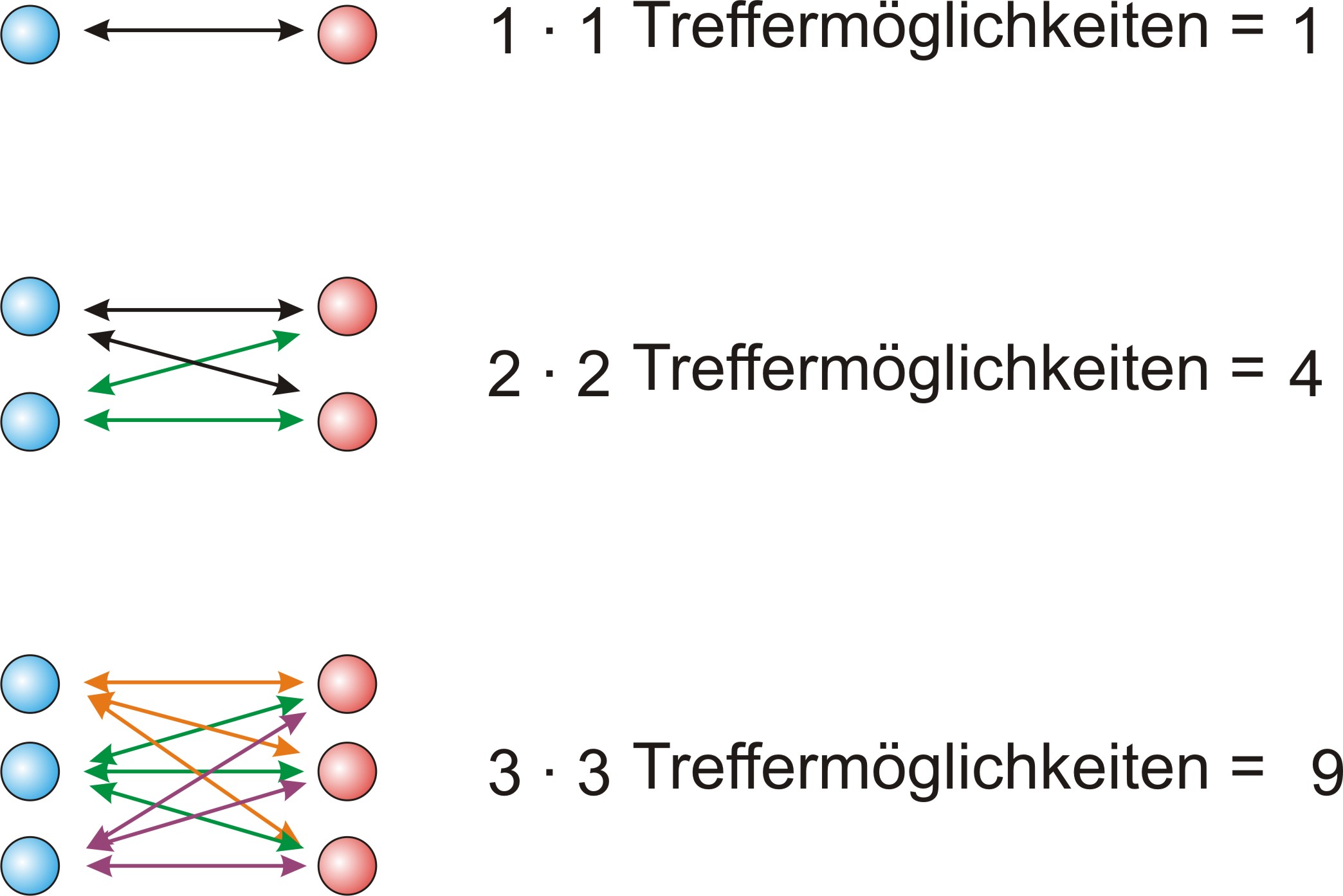
Das Kollisionsmodell erklärt, warum die Reaktionsgeschwindigkeit vom Produkt der Konzentrationen der Reaktionspartner abhängt. Entscheidend ist die Anzahl der möglichen Zusammenstöße (Treffermöglichkeiten) zwischen Edukt-Teilchen:
↑ Zum Vergrößern klicken
✕
Das Kollisionsmodell liefert die Grundlage für das Massenwirkungsgesetz: Die Geschwindigkeit der Hinreaktion ist proportional zum Produkt der Edukt-Konzentrationen, die der Rückreaktion proportional zum Produkt der Produkt-Konzentrationen.
Aktivierungsenergie und Katalysator
Das Energiediagramm zeigt, wie ein Katalysator die Aktivierungsenergie senkt und damit die Reaktion beschleunigt:
↑ Zum Vergrößern klicken
✕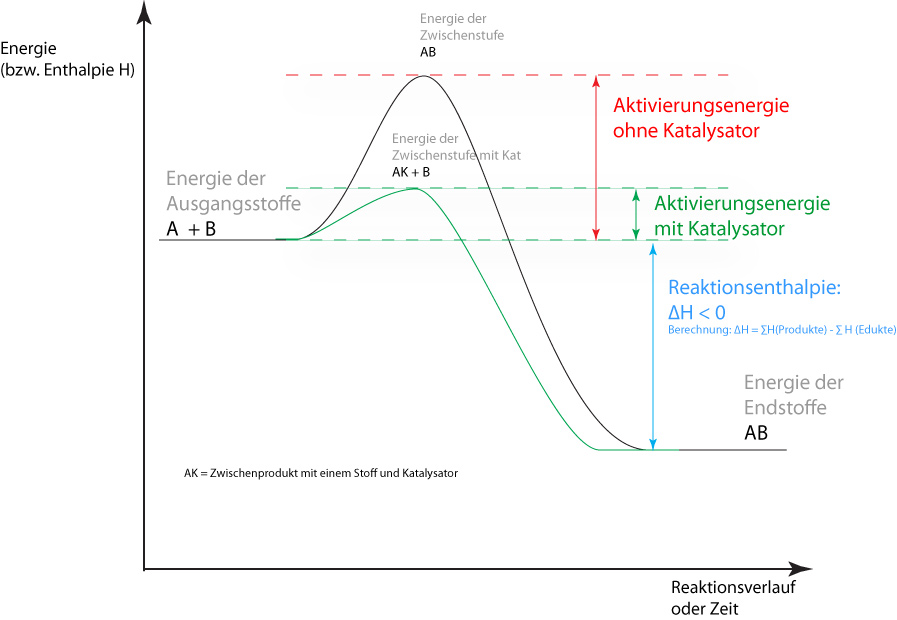
Wichtiger Hinweis zum Katalysator: Ein Katalysator senkt die Aktivierungsenergie für Hin- und Rückreaktion gleichermaßen. Er beschleunigt das Erreichen des Gleichgewichts – verschiebt es aber nicht. Die Lage des Gleichgewichts (Kc-Wert) bleibt durch einen Katalysator unverändert.
Auf einen Blick – die wichtigsten Aussagen
Pfeilnotation
Die Länge der Gleichgewichtspfeile zeigt die Lage des Gleichgewichts: Längerer Pfeil = bevorzugte Reaktionsrichtung.
Kollisionsmodell
Treffermöglichkeiten = n(A) · n(B). Verdoppelt man beide Konzentrationen, vervierfacht sich die Reaktionsrate (2·2 = 4).
Aktivierungsenergie
Ein Katalysator senkt die Aktivierungsenergie über ein energieärmeres Zwischenprodukt (AK). Die Reaktionsenthalpie ΔH bleibt unverändert.
Katalysator ≠ Verschiebung
Ein Katalysator beschleunigt Hin- und Rückreaktion gleichermaßen. Er bringt das System schneller ins Gleichgewicht – verschiebt es aber nicht.
Häufige Fragen – Schreibweise und Kollisionsmodell
Was bedeutet es, wenn ein Gleichgewichtspfeil länger ist als der andere?
Ein längerer Pfeil zeigt die bevorzugte Reaktionsrichtung an. Zeigt der längere Pfeil nach rechts (→⇌), liegt das Gleichgewicht auf der Produktseite – es bilden sich mehr Produkte als Edukte. Zeigt er nach links (⇌←), überwiegen die Edukte. Gleich lange Pfeile (⇌) bedeuten: ähnlich viele Edukte und Produkte im Gleichgewicht. Das genaue Verhältnis beschreibt der Kc-Wert.
Was besagt das Kollisionsmodell für Gleichgewichtsreaktionen?
Die Geschwindigkeit einer Reaktion hängt davon ab, wie oft sich Teilchen treffen und zusammenstoßen. Die Anzahl der Treffermöglichkeiten ist proportional zum Produkt der Teilchenzahlen (bzw. Konzentrationen) der Reaktionspartner: Wenn n(A) = 2 und n(B) = 2, gibt es 2 · 2 = 4 Treffermöglichkeiten. Bei n(A) = 3 und n(B) = 3 sind es 3 · 3 = 9. Dieses Prinzip bildet die Grundlage des Massenwirkungsgesetzes.
Was passiert mit der Reaktionsgeschwindigkeit, wenn man eine Konzentration verdoppelt?
Für die Reaktion A + B → Produkte gilt nach dem Kollisionsmodell: v ∝ [A] · [B]. Verdoppelt man nur [A] (von 1 auf 2), verdoppeln sich die Treffermöglichkeiten. Verdoppelt man beide Konzentrationen, vervierfachen sich die Treffermöglichkeiten (2 · 2 = 4). Die Reaktionsgeschwindigkeit steigt also quadratisch, wenn man beide Eduktkonzentrationen verdoppelt. Wichtig: Das gilt analog für die Rückreaktion mit den Produktkonzentrationen.
Wie wirkt ein Katalysator auf die Aktivierungsenergie – und warum verschiebt er das Gleichgewicht nicht?
Ein Katalysator bildet ein energieärmeres Zwischenprodukt (AK) mit einem der Reaktionspartner. Dadurch ist die Aktivierungsenergie für die Hinreaktion und für die Rückreaktion gleichermaßen kleiner. Beide Reaktionen werden schneller – aber im gleichen Verhältnis. Da sich beide Geschwindigkeiten proportional ändern, bleibt das Gleichgewicht (Kc) unverändert.
Merksatz: Ein Katalysator verändert nicht, wo das Gleichgewicht liegt, sondern nur, wie schnell es erreicht wird. Mehr zur Verschiebung des Gleichgewichts: Prinzip von Le Chatelier.Was ist der Unterschied zwischen Reaktionsenthalpie ΔH und Aktivierungsenergie EA?
Die Reaktionsenthalpie ΔH ist der Energieunterschied zwischen Edukten und Produkten – sie beschreibt, ob eine Reaktion exotherm (ΔH < 0) oder endotherm (ΔH > 0) ist. Die Aktivierungsenergie EA ist die Energiebarriere, die Teilchen überwinden müssen, damit die Reaktion überhaupt abläuft. Ein Katalysator senkt EA, ändert aber nicht ΔH. Die thermodynamischen Hintergründe zu ΔH findest du in der Energetik: Enthalpie H.
Lernkarten – Schreibweise und Kollisionsmodell
Klicke auf eine Karte, um die Antwort zu sehen.
1Was zeigt ein längerer Pfeil auf der rechten Seite des Gleichgewichtspfeils (A ⇌⟹ B) an?
Das Gleichgewicht liegt auf der Produktseite. Es überwiegen die Produkte. Kc > 1.
2Wie viele Treffermöglichkeiten gibt es bei 4 blauen und 4 roten Teilchen?
4 · 4 = 16 Treffermöglichkeiten. Allgemein: Treffermöglichkeiten = n(A) · n(B).
3Erkläre: Warum ändert ein Katalysator die Lage des Gleichgewichts nicht?
Ein Katalysator senkt die Aktivierungsenergie für Hin- UND Rückreaktion gleichermaßen. Beide Geschwindigkeiten steigen im gleichen Verhältnis → Kc bleibt unverändert.
4Was ändert ein Katalysator, was ändert er nicht?
Ändert: Aktivierungsenergie EA (senkt sie) · Reaktionsgeschwindigkeit (erhöht sie) · Zeit bis zum GG (verkürzt sie)
Ändert nicht: ΔH · Kc · Gleichgewichtslage5Bei 25 °C beträgt Kc für A ⇌ B = 9. Im GG gilt [A] = 0,3 mol/L. Berechne [B] und zeichne die passenden Gleichgewichtspfeile.
Kc = [B]/[A] = 9
[B] = 9 · 0,3 = 2,7 mol/L
Produkte überwiegen stark → längerer Pfeil rechts (A ⇌⟹ B)Weiter im Kapitel Gleichgewichtsreaktionen
← Estergleichgewicht → Benzoesäure-Gleichgewicht
🔁 Verwandte Seiten: Massenwirkungsgesetz · Prinzip von Le Chatelier · Enthalpie H (Energetik)
-
2.9 Säure-Base-Reaktion mit Benzoesäure
Was du auf dieser Seite lernst
Am Beispiel der Benzoesäure lernst du, wie chemische Gleichgewichte in der Säure-Base-Chemie konkret aussehen. Du verstehst, warum schwache Säuren nicht vollständig reagieren, warum Benzoesäure sich kaum in Wasser löst – und wie die Zugabe einer starken Base oder starken Säure das Gleichgewicht vollständig auf eine Seite verschiebt.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säure-Base-Reaktionen hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9) · → Stärke von Säuren und Basen (Kl. 9)
2.8 Allgemeines Zahlenbeispiel
A + B ⇌ C + D Vorher 1000 1000 0 0 Nachher 1000 − X 1000 − X X X z.B. im GG 800 800 200 200 2.9 Säure-Base-Reaktionen mit Benzoesäure
↑ Zum Vergrößern klicken
✕
a) Benzoesäure + Wasser
Man gibt feste Benzoesäure in Wasser. Dabei beobachtet man, dass die Benzoesäure als weiße Substanz oben auf dem Wasser schwimmt. Auch mit Schütteln löst sie sich nicht auf.
Frage: Warum löst sich Benzoesäure nicht in Wasser? Dafür muss man sich einmal Benzoesäure anschauen (Hinweis: Benzoesäure ist noch vereinfacht „falsch" geschrieben, da wir die Aromaten erst später genauer betrachten).
↑ Zum Vergrößern klicken
✕Erklärt, warum Benzoesäure nur schlecht in Wasser löslich ist!
✕Lösung: Löslichkeit der Benzoesäure
Bei Benzoesäure ist ein großer Teil unpolar (der Benzolring). Der polare Teil (die –COOH-Gruppe) ist kleiner. Die Benzoesäure kann zwar mit Wasser H-Brücken ausbilden, aber der große unpolare Rest sorgt für eine schlechte Löslichkeit.
↑ Zum Vergrößern klicken
Hinweis: Ähnliches löst sich in Ähnlichem.
Zusammenfassung Beobachtung: wenig löslich in Wasser; die Lösung reagiert schwach sauer.
Formuliert die Reaktionsgleichung für die Reaktion von Benzoesäure mit Wasser mit bindenden und nichtbindenden Elektronenpaaren (Hinweis: Benzoesäure ist jetzt schon etwas vereinfacht geschrieben, indem die H-Atome am Ring weggelassen wurden).
✕Lösung: Reaktionsgleichung Benzoesäure + Wasser
↑ Zum Vergrößern klicken
Es findet nur eine schwache Reaktion mit H2O statt. Es reagieren nur wenige Benzoesäuremoleküle. Das Gleichgewicht liegt links.

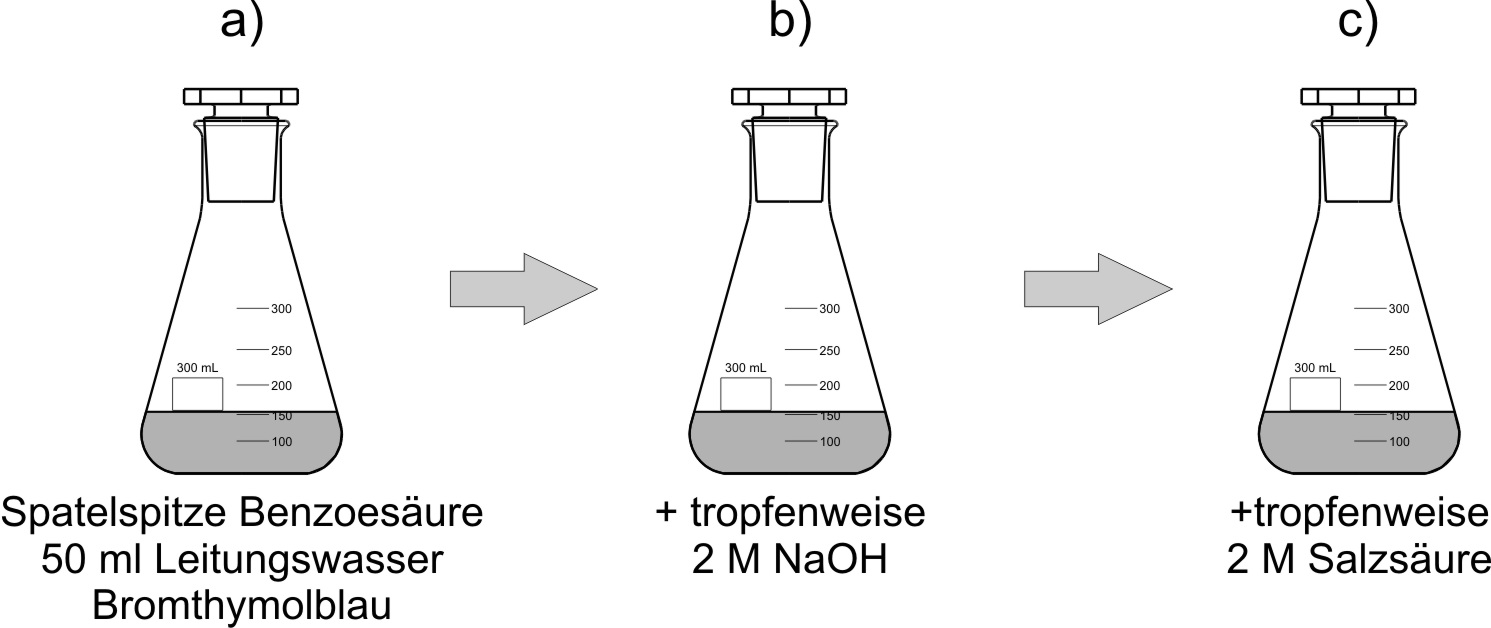
b) Benzoesäure + Natronlauge (Neutralisation)
Man gibt vorsichtig Natronlauge zu und schüttelt die Lösung, bis die Benzoesäure vollständig aufgelöst ist.
Beobachtung: Es entsteht eine klare Lösung.Formuliert hierfür auch wieder eine Reaktionsgleichung mit bindenden und nichtbindenden Elektronenpaaren.
✕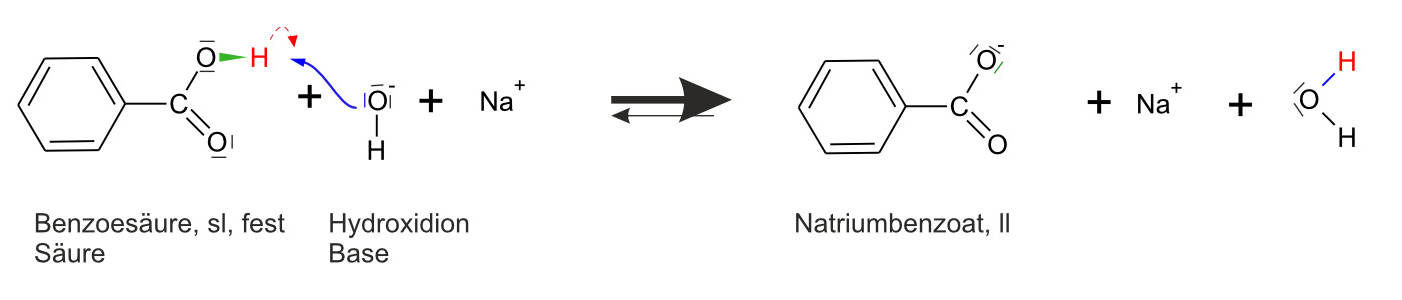
Die Benzoesäuremoleküle reagieren praktisch vollständig (das Gleichgewicht liegt weit auf der rechten Seite).
c) Gelöstes Natriumbenzoat + verd. Salzsäure
Die klare Natriumbenzoat-Lösung wird mit verdünnter Salzsäure versetzt.
✕
Beobachtung: Die klare Lösung wird trübe. Eine weiße, pulverartige Substanz schwimmt wieder auf der Oberfläche.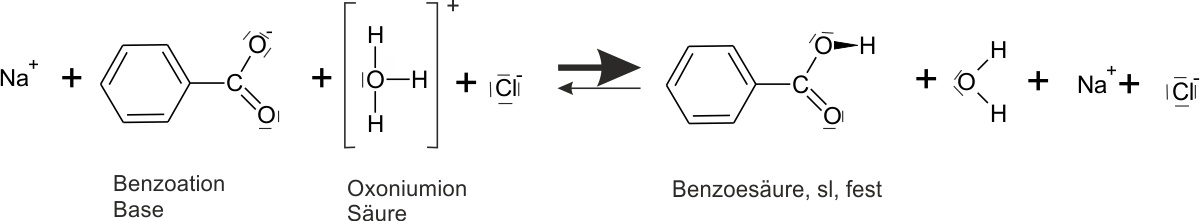
Feste Benzoesäure scheidet sich ab; die Benzoat-Anionen reagieren praktisch vollständig.
Auf einen Blick – die wichtigsten Aussagen
SCHWACHE SÄURE
Benzoesäure ist eine schwache Säure: das Gleichgewicht mit Wasser liegt links – es reagieren nur wenige Moleküle.
LÖSLICHKEIT
Der große unpolare Benzolring überwiegt die polare –COOH-Gruppe: Benzoesäure ist deshalb wenig wasserlöslich.
STARKE BASE
Natronlauge (starke Base) lässt Benzoesäure vollständig reagieren → klare Natriumbenzoat-Lösung entsteht.
STARKE SÄURE
Salzsäure (starke Säure) verdrängt Benzoesäure aus dem Benzoat-Salz → weißer Feststoff fällt wieder aus.
Häufige Fragen – Benzoesäure-Gleichgewicht
Warum löst sich Benzoesäure kaum in Wasser?
Benzoesäure besteht aus einem großen unpolaren Benzolring und einer kleineren polaren Carboxylgruppe (–COOH). Da „Ähnliches Ähnliches löst", ist der unpolare Anteil so dominant, dass die Wasserlöslichkeit sehr gering bleibt – obwohl die –COOH-Gruppe H-Brücken zu Wasser ausbilden kann. Mehr zur Struktur von Benzol und seinen Derivaten: → Aromaten (Kursstufe).
Warum liegt das Gleichgewicht von Benzoesäure + Wasser auf der linken Seite?
Benzoesäure ist eine schwache Säure: Sie gibt Protonen nur in geringem Umfang an Wasser ab. Im Gleichgewicht überwiegen daher die Edukte (undissoziierte Benzoesäure + Wasser) gegenüber den Produkten (Benzoat-Ion + Hydronium-Ion). Man sagt: das Gleichgewicht liegt links. Ein kleiner Kc-Wert (Ks ≈ 6,3 · 10−5) bestätigt das. Grundlagen zur Gleichgewichtslage: → Merkmale eines chemischen Gleichgewichts.
Was geschieht, wenn man Benzoesäure mit Natronlauge versetzt?
Natronlauge enthält OH−-Ionen (eine starke Base). Diese reagieren mit der Benzoesäure vollständig zu Natriumbenzoat (C6H5COO− Na+) und Wasser. Das Benzoat-Ion ist gut wasserlöslich → die zuvor trübe Suspension wird klar. Diese vollständige Reaktion ist möglich, weil NaOH eine viel stärkere Base ist als Wasser. Verwandte Grundlagen: → Neutralisation (Kl. 9).
Was passiert beim Ansäuern von Natriumbenzoat-Lösung mit Salzsäure?
Salzsäure (HCl) ist eine starke Säure und gibt bereitwillig Protonen an das Benzoat-Ion ab. Dabei wird Benzoesäure zurückgebildet, die sich wegen ihrer geringen Wasserlöslichkeit sofort als weißer Feststoff abscheidet (Lösung wird trüb). Stärkere Säuren verdrängen schwächere Säuren aus ihren Salzen – ein direktes Anwendungsbeispiel des Stärke-Prinzips von Säuren und Basen (Kl. 9).
Wie berechnet man Kc für das allgemeine Zahlenbeispiel A + B ⇌ C + D?
Im Zahlenbeispiel liegen im Gleichgewicht vor: A = 800, B = 800, C = 200, D = 200 (gleiche Einheit, z. B. mmol/L). Das Massenwirkungsgesetz ergibt:
Kc = [C] · [D] / ([A] · [B]) = 200 · 200 / (800 · 800) = 40.000 / 640.000 ≈ 0,0625
Ein Kc < 1 zeigt: die Edukte überwiegen im Gleichgewicht (Gleichgewicht liegt links). Mehr dazu: → Massenwirkungsgesetz (MWG).
Lernkarten – Benzoesäure-Gleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was versteht man unter einer schwachen Säure – und wo liegt ihr Gleichgewicht?
Eine schwache Säure gibt Protonen nur in geringem Umfang ab. Das Gleichgewicht liegt auf der Seite der Edukte (undissoziierte Säure überwiegt). Ks ist klein (≪ 1).
2Warum ist Benzoesäure nur wenig in Wasser löslich?
Der große unpolare Benzolring überwiegt die polare –COOH-Gruppe. Da ähnliches ähnliches löst, bleibt Benzoesäure in Wasser weitgehend unlöslich.
3Was beobachtet man beim Zugeben von Natronlauge zur Benzoesäure-Suspension?
Die trübe Suspension wird klar. Benzoesäure reagiert vollständig mit OH− zu gut löslichem Natriumbenzoat. Die starke Base verschiebt das Gleichgewicht vollständig nach rechts.
4Was passiert, wenn man Natriumbenzoat-Lösung mit verdünnter Salzsäure ansäuert?
Die klare Lösung wird trübe: Benzoesäure wird zurückgebildet und fällt als weißer Feststoff aus. HCl (starke Säure) verdrängt Benzoesäure (schwache Säure) aus ihrem Salz.
5Rechenaufgabe: A + B ⇌ C + D. Im GG: [A] = [B] = 0,80 mol/L, [C] = [D] = 0,20 mol/L. Berechne Kc und gib die Gleichgewichtslage an.
Kc = (0,20 · 0,20) / (0,80 · 0,80) = 0,04 / 0,64 ≈ 0,0625
Kc < 1 → Gleichgewicht liegt links (Edukte überwiegen).Weiter im Kapitel Gleichgewichtsreaktionen
← 2.6/2.7 Schreibweise und Kollisionsmodell → 2.10 Verschiebung des Gleichgewichts
← 2.5 Estergleichgewicht → 2.12 Massenwirkungsgesetz
🔁 Grundlagen: Brønsted-Definition (Kl. 9) · Stärke von Säuren und Basen (Kl. 9) · Neutralisation (Kl. 9)
🔗 Weiterführend: Aromaten – Benzol und Derivate (Kursstufe) · Autoprotolyse und pH-Wert (Kursstufe)


