Indikatoren
-
3.2 Ammoniak-Gas + Wasser
Was du auf dieser Seite lernst
Ammoniak ist ein Gas, das sich außergewöhnlich gut in Wasser löst – das zeigt der Springbrunnenversuch eindrucksvoll. Du lernst, wie Ammoniak mit Wasser nach der Brønsted-Theorie reagiert (Protolyse), warum dabei eine basische Lösung entsteht, und verstehst im Exkurs, warum Sprudelwasser sauer ist und wie man daraus den pH-Wert berechnet.
Grundlagen aus der 9. Klasse
Die Grundlagen zur Brønsted-Theorie (Protonendonator / Protonenakzeptor) hast du bereits in der 9. Klasse kennengelernt: → Brønsted-Theorie (Kl. 9) · → Säure-Base-Reaktionen (Kl. 9)
3.2 Ammoniak-Gas + Wasser (Springbrunnen 2)
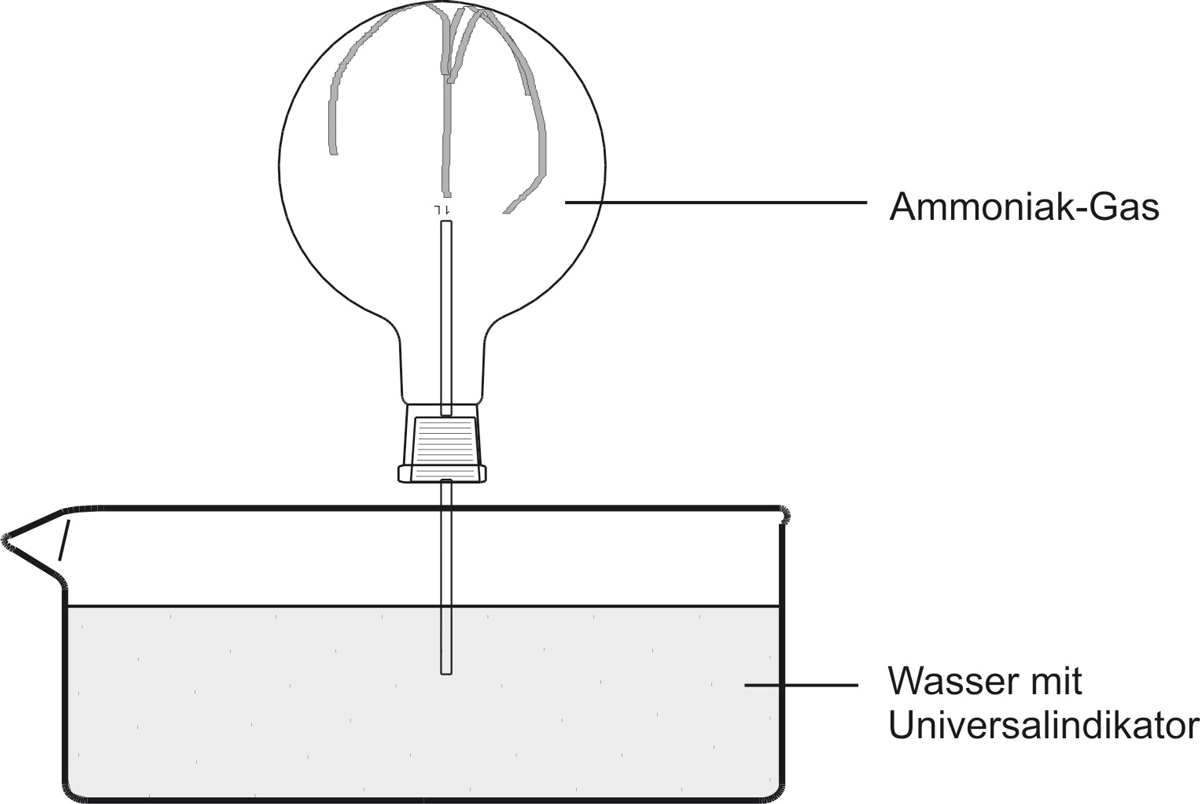
a) Versuch
↑ Zum Vergrößern klicken
✕
b) Beobachtung
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach blau um. Die blaue wässrige Lösung riecht nach Ammoniak.
c) Erklärung
Ammoniak-Gas löst sich sehr gut in Wasser und reagiert teilweise mit Wasser. Im Kolben entsteht durch das Lösen des Gases ein starker Unterdruck. Die entstehenden Hydroxid-Ionen (OH⁻) färben den Universalindikator blau.
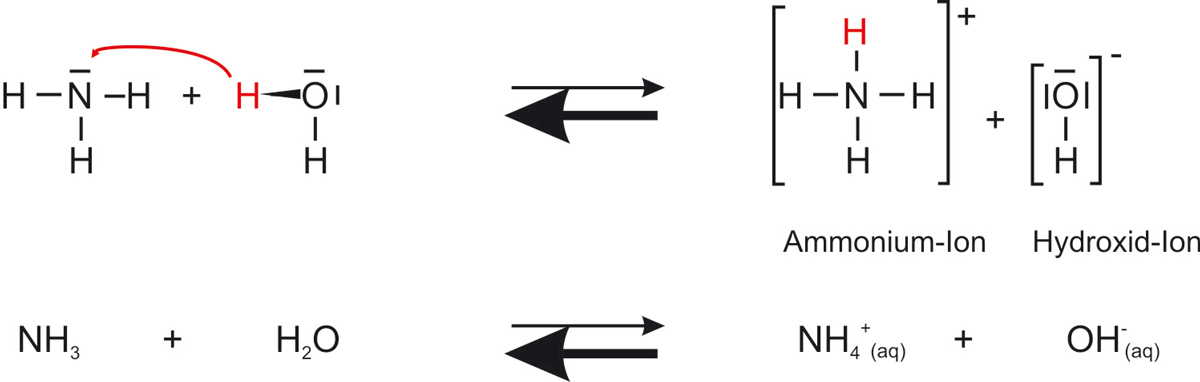
d) Reaktionsgleichung (mit Strukturformeln und Summenformeln)
Versuche die Gleichung erst selbst zu formulieren!
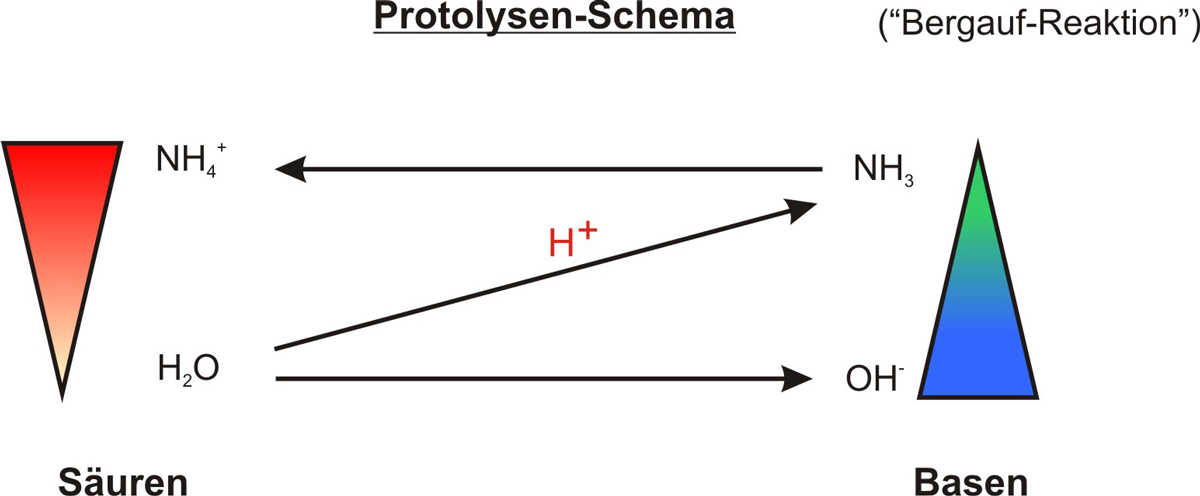
Formuliere nun das Protolyseschema:
Exkurs: Was macht den Sprudel sauer?
Kohlenstoffdioxid reagiert beim Lösen in Wasser im Gleichgewicht zu Kohlensäure:
CO₂ (g) + H₂O (l) ⇌ „H₂CO₃" (aq) – instabil (→ Erlenmeyer-Regel: zwei OH-Gruppen am selben C-Atom sind nicht beständig)
1. Protolysestufe: H₂CO₃ (aq) + H₂O (l) ⇌ HCO₃⁻ (aq) + H₃O⁺ (aq)
2. Protolysestufe: HCO₃⁻ (aq) + H₂O (l) ⇌ CO₃²⁻ (aq) + H₃O⁺ (aq)
Nachweis der H₃O⁺-Ionen durch:
- Geschmack (sauer)
- pH-Papier
- pH-Meter
Messwert: pH(Sprudel) = 5,1
Berechnung der Oxoniumionen-Konzentration:
pH = −lg c(H₃O⁺)
c(H₃O⁺) = 10−pH = 10−5,1 ≈ 7,9 · 10−6 mol/L
Auf einen Blick – die wichtigsten Aussagen
Springbrunneneffekt
NH₃ löst sich so gut in Wasser, dass im Kolben ein starker Unterdruck entsteht – das Wasser „schießt" nach oben in den Rundkolben.
Protolyse (Brønsted)
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻. NH₃ ist Protonenakzeptor (Base), H₂O ist Protonendonator (Säure). Lösung basisch (pH > 7).
Erlenmeyer-Regel
H₂CO₃ ist instabil – zwei OH-Gruppen am selben C-Atom sind nicht beständig. H₂CO₃ zerfällt sofort in CO₂ und H₂O.
pH-Rechnung
pH = −lg c(H₃O⁺) · c(H₃O⁺) = 10−pH
Sprudel: pH 5,1 → c(H₃O⁺) ≈ 7,9 · 10−6 mol/LHäufige Fragen – Ammoniak und Wasser
Warum steigt beim Springbrunnenversuch das Wasser von selbst auf?
Ammoniak löst sich außergewöhnlich gut in Wasser (ca. 700 Liter NH₃ in 1 Liter Wasser bei Raumtemperatur). Sobald Wasser mit dem Ammoniak-Gas in Berührung kommt, löst sich das Gas nahezu vollständig. Der Gasdruck im Kolben fällt schlagartig ab – es entsteht ein starker Unterdruck. Der Atmosphärendruck drückt daraufhin das Wasser durch die Glasspitze nach oben in den Kolben.
Ist NH₃ in Wasser eine Säure oder eine Base?
Nach Brønsted ist NH₃ eine Base: Es nimmt ein Proton (H⁺) vom Wasser auf und bildet das Ammoniumion NH₄⁺. Gleichzeitig gibt Wasser ein Proton ab und wird zur konjugierten Base OH⁻. Die Reaktion verläuft als Gleichgewicht:
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
Da OH⁻-Ionen entstehen, ist die Lösung basisch (pH > 7), was der Universalindikator durch Blaufärbung anzeigt.Was bedeutet „konjugiertes Säure-Base-Paar"?
Ein konjugiertes Säure-Base-Paar unterscheidet sich nur um ein Proton H⁺. Bei der Ammoniak-Protolyse gibt es zwei solche Paare:
- NH₄⁺ / NH₃ – NH₄⁺ ist die Säure, NH₃ die konjugierte Base
- H₂O / OH⁻ – H₂O ist die Säure, OH⁻ die konjugierte Base
Das Protolyseschema stellt diese Paare mit Pfeilen dar und zeigt, in welche Richtung das Proton wandert. Mehr dazu auf der Seite → Brønsted-Theorie.
Was ist die Erlenmeyer-Regel und wozu braucht man sie?
Die Erlenmeyer-Regel besagt: Verbindungen, bei denen zwei Hydroxyl-Gruppen (OH) an demselben Kohlenstoffatom gebunden sind, sind instabil und wandeln sich spontan um. Kohlensäure H₂CO₃ hätte formal zwei OH-Gruppen am gleichen C-Atom – sie ist daher so instabil, dass sie sofort in CO₂ und H₂O zerfällt. Diese Regel erklärt, warum im Sprudelwasser kein stabiles H₂CO₃ vorliegt, sondern CO₂ im Gleichgewicht mit Wasser steht und dabei H₃O⁺-Ionen entstehen.
Wie berechnet man aus dem pH-Wert die Oxoniumionen-Konzentration?
Formel: pH = −lg c(H₃O⁺), umgestellt: c(H₃O⁺) = 10−pH
Beispiel Sprudel mit pH = 5,1:
c(H₃O⁺) = 10−5,1 ≈ 7,9 · 10−6 mol/LZum Vergleich: Reines Wasser hat c(H₃O⁺) = 10−7 mol/L (pH = 7). Weitere Berechnungen findest du auf der Seite → pH-Wert berechnen.
Lernkarten – Ammoniak und Wasser
Klicke auf eine Karte, um die Antwort zu sehen.
1Warum entsteht beim Springbrunnenversuch ein Unterdruck im Kolben?
NH₃ löst sich extrem gut in Wasser → Gas verschwindet aus der Gasphase → Druck sinkt → Unterdruck → Atmosphärendruck drückt Wasser nach oben.
2Formuliere die vollständige Protolysegleichung von NH₃ mit Wasser.
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
NH₃ = Base (Protonenakzeptor)
H₂O = Säure (Protonendonator)3Nenne die beiden konjugierten Säure-Base-Paare bei der Ammoniak-Protolyse.
Paar 1: NH₄⁺ (Säure) / NH₃ (Base)
Paar 2: H₂O (Säure) / OH⁻ (Base)4Warum ist Sprudelwasser sauer, obwohl H₂CO₃ instabil ist?
CO₂ reagiert im Gleichgewicht mit H₂O. Auch ohne stabiles H₂CO₃ entstehen durch Protolyse H₃O⁺-Ionen (Erlenmeyer-Regel) → saure Lösung (pH ≈ 5,1).
5Berechne: Ein Sprudel hat pH = 4,5. Wie groß ist c(H₃O⁺)?
c(H₃O⁺) = 10−pH = 10−4,5 ≈ 3,2 · 10−5 mol/L
Weiter im Kapitel Säure-Base-Reaktionen
← 3 Protolyse-Reaktionen (Übersicht) → 3.3 Neutralisation
🔁 Grundlagen (Kl. 9): Säure-Base-Reaktionen (Kl. 9) · Brønsted-Theorie (Kl. 9) · Neutralisation (Kl. 9)
📈 Vertiefung: pH-Wert berechnen · pKB-Wert (Basestärke) · Pufferlösung
-
5. Indikatoren
Was du auf dieser Seite lernst
Du lernst, wie Säure-Base-Indikatoren funktionieren und warum ihr Farbumschlag beim pKS-Wert der schwachen Indikatorsäure liegt. Mit der Henderson-Hasselbalch-Gleichung berechnest du das Konzentrationsverhältnis HIn/In⁻ und bestimmst die Farbe des Indikators bei beliebigem pH. Die Farbskalen der wichtigsten Indikatoren geben dir einen schnellen Überblick.
Grundlagen – Kursstufe Säure-Base
Indikatoren sind Anwendungen der Henderson-Hasselbalch-Gleichung, die du auf der → Zusammenfassungsseite 4.6 hergeleitet hast. Das Prinzip des kleinsten Zwanges (Le Chatelier) wurde in der → Gleichgewichtschemie eingeführt.
5. Indikatoren
In der Regel ist ein Säure-Base-Indikator eine schwache, farbige organische Säure, deren korrespondierende Base eine andere Farbe hat:
HIn + H2O ⇌ In⁻ + H3O+Indikator-
säure
(Farbe 1)korrespond.
Indikator-
base
(Farbe 2)Farbwechsel – Prinzip des kleinsten Zwanges
Das Gleichgewicht reagiert auf pH-Änderungen nach dem Prinzip von Le Chatelier:
Saure Lösung (niedriger pH)
Hohe H3O+-Konzentration drängt das GG nach links → Farbe 1 überwiegt
Basische Lösung (hoher pH)
Niedrige H3O+-Konzentration drängt das GG nach rechts → Farbe 2 überwiegt
Hinweis: Die Farben Rot/Blau sind im Tafelbild willkürlich gewählt. Andere Indikatoren ergeben andere Farben – z. B. Phenolphthalein: sauer/neutral = farblos, alkalisch = pink/magenta.
Berechnung: Henderson-Hasselbalch-Gleichung für Indikatoren
Mit der allgemeinen Henderson-Hasselbalch-Gleichung (→ Zusammenfassung 4.6.3) kann man für jeden pH-Wert berechnen, in welchem Verhältnis die Indikatorsäure HIn zur Indikatorbase In⁻ vorliegt:
↑ Zum Vergrößern klicken
✕
Merksatz: Der Indikator schlägt um, wenn c(In⁻) = c(HIn), also wenn lg(1) = 0 → pH = pKS(HIn). Der sichtbare Umschlagbereich liegt bei pKS ± 1, weil das Auge erst ab einem 10:1-Verhältnis eine einheitliche Farbe wahrnimmt.
Beispiel: Lackmus (pKS = 7, KS = 10−7)
✕Aufgabe a) Berechne das Konzentrationsverhältnis von HIn (rot) zu In⁻ (blau) bei pH = 5!
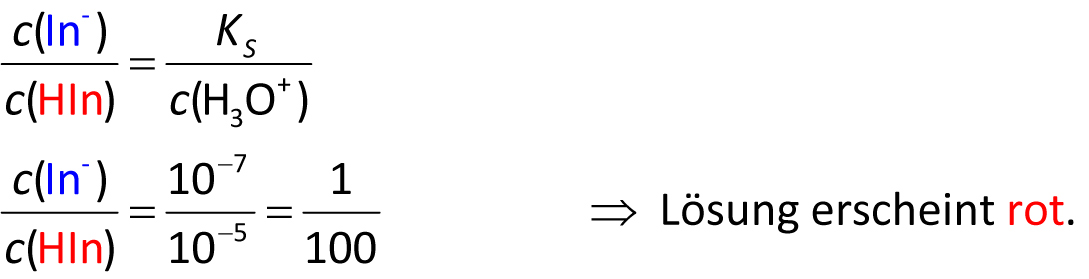 ✕
✕Aufgabe b) Welche Farbe hat der Lackmus-Indikator bei pH = 8?
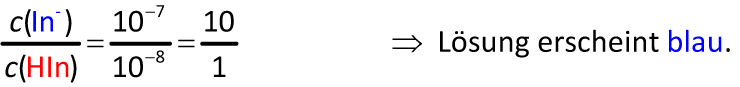
Aufgabe c) Welche Farbe liegt bei pH = 7 vor?
Bei pH = pKS = 7 gilt c(In⁻) = c(HIn) → beide Formen gleich konzentriert → Mischfarbe aus Rot und Blau = Purpur/Violett.
Das ist der Umschlagspunkt des Indikators.Der pH-Bereich, in dem die Farbe eines Indikators umschlägt, liegt demnach immer beim pKS-Wert der schwachen Säure HIn. Lackmus schlägt im Bereich pH ≈ pKS = 7 um (sichtbar zwischen pH 5 und pH 8).
Farbskalen wichtiger Indikatoren
Die Balken zeigen den Farbwechsel in Abhängigkeit vom pH-Wert (0–14). Der Umschlagbereich liegt stets bei pKS(HIn) ± 1. Das Auge nimmt eine einheitliche Farbe erst wahr, wenn ein Ion 10-fach überwiegt.
0 2 4 6 7 8 10 12 14Methylorange
Umschlag pH 3,1–4,4 · pKS ≈ 3,5● → ●Bromkresolgrün
Umschlag pH 3,8–5,4 · pKS ≈ 4,7● → ●Methylrot
Umschlag pH 4,4–6,2 · pKS ≈ 5,1● → ●Lackmus
Umschlag pH 5–8 · pKS ≈ 7● → ●Bromthymolblau (BTB)
Umschlag pH 6,0–7,6 · pKS ≈ 7,1● → ●Phenolphthalein
Umschlag pH 8,2–10 · pKS ≈ 9,4farbl. → ●sauer neutral basisch* Phenolphthalein: farblos unterhalb pH 8,2, pink/magenta im Bereich 8,2–10, ab pH 12 wieder farblos. Für die Säure-Base-Titration ist der Umschlag bei pH ≈ 9 besonders gut geeignet (Titration starker Säure mit starker Base). Mehr dazu: Säure-Base-Titration.
Auf einen Blick – die wichtigsten Aussagen
Indikator = schwache Säure
HIn und In⁻ haben verschiedene Farben. Das Gleichgewicht verschiebt sich mit dem pH.
Umschlagbereich
Umschlag bei pH = pKS(HIn). Sichtbarer Bereich: pKS ± 1.
Henderson-Hasselbalch
pH = pKS + lg(c(In⁻)/c(HIn))
→ bestimmt Farbverhältnis bei jedem pHIndikatorwahl
Indikator für Titration wählen, dessen pKS(HIn) nahe dem Äquivalenzpunkt liegt.
Häufige Fragen – Indikatoren
Warum zeigt ein Indikator verschiedene Farben bei verschiedenem pH?
Ein Indikator ist eine schwache organische Säure HIn, deren Säureform und Baseform unterschiedlich gefärbt sind. Ändert sich der pH, verschiebt sich nach Le Chatelier das Gleichgewicht HIn + H2O ⇌ In⁻ + H3O+: Bei niedrigem pH (viel H3O+) überwiegt HIn (Farbe 1), bei hohem pH überwiegt In⁻ (Farbe 2). Am Umschlagspunkt (pH = pKS) sind beide gleich konzentriert → Mischfarbe.
Welchen Indikator verwendet man für eine Titration?
Der pKS-Wert des Indikators sollte möglichst nahe am Äquivalenzpunkt der Titration liegen. Für die Titration einer starken Säure mit einer starken Base liegt der Äquivalenzpunkt bei pH = 7 → Lackmus oder Bromthymolblau (pKS ≈ 7) sind geeignet. Für schwache Säuren liegt der Äquivalenzpunkt im Basischen → Phenolphthalein (pKS ≈ 9,4) ist besser. Mehr dazu: Säure-Base-Titration.
Warum ist der Umschlagbereich immer pKS ± 1?
Das menschliche Auge nimmt eine Mischfarbe erst dann als eindeutige Farbe war, wenn eine Komponente 10-fach überwiegt (c(In⁻)/c(HIn) ≥ 10 oder ≤ 1/10). Nach der Henderson-Hasselbalch-Gleichung: pH = pKS + lg(10) = pKS + 1 bzw. pH = pKS − 1. Daraus folgt der sichtbare Umschlagbereich von pKS ± 1.
Warum ist Phenolphthalein im stark Basischen wieder farblos?
Phenolphthalein liegt in drei Formen vor: Bei pH < 8,2 als farblose Säureform, bei pH 8,2–10 als farbige chinoide Form (pink/magenta), und bei pH > 12 wird die chinoide Form durch weiteren OH⁻-Angriff in eine ebenfalls farblose Tri-Anion-Form umgewandelt. Dieses „Ausbleichen" im stark basischen Milieu ist für Titrationen zu beachten.
Wie berechnet man c(In⁻)/c(HIn) bei bekanntem pH?
Aus der Henderson-Hasselbalch-Gleichung umstellen: lg(c(In⁻)/c(HIn)) = pH − pKS, also c(In⁻)/c(HIn) = 10(pH − pKS). Beispiel Lackmus (pKS = 7) bei pH = 5: c(In⁻)/c(HIn) = 10(5−7) = 10−2 = 1/100 → 100-facher Überschuss HIn → Lösung erscheint rot. Mehr Formeln: Zusammenfassung 4.6.
Lernkarten – Indikatoren
Klicke auf eine Karte, um die Antwort zu sehen.
1Bei welchem pH-Wert schlägt ein Indikator um?
Am Umschlagspunkt gilt c(In⁻) = c(HIn).
→ pH = pKS(HIn)
Sichtbarer Bereich: pKS ± 12Was versteht man unter dem Umschlagbereich eines Indikators?
Der pH-Bereich, in dem das Auge den Farbwechsel wahrnimmt.
Liegt bei pKS ± 1, da das Auge erst bei 10:1-Verhältnis eine Reinfarbe sieht.3Wie lautet die Henderson-Hasselbalch-Gleichung für Indikatoren?
pH = pKS + lg(c(In⁻) / c(HIn))
Herleitung aus KS = c(H3O+)·c(In⁻)/c(HIn)4Warum ist Bromthymolblau für Neutraltitration gut geeignet?
pKS(BTB) ≈ 7,1 → Umschlagbereich pH 6–8.
Der Äquivalenzpunkt einer Stärkesäure-/Stärkebase-Titration liegt nahe pH 7 → BTB schlägt dort sicher um.5Rechenaufgabe: Welche Farbe hat Methylorange (pKS = 3,5) bei pH = 5?
c(In⁻)/c(HIn) = 10(5 − 3,5) = 101,5 ≈ 32
→ In⁻ überwiegt 32-fach → gelb (Baseform von Methylorange).Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← Zusammenfassung pH/pOH → Säure-Base-Titration
🔁 Grundlagen: Prinzip von Le Chatelier · Henderson-Hasselbalch-Gleichung (4.6.3)
📌 Weiterführend: Säure-Base-Titration · Pufferlösungen