Qualitative Elementaranalyse
-
01.1 Methan
1. Alkane
1.1 Methan
1.1.1 Vorkommen:
im Erdgas, Sumpfgas, Biogas, Grubengas
1.1.2 Eigenschaften:
- farb- und geruchloses Gas
- geringere Dichte als Luft
- brennbar
1.1.3 Ermittlung der Summenformel (Molekülformel) und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
Hierfür wird der zu untersuchende Stoff verbrannt und die Verbrennungsprodukte werden bestimmt.
Bildet sich Wasser, wird Wasserstoff als Element vorhanden sein;
Kohlenstoff kann man einmal als Ruß (bei unvollständiger Verbrennung) oder als Kohlenstoffdioxid nachweisen. Der Kohlenstoffdioxid-Nachweis erfolgt mit der Kalkwasserprobe. Hierfür wird das entstandene Gas in Kalkwasser eingeleitet. Trübt sich die Lösung, ist Kohlenstoffdioxid vorhanden.- Nachweis von Wasserstoff → Bildung von Wasser → WaTesMo-Papier oder wasserfreies Kupfersulfat.
- Nachweis von C → Bildung von CO2 → Nachweis als CaCO3.
Ca(OH)2 (aq) + CO2 (g) → CaCO3 (s) + H2O (l)
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) ergeben, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält
b) Bestimmung der molaren Masse
Mit Hilfe der Gaswägung kann man die Molare Masse von Methan bestimmen: M(Methan) = 16 g/mol
Molekülmasse von Methan 16 u
c) Summenformel:
Daraus ergibt sich folgende Summenformel.
CH4
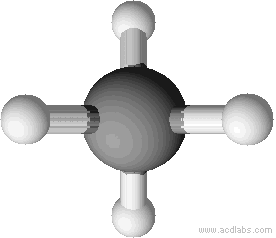
d) Strukturformel:Man zeichnet Methan meist mit einem Winkel von 90°. Dieser Winkel entspricht nicht dem Bindungswinkel (vgl. unten). Man kann sich aber vorstellen, dass man direkt auf das Molekül wie in der zweiten Abbildung dargestellt wird, blickt.
Tetraedrische Anordnung der Wasserstoffatome um das Kohlenstoffatom (Bindungswinkel 109,5 °).
Erklärung: Größtmögliche Entfernung der Wasserstoffatome.
1.1.4 Vollständige Verbrennung:0 -IV +I +IV -II +I -II
2 O2 + CH4 → CO2 + 2 H2O ΔH = - 888 kJ/molHinweis: Wenn die Ermittlungs der Oxidationszahlen Schwierigkeiten macht, dann kann man es hier nochmals nachlesen.
1l Methan benötigt zur vollständigen Verbrennung 10 Liter Luft (2 l Sauerstoff). -
01.4 Butan
Hinweis: 1.2 Ethan und 1.3 Propan wird nur bei ausreichend Zeit und entsprechend vorrätigen Chemikalien als einzelne Punkte besprochen. Da es aber sowieso ähnlich ist, wird an dieser Stelle auf den Heftaufschrieb verzichtet (vgl. weiter unten: Homologe Reihe).
1.4 Butan
1.4.1 Vorkommen
im Erdgas, fällt an bei der Benzingewinnung
1.4.2 Eigenschaften
farbloses Gas, größere Dichte als Luft
brennbar (Verbrennungsprodukte bei vollständiger Verbrennung: CO2 und H2O )
unter Druck leicht verflüssigbar
1.4.3 Ermittlung der Summenformel (Molekülformel) und Strukturformela) Qualitative Analyse (Elementaranalyse)
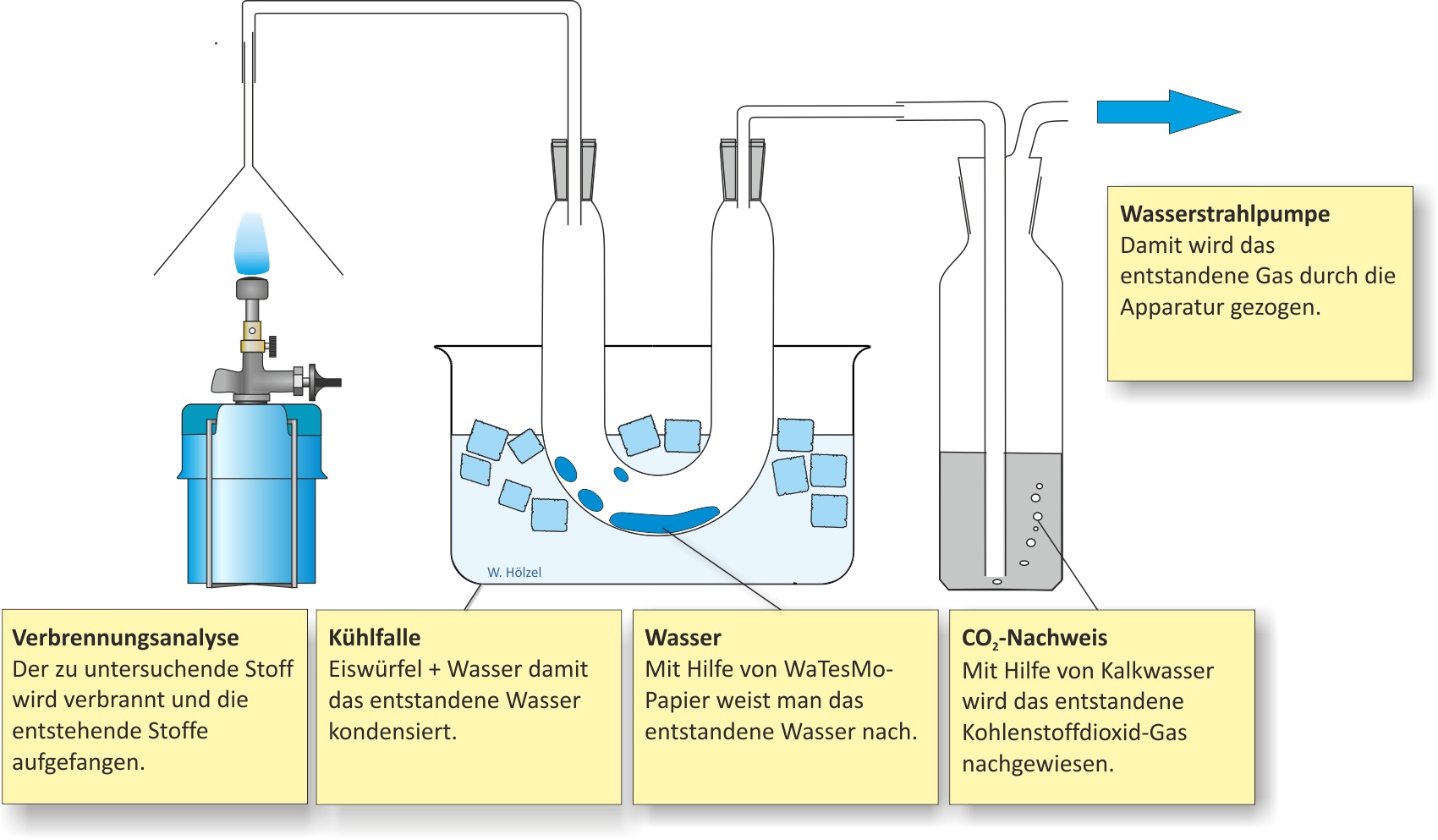
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) ergeben, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält
b) Bau und Formeln
1. Molare Masse = 58,12 g/mol
Molekülmasse = 58,12 u
2. Summenformel:C4H10
3. Strukturformel:
a) unverzweigte Kette b) verzweigte Kette
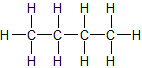
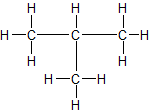
n-Butan Isobutan = 2-Methyl-Propan
Sdp.: - 0,5 °C Sdp.: - 12 °CZMK: nur van-der-Waals-Kräfte; bei n-Butan können sich die Moleküle dichter zusammenlagern und haben dadurch stärkere Zwischenmolekulare Kräfte, d.h. eine etwas höhere Siedetemperatur.
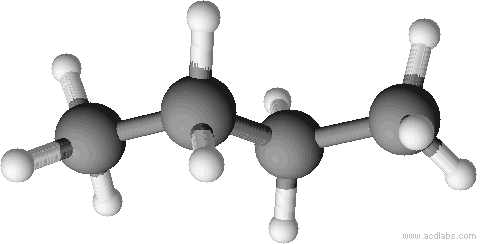
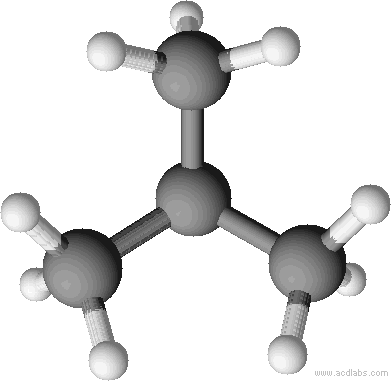
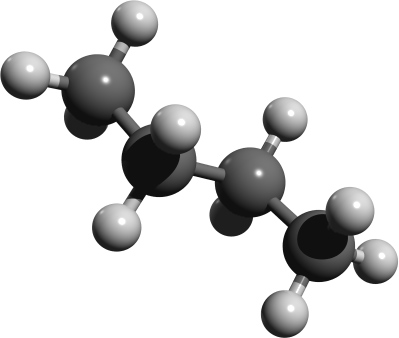
Räumliche Strukturen im Kugelstabmodell. Versucht die einzelnen Abbildungen Isobutan oder n-Butan zuzuordnen. Der Vorteil von Kugelstabmodelle sind, dass sie die Bindungen und Bindungswinkel anschaulich darstellen.
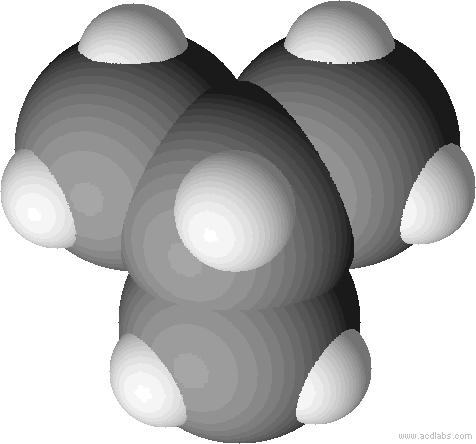
Kalottenmodell von 2-Methyl-Propan (= Isobutan). Bei Kalottenmodellen wird die Raumfüllung deutlich.
Da Strukturformeln bei größeren Molekülen zu lange dauern, hilft man sich mit der Halbstrukturformel aus, wobei die Wasserstoffatome quasi als Summenformel hinter das C geschrieben wird. Man schaut zunächst, wie viele Bindungen ein C schon hat und füllt dann mit so vielen H-Atomen auf, bis die Vierbindigkeit von Kohlenstoff erfüllt ist. Hier am Beispiel von Isobutan.
1.4.4 VerwendungHeizgas („blaue Gaskartuschen“), Kältemittel (Ersatz für FCKW), Treibgas in Sprays, Feuerzeuggas (häufig zusammen mit Propan)
1.4.5 Isomerie
(isos (griech.) = gleich; meros (griech.) = Teil)
Verbindungen, deren Moleküle bei gleicher Summenformel unterschiedliche Strukturformeln besitzen, bezeichnet man als Isomere. Isomere Verbindungen unterscheiden sich vor allem in ihren physikalischen Eigenschaften (Schmelz- und Siedepunkt) und wenig in ihren chemischen Reaktionen.
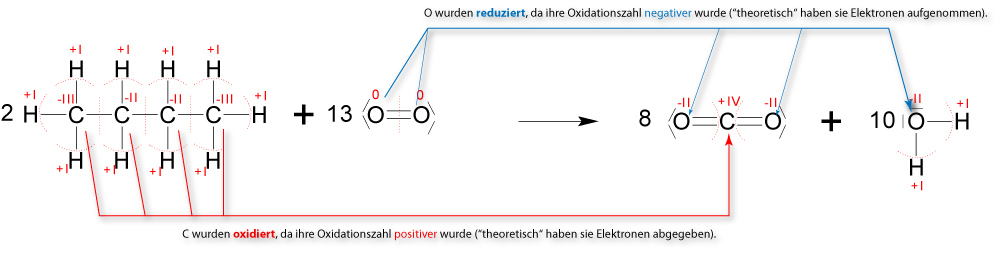
1.4.6 Vollständige Verbrennung (Oxidation)Wenn Butan vollständig verbrannt (oxidiert) wird, so entsteht dabei ausschließlich Kohlenstoffdioxid und Wasser.
-
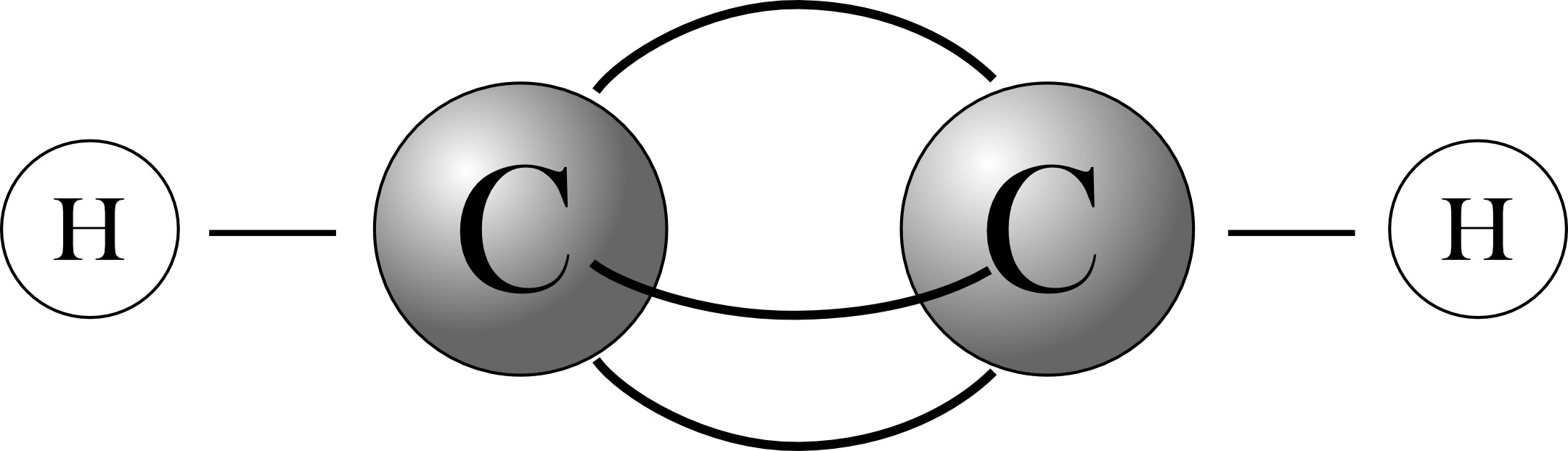
3.1 Ethin (Acetylen)
3.1 Ethin (Acetylen)
3.1.1 Eigenschaften
a) physikalische Eigenschaften
- farbloses Gas (geruchslos)
- leichter als Luft
- Smp.: -80,8°C
- Sdp.: - 84°C (Sublimation)
b) chemische
- brennt mit stark leuchtender und rußender Flamme
- entfärbt Bromwasser
- bildet mit Luft ein explosives Gemisch
- zerfällt unter Druck explosionsartig (⇨ nicht in Druckflaschen)
3.1.2 FormelermittlungVerbrennungsprodukte: H₂O, CO₂ (und bei unvollständiger Verbrennung C)
Molare Masse: M(Ethin) = 26 g/mol
Ermittel aus der molaren Masse die Summen- und die Strukturformel:
{slider title="Lösung" open="false" class="icon"}
Summenformel: C₂H₂
Strukturformel:
(linear; Bindungswinkel 180°)Bindungslänge noch geringer als bei der Doppelbindung (C=C: 134 pm; C=-C: 120 pm)
Ballmodell:3 „Bananenbindungen“, alle 4 Atome sind linear angeordnet.
{/sliders}
-
5.1.4 Versuch Ethanol reagiert mit Alkalimetall
5.1.4 Versuch: Ethanol + Alkalimetall
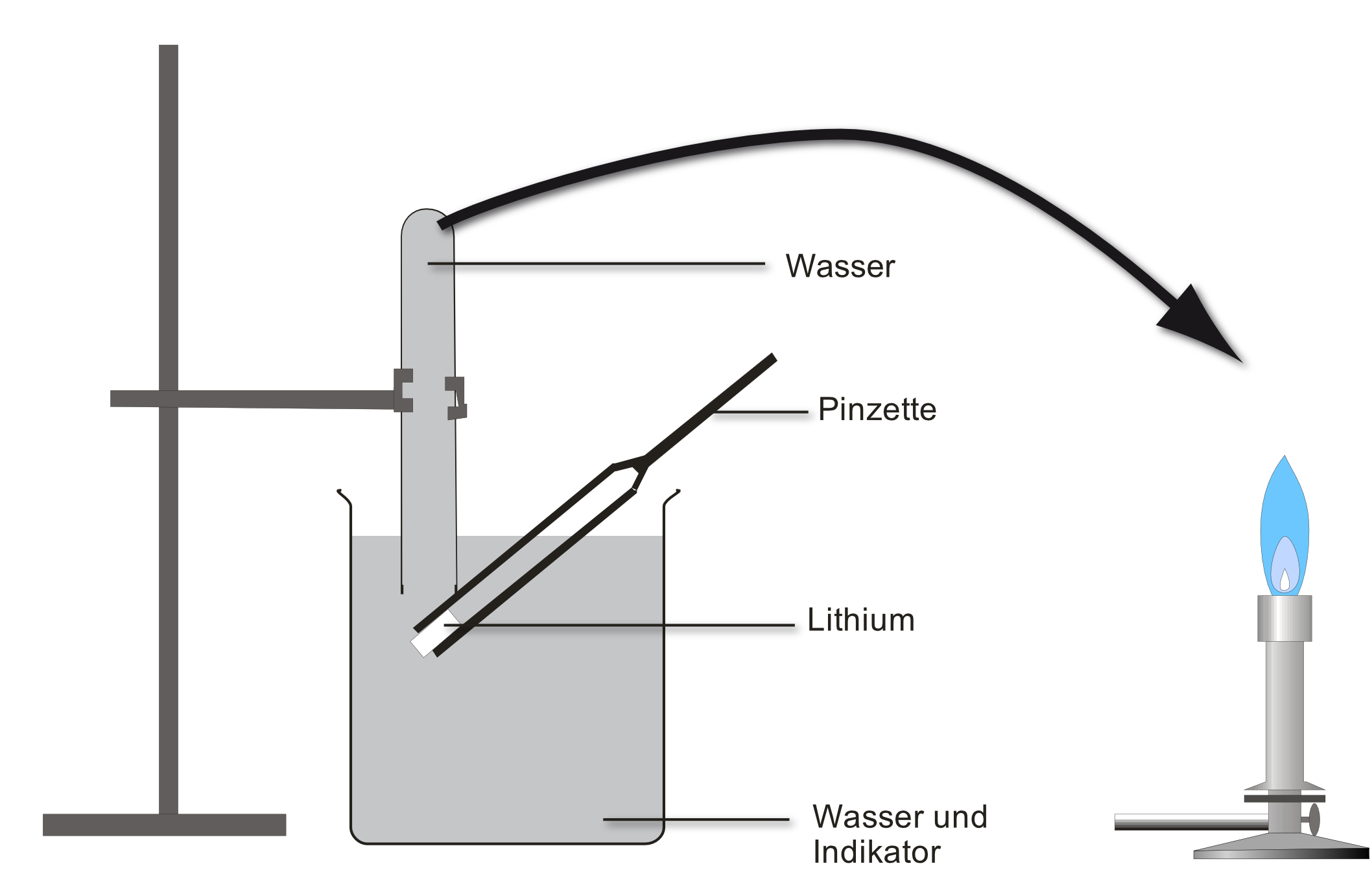
Versuch: Ein Stück Lithium ( SE ) wird auf Ethanol, Benzin und Wasser gegeben. Alternativ kann man die Experimente auch mit Natrium als Lehrerversuch durchführen. Die Reaktionsgleichungen sind mit dem Alkalimetall Natrium formuliert. Für Lithium gilt es analog.
Bei Wasser ist der Aufbau etwas komplizierter:
Beobachtung: Gasentwicklung; das entstehende Gas ist brennbar; Natrium „verschwindet“; die neu entstandene Lösung leitet den elektrischen Strom; dampft man die Lösung ein, entsteht ein weißer Feststoff.
Ergebnis:
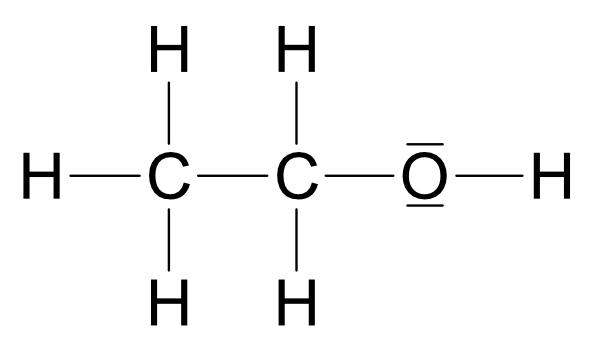
Ethanol (Struktur a) reagiert mit Natrium unter Wasserstoffbildung. Struktur b (Dimethylether) würde so nicht reagieren, da sich kein Proton abspalten kann. Somit besitzt Ethanol die Strukturformel:
1. Natrium + Wassera) Teilchengleichung (mit Strukturformeln)
2 Na (s) + 2 H₂O (l) → 2 NaOH (aq) + H₂ (g) Natrium Wasser Natriumhydroxid Wasserstoff fest flüssig gelöst gasförmig 2. Natrium + Ethanol
Man kann Ethanol ja als Derivate (=Abkömmlinge) von Wasser betrachten. Wasser hat ein Sauerstoff-Atom und zwei Wasserstoff-Atome; Ethanol hat ein Sauerstoff-Atom, ein Wasserstoff-Atom und eine Ethyl-Gruppe. Beim Ethanol ist also ein Wasserstoff-Atom durch eine Ethylgruppe ersetzt. Wenn wir diese Alkylgruppe als "Rest" betrachten, dann zeigt sich die Verwandtschaft von Ethanol mit Wasser. Hat man also die Reaktionsgleichung von Wasser mit Natrium verstanden, dann müsste einem auch die Reaktionsgleichung von Ethanol (und anderen Alkoholen) leichtfallen. Versucht nun einmal, die Reaktion von Natrium mit Ethanol zu formulieren.
a) Teilchengleichung (mit Strukturformeln)
{slider title="Lösung" open="false" class="icon"}
{/sliders}
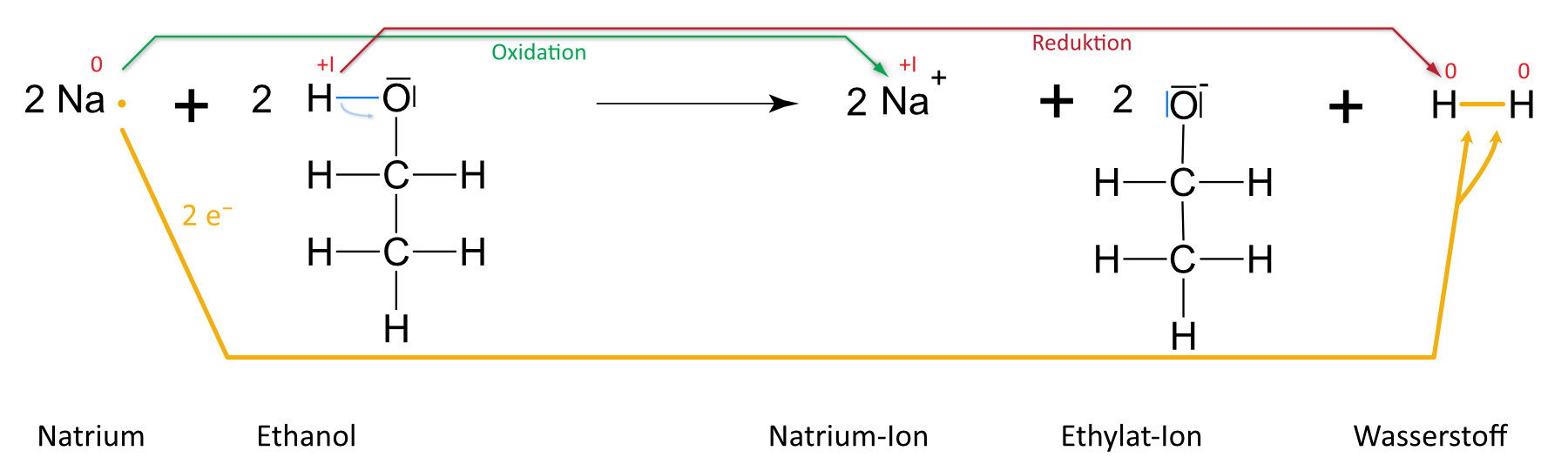
b) Reaktionsgleichung{slider title="Lösung" open="false" class="icon"}
2 Na (s) + 2 C₂H₅OH (l) 2 NaC₂H₅O (aq) + H₂ (g){/sliders}
Auswertung: Es ist keine „klassische“ Säure-Base-Reaktion nach Brönstedt. Grund: +I-Effekt (vgl. unten) der Methylgruppe (Protonierung ist erschwert). Es handelt sich hier um eine Redoxreaktion (Veränderung der Oxidationenszahlen). Formal geben zwei Moleküle Ethanol je ein Proton ab. Jedes Proton nimmt von einem Natrium- bzw. Lithiumatom ein Elektron auf; es bilden sich so zwei Wasserstoffatome, die sich zu einem Wasserstoffmolekül zusammenlagern. Analog, nur heftiger, verläuft die Reaktion mit Wasser.
Weitere Übungen:
Lithium und Methanol
Formuliert auch dafür die Reaktionsgleichung (vgl. oben)
{slider title="Lösung" open="false" class="icon"}
{/sliders}
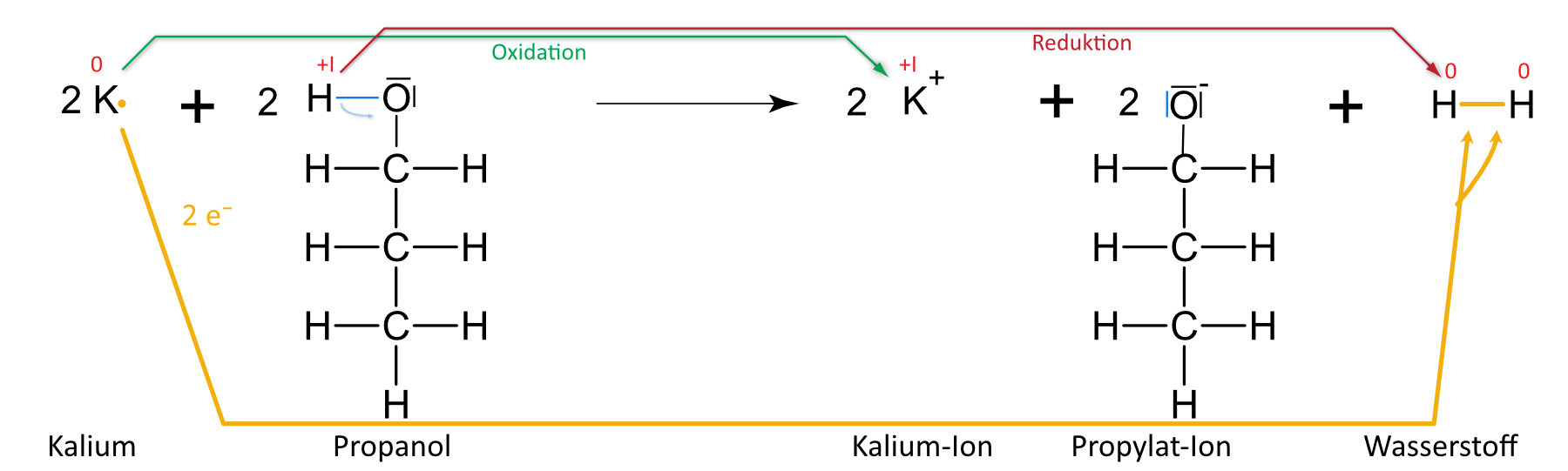
Kalium und Propanol
{slider title="Lösung" open="false" class="icon"}
{/sliders}