Schwefelsäure
-
02 Gleichgewichte
Was du auf dieser Seite lernst
Konzentrierte Schwefelsäure ist hygroskopisch – sie nimmt begierig Wasser aus der Luft auf. Auf dieser Seite untersuchst du, wie sich dabei ein dynamisches Gleichgewicht einstellt, und lernst die zweistufige Protolyse der Schwefelsäure mit Wasser kennen.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säure-Base-Reaktionen und der Bronsted-Definition hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9)
2.1 Schwefelsäure – Wasserdampf – Gleichgewicht
a) konzentrierte Schwefelsäure (H2SO4)
- enthält Schwefelsäuremoleküle
- zeichnet einmal die Strukturformel(n) (unter Berücksichtigung, dass die Edelgas-Regel erfüllt sein muss):
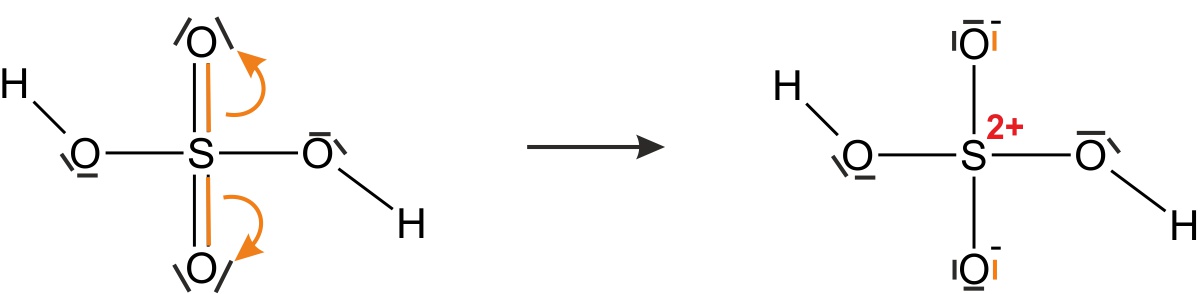
- Konzentrierte Schwefelsäure ist geruchlos.
- Siedetemperatur beträgt 300 °C.
- Konzentrierte Schwefelsäure reagiert heftig mit Wasser unter Ionenbildung (Protolyse-Reaktion).
Formuliert für die Reaktion der Schwefelsäure mit Wasser in zwei Stufen die Reaktionsgleichung in Summenformeln:
Lösung: Reaktionsgleichungen (zweistufige Protolyse)
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O → SO42− + H3O+b) Verdünnte Schwefelsäure
Verdünnte Schwefelsäure enthält folgende Ionen und Moleküle; nennt diese:Lösung: Bestandteile verdünnter Schwefelsäure
- H3O+ (Oxonium-Ion; früher Hydronium-Ion oder „Hydroxonium-Ion")
- HSO4− (Hydrogensulfat-Ion)
- SO42− (Sulfat-Ion; in geringer Konzentration)
- H2O (Wasser; in großer Menge vorhanden)
2.2 Langzeitversuch: Konzentrierte Schwefelsäure
Versuchsdurchführung: In einen Zylinder 1 werden 100 ml konzentrierte Schwefelsäure gegeben. In einen Zylinder 2 werden zunächst 900 ml Wasser und dann vorsichtig 100 ml konzentrierte Schwefelsäure gegeben. Beide Zylinder werden mehrere Jahre offen im gleichen Zimmer stehengelassen.
↑ Zum Vergrößern klicken
✕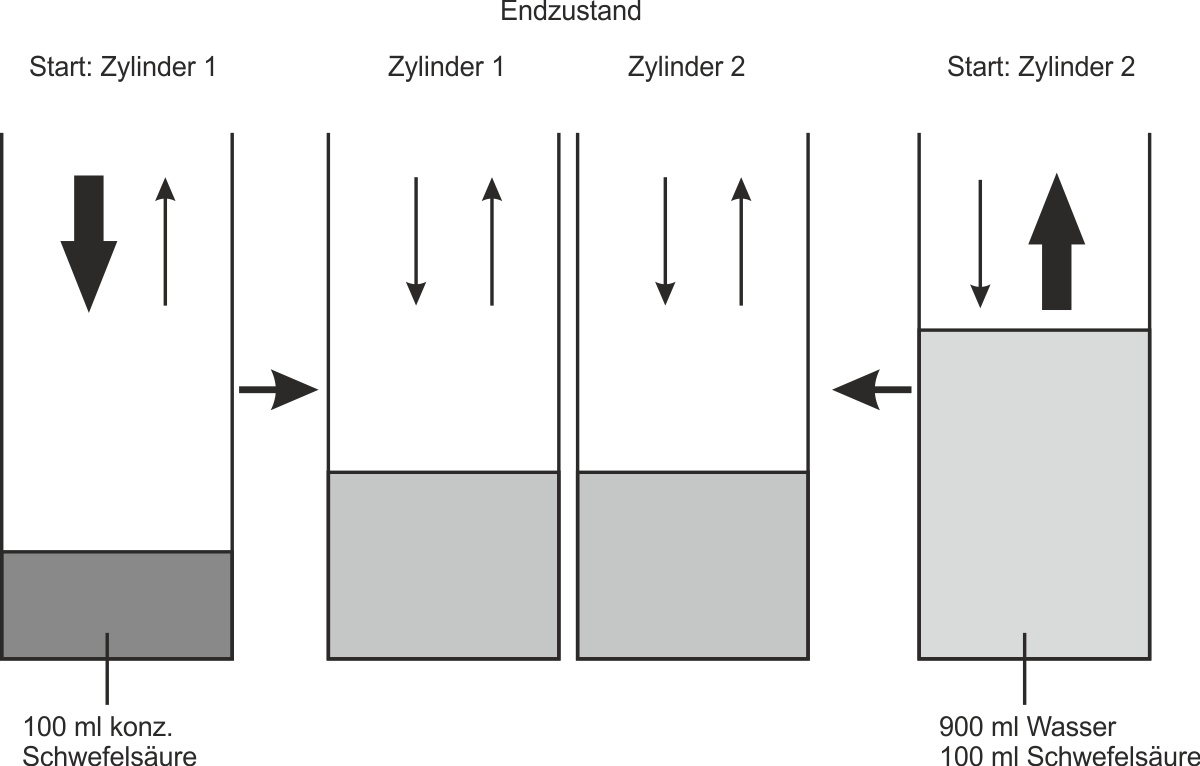
Versucht eine Deutung dieses Versuchs:
Lösung: Deutung des Langzeitversuchs
- Zylinder 1 (konz. H2SO4) nimmt mehr H2O-Moleküle aus der Umgebungsluft auf, als er abgibt.
- Zylinder 2 (verdünnte H2SO4) gibt mehr H2O-Moleküle an die Umgebungsluft ab, als er aufnimmt.
- Nach einigen Jahren hat sich ein Gleichgewichtszustand eingestellt: Pro Zeiteinheit werden gleich viele H2O-Moleküle an die Umgebung abgegeben wie H2O-Moleküle in die Lösung aufgenommen werden.
Auf einen Blick – die wichtigsten Aussagen
Hygroskopie
Konzentrierte H2SO4 ist hygroskopisch – sie zieht Wasser aus der Luft an. Je konzentrierter die Lösung, desto stärker diese Eigenschaft.
Dynamisches Gleichgewicht
Im Gleichgewicht sind Auf- und Abgabe von H2O-Molekülen gleich groß – es herrscht mikroskopische Aktivität bei makroskopischer Konstanz.
Zweistufige Protolyse
H2SO4 gibt in zwei Stufen je ein Proton ab. Im zweiten Schritt ist HSO4− eine schwächere Säure als H2SO4.
Siedepunkt 300 °C
Der hohe Siedepunkt von 300 °C erklärt sich durch starke zwischenmolekulare Kräfte (Wasserstoffbrücken und van-der-Waals-Kräfte).
Häufige Fragen – Schwefelsäure-Gleichgewicht
Was bedeutet „hygroskopisch" und warum ist konzentrierte Schwefelsäure so wassergierig?
Als hygroskopisch bezeichnet man Stoffe, die Wasser aus der Umgebungsluft aufnehmen. Konzentrierte H2SO4 reagiert heftig mit Wasser unter starker Wärmefreisetzung (Protolyse). Da diese Reaktion sehr exotherm ist, liegt das Gleichgewicht stark auf der Seite der Produkte – die Säure „zieht" Wassermoleküle regelrecht aus der Luft, bis sich ein dynamisches Gleichgewicht eingestellt hat.
Warum gibt verdünnte Schwefelsäure Wasser an die Luft ab, konzentrierte aber nicht?
Der entscheidende Faktor ist der Wasserdampfdruck der Lösung. Verdünnte Schwefelsäure hat einen höheren Wasserdampfdruck als die Umgebungsluft → H2O-Moleküle verdunsten. Konzentrierte H2SO4 hat dagegen einen sehr niedrigen Wasserdampfdruck → sie nimmt Wasser auf. Im Langzeitversuch gleichen sich beide Zylinder auf einen gemeinsamen Gleichgewichtszustand an. Mehr dazu auf der Seite Verschiebung des Gleichgewichts.
Was ist ein chemisches Gleichgewicht und woran erkennt man es?
Ein chemisches Gleichgewicht liegt vor, wenn Hin- und Rückreaktion gleich schnell ablaufen. Äußerlich scheint die Reaktion zum Stillstand gekommen zu sein (makroskopische Konstanz), auf molekularer Ebene laufen aber ständig beide Richtungen ab (dynamisches Gleichgewicht). Im Langzeitversuch erkennt man das Gleichgewicht daran, dass sich die Füllhöhen der Zylinder nicht mehr verändern. Weitere Merkmale findest du auf der Seite Merkmale eines chemischen Gleichgewichts.
Wie läuft die zweistufige Protolyse der Schwefelsäure mit Wasser ab?
H2SO4 ist eine zweiprotonige Säure und gibt ihre Protonen in zwei Schritten ab:
1. Stufe (vollständig):
H2SO4 + H2O → HSO4− + H3O+2. Stufe (unvollständig):
HSO4− + H2O ⇌ SO42− + H3O+Da HSO4− eine schwächere Säure ist, läuft die zweite Stufe nicht vollständig ab → daher enthält verdünnte Schwefelsäure sowohl SO42−- als auch HSO4−-Ionen. Die Grundlagen zur Protolyse hast du in der 9. Klasse kennengelernt: Bronsted-Definition (Kl. 9).
Warum darf man niemals Wasser zu konzentrierter Schwefelsäure geben?
Die Reaktion von konz. H2SO4 mit Wasser ist stark exotherm. Gibt man Wasser zu Säure, kann sich das Wasser an der Oberfläche spontan in Dampf verwandeln, was zu einem explosionsartigen Verspritzen der Säure führt. Richtig ist daher: immer Säure langsam in Wasser geben, nie umgekehrt! Die thermodynamischen Hintergründe (Reaktionsenthalpie) findest du in der Einheit Enthalpie H (Energetik).
Lernkarten – Schwefelsäure-Gleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeutet „hygroskopisch" und welcher bekannte Stoff zeigt diese Eigenschaft besonders stark?
Hygroskopisch = Wasser aus der Luft aufnehmend. Konzentrierte H2SO4 ist ein typisches Beispiel: Sie kann sogar organische Stoffe durch Wasserentzug verkohlen.
2Nenne die vier Teilchenarten, die in verdünnter Schwefelsäure vorhanden sind.
H3O+ (Oxonium-Ion) · HSO4− (Hydrogensulfat-Ion) · SO42− (Sulfat-Ion, wenig) · H2O (viele Wassermoleküle)
3Was passiert mit Zylinder 1 (konz. H2SO4) und Zylinder 2 (verd. H2SO4) im Langzeitversuch?
Zylinder 1 nimmt H2O auf → Füllstand steigt. Zylinder 2 gibt H2O ab → Füllstand sinkt. Nach Jahren: gleiche Konzentration → dynamisches Gleichgewicht.
4Schreibe die zweistufige Protolyse von H2SO4 mit Wasser auf.
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O ⇌ SO42− + H3O+
(Stufe 1 vollständig, Stufe 2 unvollständig)5Berechne die Stoffmenge H2SO4 in 100 ml konz. Schwefelsäure (ρ = 1,84 g/ml; w = 98 %; M = 98 g/mol).
m(Lösung) = 100 ml · 1,84 g/ml = 184 g
m(H2SO4) = 184 g · 0,98 = 180,3 g
n = 180,3 g ÷ 98 g/mol ≈ 1,84 molWeiter im Kapitel Gleichgewichtsreaktionen
← Calciumhydroxid-Gleichgewicht → Modellexperiment: Stechheberversuch
🔁 Verwandte Seiten: Merkmale eines chemischen Gleichgewichts · Prinzip von Le Chatelier · Brønsted-Definition (Kl. 9)
-
5 Stärke von Säuren und Basen
5 Stärke von Säuren und Basen - Säurestärke und Molekülstruktur
Hinweis 1: Das Kapitel stammt aus dem Oberstufenbereich. Ich halte es für das Verständnis für Säure-Base-Reaktionen wichtig, weil man sonst bei einer Reaktion mit zwei Ampholyten (z.B. Wasser und Ammoniak) gar nicht weiß, wer die Säure ist und wer als Base funktioniert.
Hinweis 2: Auch hier ist es von Vorteil, wenn man ein Periodensystem der Elemente zur Hand hat.
Brønsted-Theorie:
Säurestärke ist die Tendenz Protonen abzugeben.
Basenstärke Tendenz Protonen aufzunehmen.Bsp. HCl + H₂O → H₃O⁺ + Cl⁻
Säure 1 Base 2 Säure 2 Base 1Info: Supersäuren = Säuren die stärker als H₂SO₄ sind.
Je stärker die Säure desto schwächer die konjugierte (korrespondierende) Base.
5.1 Binäre Säuren.
Faktoren für Säurestärke von Bedeutung:
- Elektronegativität (innerhalb einer Periode)
- Atomgröße (innerhalb einer Gruppe)
a) innerhalb einer Periode (binäre H-Verbindungen)
Säurestärke nimmt mit der EN zu (Atomgrößenunterschiede sind „zu“ gering)
⇨ Elektronen werden stärker dem H-Atom entzogen ⇨ erleichterte Protonenabspaltung.Bsp.:
2. Periode:
Zunahme der EN: N < O < F
Zunahme der Säurestärke NH₃ < H₂O < HF
Gegenüber Wasser Base Säure
3. Periode
Zunahme der EN: P < S < Cl
Zunahme der Säurestärke PH₃ < H₂S < HCl
b) innerhalb einer Gruppe (binäre H-Verbindungen):
Säurestärke nimmt mit der Atomgröße zu (stärkere Auswirkung als Elektronegativität)
⇨ bei einem großen Atom ist die Valenzelektronenwolke auf einem größeren Raum verteilt ⇨ H⁺ ist weniger fest gebunden.H₂O < H₂S < H₂Se < H₂Te
HF < HCl < HBr < HI5.2 Oxosäuren
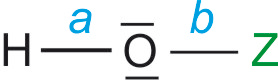
Sauerstoff hat in etwa die gleiche Größe
a) EN von Z ist entscheidend.
Je größer die EN von Z, desto stärker ist die Säure (-I-Effekt).HOI < HOBr < HOCl
hyopoiodige Säure hypobromige hypochlorige Säureb) An Z sind weitere O-Atome gebunden ⇨ stärkerer –I-Effekt (bzw. höhere Formalladung am Z. )
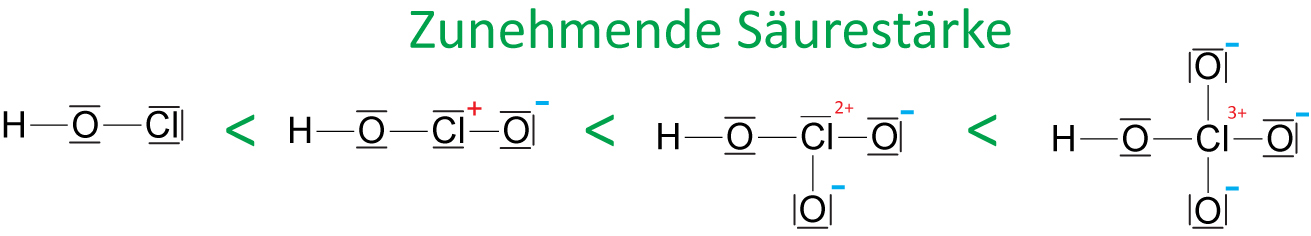
hypochlorige – chlorige – Chlor – Perchlorsäuren
⇨ Man kann Säurestärke abschätzen: Je mehr mehr O-Atome an das Z-Atom jedoch nicht an H-Atom gebunden sind, desto die Säure:
H-O-NO < H-O-NO₂
salpetrige Säure Salpetersäure
(H-O-)₂SO < (H-O-)₂SO₂
schweflige Säure Schwefelsäure
