Was du auf dieser Seite lernst
Du lernst, wie die Neutralisationsenthalpie mithilfe eines Kalorimeters experimentell bestimmt wird und welche Formel dabei verwendet wird. Im zweiten Teil erfährst du, wie sich die Lösungsenthalpie aus Gitterenthalpie und Hydrationsenthalpie zusammensetzt – mit konkreten Beispielen für NaCl, KNO₃, CaCl₂ und NaOH.
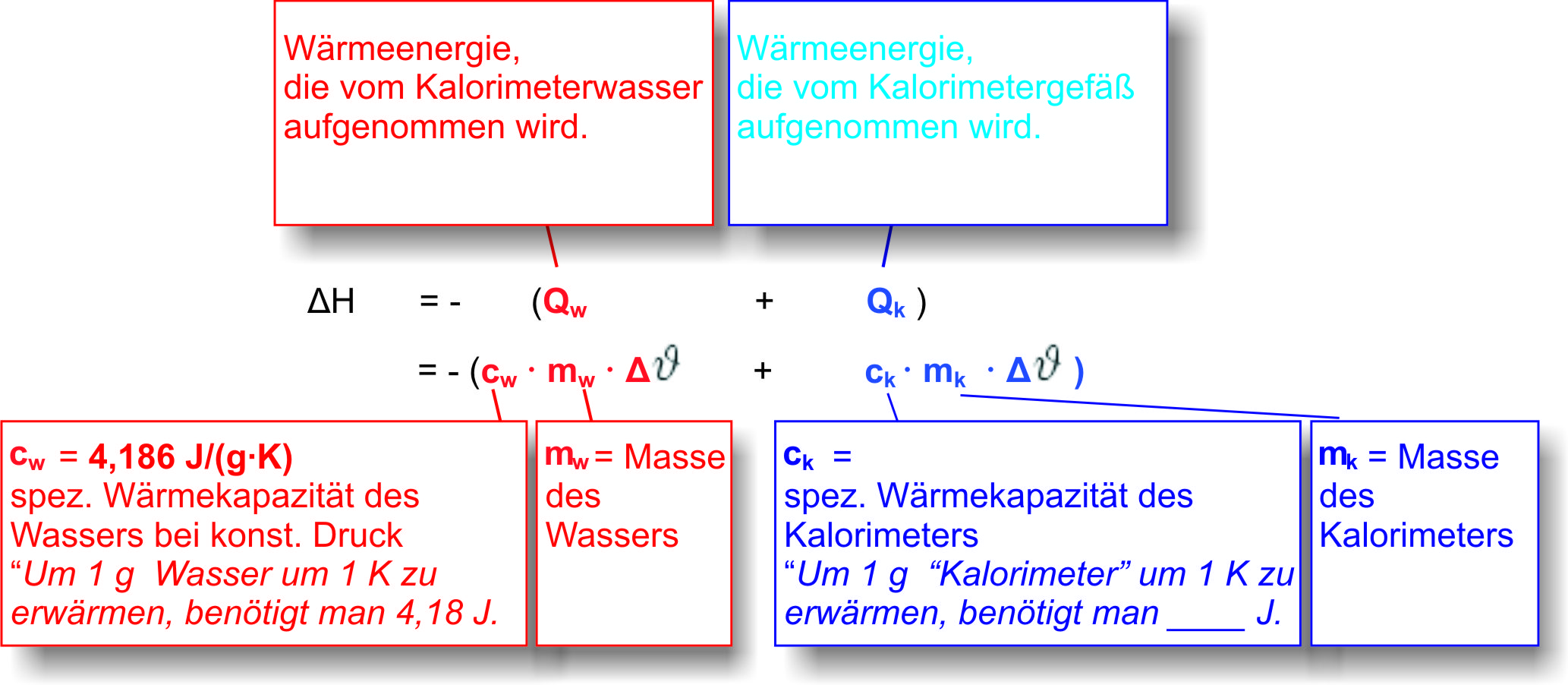
7.2 Bestimmung der Neutralisationsenthalpie
→ vgl. Experiment und Arbeitsblatt:
↑ Zum Vergrößern klicken
✕
Lösungsenthalpien
vgl. dazu Experimente im Unterricht und Arbeitsblätter
Der beim Lösen beobachtete Temperatureffekt hängt von zwei Faktoren ab:
- der aufzubringenden Gitterenergie: Die entgegengesetzt geladenen Ionen im Kristall müssen voneinander getrennt werden.
- der freiwerdenden Hydrationsenthalpie (Solvatationsenthalpie)
Lösungsenthalpie = Gitterenthalpie + Solvationsenthalpie
ΔHsolv = ΔHL + ΔHhyd
Lösungswärme = Gitterenergie + Hydrationsenergie
⚠️ Hinweis zur NaCl-Rechnung: Die Notation „(-851 + 77 kJ/mol)" im Original gibt die Summe der Hydrationsenthalpien der Einzelionen an (Na⁺ und Cl⁻ getrennt aufgeführt). Diese Werte weichen von gängigen Tabellenwerken ab und sollten mit dem aktuellen Unterrichtsmaterial abgeglichen werden.
Lösungsenthalpie NaCl in Wasser:
ΔHsolv = (+778 kJ/mol) + (−851 + 77 kJ/mol) = +4 kJ/mol (25 °C)
Die Lösung kühlt sich leicht ab (endothermer Vorgang).
Kaliumnitrat (KNO₃):
ΔHsolv = +34,9 kJ/mol (nach Atkins »Alles Chemie«: +23,8 kJ/mol)
Calciumchlorid (CaCl₂):
ΔHsolv = −82,98 kJ/mol (nach Atkins »Alles Chemie«: −81,3 kJ/mol)
Die Lösung erwärmt sich, die Lösungsenthalpie ist daher negativ. Der Literaturwert beträgt −83 kJ/mol.
Natriumhydroxid (NaOH):
ΔHsolv = −44,5 kJ/mol (nach Atkins »Alles Chemie«)
Auf einen Blick – die wichtigsten Aussagen
Kalorimeterformel
Die freigesetzte Wärme Q = m · c · ΔT gibt die Neutralisationswärme an. Daraus berechnet sich die molare Neutralisationsenthalpie ΔHN.
Lösungsenthalpie
ΔHsolv = ΔHL + ΔHhyd · Wenn |ΔHhyd| > |ΔHL|, ist die Reaktion exotherm (z. B. CaCl₂).
Gitterenthalpie
Die Gitterenthalpie ist stets positiv (endotherm): Energie wird benötigt, um die Ionenbindungen im Kristall aufzubrechen.
Hydrationsenthalpie
Die Hydrationsenthalpie ist stets negativ (exotherm): Wasser-Dipole lagern sich an die Ionen an und geben Energie frei.
Häufige Fragen zur Neutralisations- und Lösungsenthalpie
Was versteht man unter der Neutralisationsenthalpie?
Die Neutralisationsenthalpie ΔHN ist die Enthalpieänderung, die bei der vollständigen Neutralisation einer starken Säure mit einer starken Base (je 1 mol H⁺ + OH⁻ → H₂O) auftritt. Sie beträgt für starke Säure/Base-Paare stets ca. −57,3 kJ/mol, da in beiden Fällen vollständige Dissoziation vorliegt und immer dieselbe Reaktion H⁺ + OH⁻ → H₂O abläuft.
Wie wird die Neutralisationsenthalpie im Kalorimeter bestimmt?
Man misst die Temperaturerhöhung ΔT, die bei der Reaktion entsteht. Mit der Kalorimeterformel Q = m · c · ΔT (m = Masse der Lösung, c = spez. Wärmekapazität ≈ 4,18 J/(g·K)) berechnet man die freigesetzte Wärme Q. Aus Q und der Stoffmenge n folgt die molare Enthalpie: ΔHN = −Q / n. Das negative Vorzeichen zeigt an, dass das System Wärme abgibt (exotherme Reaktion).
→ Mehr zu Kalorimetrie: 7. Kalorimetrie
Was ist der Unterschied zwischen Gitterenthalpie und Hydrationsenthalpie?
Die Gitterenthalpie ΔHL (immer positiv/endotherm) ist die Energie, die aufgewendet werden muss, um den Ionenkristall in seine gasförmigen Einzelionen zu zerlegen. Die Hydrationsenthalpie ΔHhyd (immer negativ/exotherm) ist die Energie, die beim Anlagerung von Wassermolekülen an die Ionen frei wird. Das Vorzeichen der Lösungsenthalpie hängt davon ab, welcher Beitrag überwiegt.
Warum löst sich CaCl₂ exotherm, NaCl aber fast atherm?
Bei CaCl₂ ist die Hydrationsenthalpie (Ca²⁺ ist zweifach geladen → sehr stark hydratisiert) deutlich größer als die Gitterenthalpie: ΔHsolv ≈ −83 kJ/mol. Die Lösung erwärmt sich spürbar. Bei NaCl gleichen sich Gitterenthalpie (+786 kJ/mol) und Hydrationsenthalpie (ca. −782 kJ/mol) fast aus: ΔHsolv ≈ +4 kJ/mol. Der Temperatureffekt ist minimal und schwach endotherm.
Warum weichen experimentelle Werte vom Literaturwert ab?
Im einfachen Schulversuch gibt es mehrere Fehlerquellen: Das Kalorimeter ist nicht ideal wärmeisoliert (Wärmeverlust an die Umgebung), die spezifische Wärmekapazität der Lösung weicht von der des reinen Wassers ab, und die Wärmekapazität des Kalorimetergefäßes selbst wird oft vernachlässigt. Eine Wärmekapazitätskorrektur (Kalorimeterkorrektur) verbessert die Genauigkeit erheblich. → Vgl. 6. Wärmekapazität
Lernkarten – Neutralisations- und Lösungsenthalpie
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist die Neutralisationsenthalpie und welchen Wert hat sie für starke Säuren und Basen?
ΔHN = Enthalpieänderung bei H⁺ + OH⁻ → H₂O.
Für starke Säure/Base: −57,3 kJ/mol (exotherm, da vollständige Dissoziation).
Wie lautet die Kalorimeterformel zur Berechnung der Reaktionswärme Q?
Q = m · c · ΔT
m = Masse der Lösung (g)
c = spez. Wärmekapazität (≈ 4,18 J/(g·K))
ΔT = Temperaturänderung (K)
Wie setzt sich die Lösungsenthalpie zusammen? Nenne Formel und Vorzeichen der Beiträge.
ΔHsolv = ΔHL + ΔHhyd
Gitterenthalpie ΔHL: positiv (endotherm)
Hydrationsenthalpie ΔHhyd: negativ (exotherm)
CaCl₂ löst sich stark exotherm, KNO₃ stark endotherm. Erkläre das mithilfe der Lösungsenthalpie.
CaCl₂: ΔHhyd ≫ ΔHL → ΔHsolv sehr negativ (−83 kJ/mol).
KNO₃: ΔHL ≫ |ΔHhyd| → ΔHsolv positiv (+35 kJ/mol).
🔢 Berechnung: Beim Lösen von 0,1 mol KNO₃ steigt die Temperatur von 25,0 °C auf 22,5 °C (m = 100 g). Bestimme Q und ΔHsolv.
Q = 100 g · 4,18 J/(g·K) · (−2,5 K) = −1045 J (Wärme wird dem Wasser entzogen)
ΔHsolv = −Q/n = +1045 J / 0,1 mol = +10,45 kJ/mol
(endotherm → plausibel für KNO₃)
Weiter im Kapitel Energetik
← 7. Kalorimetrie → 8. Enthalpie H 6. Wärmekapazität 5. Reaktionswärme Q 8.3 Standardbildungsenthalpie
