Was du auf dieser Seite lernst
Warum ist Salzsäure stärker als Flusssäure, obwohl Fluor elektronegativer ist? Und warum sind Perchlorsäure und Salpetersäure so viel stärker als die entsprechenden Hypo-Säuren? Auf dieser Seite lernst du, welche Faktoren – Elektronegativität, Atomgröße, -I-Effekt und mesomerer Effekt – die Stärke von Säuren bestimmen, und vergleichst Salzsäure mit Essigsäure quantitativ.
Grundlagen aus der 9. Klasse
Das Brønsted-Konzept – Säure als Protonendonator, Base als Protonenakzeptor, konjugiertes Säure-Base-Paar – kennst du bereits aus der 9. Klasse: → Brønsted-Definition (Kl. 9) · → Mehrprotonige Säuren (3.4)
3.5 Stärke von Säuren und Basen
Brønsted-Theorie:
Säurestärke ist die Tendenz, Protonen abzugeben.
Basenstärke ist die Tendenz, Protonen aufzunehmen.
| HCl | + | H₂O | ⇌ | H₃O⁺ | + | Cl⁻ |
| Säure 1 | Base 2 | Säure 2 | Base 1 |
Je stärker die Säure, desto schwächer die konjugierte (korrespondierende) Base.
3.5.1 Säurestärke und Molekülstruktur
A) Säuren, an denen H-Atome nicht an O-Atome gebunden sind
Faktoren für die Säurestärke von Bedeutung:
- Elektronegativität (innerhalb einer Periode)
- Atomgröße (innerhalb einer Gruppe)
a) Innerhalb einer Periode (binäre H-Verbindungen):
Säurestärke nimmt mit der EN zu (Atomgrößenunterschiede sind zu gering).
⇨ Elektronen werden stärker dem H-Atom entzogen ⇨ erleichterte Protonenabspaltung.
| 2. Periode | Zunahme EN: | N | < | O | < | F |
| Zunahme Säurestärke: | NH₃ | < | H₂O | < | HF | |
| Gegenüber Wasser: | Base | Säure | ||||
| 3. Periode | Zunahme EN: | P | < | S | < | Cl |
| Zunahme Säurestärke: | PH₃ | < | H₂S | < | HCl |
b) Innerhalb einer Gruppe (binäre H-Verbindungen):
Säurestärke nimmt mit der Atomgröße zu (stärkerer Einfluss als Elektronegativität).
⇨ Bei einem großen Atom ist die Valenzelektronenwolke auf einem größeren Raum verteilt ⇨ H⁺ ist weniger fest gebunden.
| 6. Gruppe: | H₂O | < | H₂S | < | H₂Se | < | H₂Te |
| 7. Gruppe: | HF | < | HCl | < | HBr | < | HI |
B) Oxosäuren
↑ Zum Vergrößern klicken
✕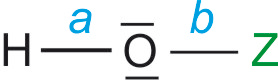
Sauerstoff hat in etwa die gleiche Größe.
a) EN von Z ist entscheidend.
Je größer die EN von Z, desto stärker ist die Säure (–I-Effekt).
| HOI | < | HOBr | < | HOCl |
| hypoiodige Säure | hypobromige Säure | hypochlorige Säure |
b) An Z sind weitere O-Atome gebunden ⇨ stärkerer –I-Effekt (bzw. höhere Formalladung am Z).
↑ Zum Vergrößern klicken
✕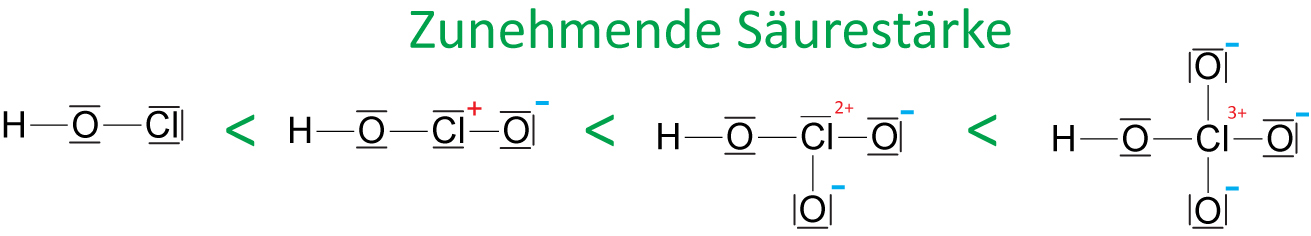
hypochlorige Säure < chlorige Säure < Chlorsäure < Perchlorsäure
⇨ Man kann Säurestärke abschätzen: Je mehr O-Atome an das Z-Atom, jedoch nicht an H gebunden sind, desto stärker die Säure:
| H–O–N=O | < | H–O–NO₂ |
| salpetrige Säure | Salpetersäure | |
| (H–O–)₂S=O | < | (H–O–)₂SO₂ |
| schweflige Säure | Schwefelsäure |
c) Mehrprotonige Säuren:
Für jede Dissoziationsstufe liegt eine eigene Säurekonstante bzw. ein eigener pKS-Wert vor:
| Gleichgewicht | KS | pKS |
|---|---|---|
|
H₃PO₄ + H₂O ⇌ H₂PO₄⁻ + H₃O⁺ Phosphorsäure → Dihydrogenphosphat-Ion |
7,4 · 10⁻³ | 2,13 |
|
H₂PO₄⁻ + H₂O ⇌ HPO₄²⁻ + H₃O⁺ Dihydrogenphosphat-Ion → Hydrogenphosphat-Ion |
6,3 · 10⁻⁸ | 7,20 |
|
HPO₄²⁻ + H₂O ⇌ PO₄³⁻ + H₃O⁺ Hydrogenphosphat-Ion → Phosphat-Ion |
7,4 · 10⁻¹³ | 12,36 |
d) Mesomerer Effekt
+M-Effekt (Mesomerie-Effekt) der Anionen:
↑ Zum Vergrößern klicken
✕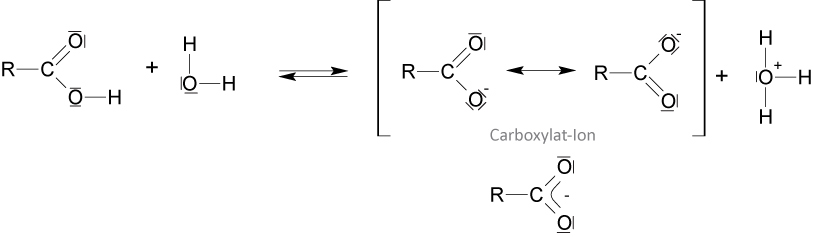
Eine Säure ist umso stärker, je …
… stabiler das gebildete Anion (z. B. durch Hydratation oder Mesomeriestabilisierung).
… instabiler das Säuremolekül an der H-Bindung.
3.6 Vergleich Säurestärke: Salzsäure und Essigsäure
Versuch: pH-Wert-Messung bei gleicher Konzentration (c = 0,1 mol/L):
| Lösung | Beobachtung |
|---|---|
| Salzsäure (c = 0,1 mol/L) | pH = 1 |
| Essigsäure (c = 0,1 mol/L) | pH = 2,9 |
Erklärung:
a) Salzsäure – vollständig protolysiert (Gleichgewicht ganz rechts):
b) Essigsäure – unvollständig protolysiert (Gleichgewicht liegt links):
| HAc | H₃O⁺ | Ac⁻ | |
|---|---|---|---|
| Ausgangszustand | 0,1 mol/L | ≈ 0 | 0 |
| Gleichgewicht | ≈ 0,099 mol/L | 1,6 · 10⁻³ mol/L | 1,6 · 10⁻³ mol/L |
⇨ Gleichgewicht liegt links – nur jedes ~60. HAc-Molekül protolysiert (Protolysegrad ≈ 1,6 %).
Auf einen Blick – die wichtigsten Aussagen
Periode: Elektronegativität
Innerhalb einer Periode nimmt die Säurestärke mit steigender EN zu: NH₃ < H₂O < HF (2. Periode). Die EN bestimmt, wie leicht das Proton abgespalten wird.
Gruppe: Atomgröße
Innerhalb einer Gruppe nimmt die Säurestärke mit der Atomgröße zu: HF < HCl < HBr < HI. Die Valenzelektronenwolke ist weiter verteilt, das H⁺ weniger fest gebunden.
Oxosäuren: –I-Effekt
Je mehr O-Atome an Z (nicht an H) gebunden, desto stärker die Säure: HOCl < HClO₂ < HClO₃ < HClO₄. Jedes zusätzliche O erhöht die Formalladung am Z-Atom.
Mesomerie & Stabilisierung
Je stabiler das konjugierte Anion (Mesomerie, Hydratation), desto stärker die Säure. Essigsäure ist stärker als vergleichbare Alkohole – das Carboxylat-Ion ist mesomeriestabilisiert.
Häufige Fragen – Säurestärke und Molekülstruktur
Warum ist HCl stärker als HF, obwohl Fluor elektronegativer ist?
Innerhalb einer Gruppe überwiegt der Einfluss der Atomgröße gegenüber der Elektronegativität. Das Chloratom ist größer als Fluor – die Valenzelektronenwolke ist weiter ausgedehnt, die H–Cl-Bindung daher schwächer als die H–F-Bindung. Das Proton kann leichter abgespalten werden. Innerhalb einer Periode hingegen ist Atomgrößenunterschied gering, sodass dort die EN dominiert.
Wie erklärt man die unterschiedliche Stärke der Chlorsäuren?
Die Chlorsäuren unterscheiden sich in der Anzahl der O-Atome, die direkt an Cl gebunden sind (aber nicht an H). Jedes zusätzliche Sauerstoffatom zieht über den –I-Effekt Elektronen aus der O–H-Bindung ab und erhöht außerdem die Formalladung am Cl-Atom. Dadurch wird das Proton leichter abgegeben: HOCl (0 zusätzliche O) < HClO₂ (1) < HClO₃ (2) < HClO₄ (3).
Was ist der pKS-Wert und wie hängt er mit der Säurestärke zusammen?
Der pKS-Wert ist der negative dekadische Logarithmus der Säurekonstanten KS: pKS = –lg(KS). Je kleiner der pKS-Wert, desto stärker die Säure. Salzsäure hat pKS ≈ –7 (starke Säure), Essigsäure pKS = 4,75 (schwache Säure). Mehr dazu auf der Seite → pKS-Wert (3.7).
Warum hat Essigsäure (c = 0,1 mol/L) einen pH-Wert von 2,9 statt 1?
Essigsäure ist eine schwache Säure – sie protolysiert nur unvollständig. Bei c = 0,1 mol/L stellen sich im Gleichgewicht nur ca. 1,6 · 10⁻³ mol/L H₃O⁺-Ionen ein (Protolysegrad ≈ 1,6 %). Das entspricht pH ≈ 2,9. Salzsäure dagegen ist vollständig protolysiert: bei gleicher Konzentration liefert jedes HCl-Molekül ein H₃O⁺ → pH = 1.
Warum erhöht Mesomerie des Anions die Säurestärke?
Wenn das nach der Protonenabgabe entstehende Anion durch Mesomerie stabilisiert ist, liegt ein energieärmerer, stabilerer Zustand vor. Das Gleichgewicht der Protolyse verschiebt sich dadurch weiter auf die rechte Seite – die Säure gibt das Proton bereitwilliger ab. Ein typisches Beispiel ist das Carboxylat-Ion (–COO⁻): Die negative Ladung ist gleichmäßig auf beide Sauerstoffatome verteilt, was das Anion gegenüber einem Alkoholat-Ion (R–O⁻, keine Mesomerie) deutlich stabilisiert. Essigsäure (CH₃COOH) ist daher stärker als Ethanol (C₂H₅OH).
Lernkarten – Säurestärke
Klicke auf eine Karte, um die Antwort zu sehen.
Wie ändert sich die Säurestärke binärer H-Verbindungen innerhalb einer Periode? Nenne ein Beispiel.
Sie nimmt mit steigender Elektronegativität zu.
2. Periode: NH₃ < H₂O < HF
NH₃ ist eine Base, HF eine Säure gegenüber Wasser.
Wie ändert sich die Säurestärke innerhalb einer Gruppe? Erkläre den Grund.
Sie nimmt mit steigender Atomgröße zu: HF < HCl < HBr < HI.
Beim größeren Atom ist die Valenzelektronenwolke weiter verteilt → H⁺ weniger fest gebunden → leichtere Abspaltung.
Bringe die Chlorsäuren in die Reihenfolge zunehmender Säurestärke und erkläre das Prinzip.
HOCl < HClO₂ < HClO₃ < HClO₄
Mehr O-Atome an Cl → stärkerer –I-Effekt → höhere Formalladung am Cl → schwächere O–H-Bindung → stärkere Säure.
Warum ist Essigsäure eine stärkere Säure als Ethanol, obwohl beide eine O–H-Gruppe haben?
Das Carboxylat-Ion (CH₃COO⁻) ist mesomeriestabilisiert: Die negative Ladung ist gleichmäßig auf beide O-Atome verteilt. Das Ethanol-Anion (C₂H₅O⁻) hat keine Mesomerie → Essigsäure gibt H⁺ bereitwilliger ab.
Essigsäure: c₀ = 0,1 mol/L, pH = 2,9. Berechne den Protolysegrad α in %.
[H₃O⁺] = 10⁻²·⁹ ≈ 1,26 · 10⁻³ mol/L
α = [H₃O⁺] / c₀ = 1,26 · 10⁻³ / 0,1 = 0,0126
α ≈ 1,3 %
Nur jedes ~77. Molekül protolysiert.
Weiter im Kapitel Säure-Base-Reaktionen
← 3.4 Mehrprotonige Säuren → 3.7 pKS-Wert → Pufferlösungen
🔁 Grundlagen: Brønsted-Definition (Kl. 9) · Mehrprotonige Säuren (3.4)
