2.7 Lewis – Formeln für Moleküle
(= Valenzstrichformeln)
Regeln zum Aufstellen einer Lewis-Formel Teil I:
Für Atome gilt zunächst:
- Man zeichnet an jedes Atom die Außenelektronen als (Valenzelektronen) als Punkte ein. Die Elektronen der inneren Schalen werden nicht berücksichtigt.
- Einfach besetzte „Kugelwolken“ (Orbitale) werden mit einem Punkt, doppelt besetzte „Kugelwolken“ (Orbitale) mit einem Strich symbolisiert.
Ferner gilt für Moleküle
- Die Elementsymbole der Atome werden entsprechend ihrer Verknüpfung im Molekül angeordnet.
- Zwischen den Atomen werden nun so viele bindende Elektronenpaare gebildet, dass alle Atome die Edelgasregel („Oktettregel“) erfüllen (vgl. dazu spätere Seite). Dabei sind Einfach- und Mehrfachbindungen möglich.
- Bindende und nichtbindende Elektronenpaare werden durch einen Strich ersetzt.
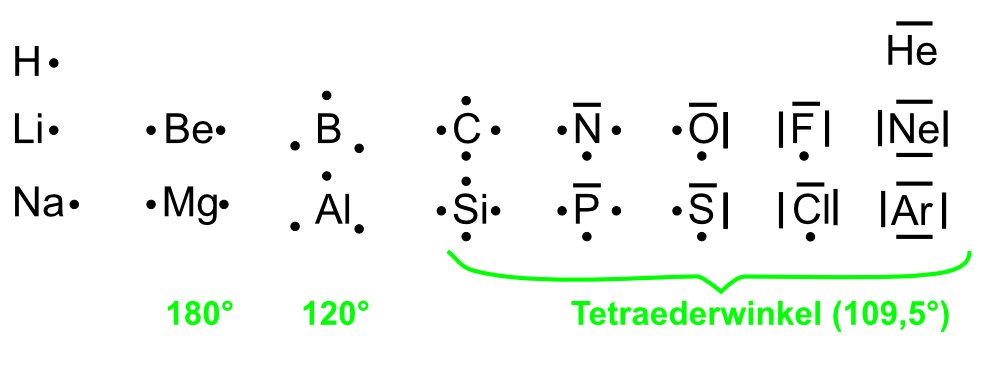
Am Einfachsten versteht man es, wenn man die ersten Elemente der Hauptgruppe zeichnet:
Versucht mal (den Regeln oben folgend) die Lewis-Formeln für die Elemente der ersten drei Perioden zu zeichnen. Wenn ihr nicht weiter kommt, kurz die Lösung aufklappen, dann wieder zuklappen und den Rest machen. Ein Periodensystem wäre recht hilfreich:
{slider title="Lösung" open="false" class="icon"}
Zusammenhang zwischen Lewis-Formel und PSE
{/sliders}