Was du auf dieser Seite findest
Das Kapitel Alkane ist das erste Kapitel der Organischen Chemie in Klasse 10 (Baden-Württemberg). Du lernst die einfachsten Kohlenwasserstoffe kennen: von Methan über Butan bis zur homologen Reihe, Nomenklatur, Eigenschaften und schließlich die radikalische Substitution als ersten organischen Reaktionsmechanismus.
Grundlagen aus der 9. Klasse
Atombindung, Lewis-Formeln und das Konzept der Elektronenpaarbindung hast du in der 9. Klasse kennengelernt: → Atombindung (Kl. 9) · → Lewis-Formeln (Kl. 9)
Unterseiten im Überblick
1.1
Methan
Lewis-Formel · Kugelstabmodell · Verbrennung
1.2 · bei ausreichend Zeit
Ethan
Noch kein eigener Artikel online
1.3 · bei ausreichend Zeit
Propan
Noch kein eigener Artikel online
1.4
Butan
Konstitutionsisomerie · Strukturformeln · Verbrennung
1.5
Homologe Reihe der Alkane
CₙH₂ₙ₊₂ · Strukturformeln C₁–C₁₇ · Siedepunkte
1.6
Genfer Nomenklatur
Hauptkette · Substituenten · Lokanten · → Übungen
1.7
Struktur und Eigenschaften
Einfachbindung · Van-der-Waals-Kräfte · unpolar · hydrophob
1.8
Angriffsfreudige Teilchen
Radikale · Elektrophile · Nucleophile
1.9
Reaktion mit Halogenen
Radikalische Substitution · Start / Kette / Abbruch · Halogenalkane
Vollständige Inhaltsübersicht
- 1.1 Methan – Lewis-Formel, Kugelstabmodell, qualitative Elementaranalyse, Verbrennung
- 1.2 Ethan (bei ausreichend Zeit – noch kein Artikel)
- 1.3 Propan (bei ausreichend Zeit – noch kein Artikel)
- 1.4 Butan – Strukturformeln, Konstitutionsisomerie (n-Butan / Isobutan), Verbrennung
- 1.5 Homologe Reihe der Alkane – allgemeine Formel CₙH₂ₙ₊₂, Strukturformeln C₁–C₁₇, Siedepunkttrend
- 1.6 Genfer Nomenklatur der Alkane – Hauptkette, Substituenten, Lokanten | → Übungen zur Nomenklatur
- 1.7 Struktur und Eigenschaften der Alkane – Einfachbindung, Van-der-Waals-Kräfte, unpolar, Siedepunkte
- 1.8 Angriffsfreudige Teilchen – Radikale, Elektrophile, Nucleophile
- 1.9 Reaktion von Alkanen mit Halogenen – Radikalische Substitution: Start-, Ketten- und Abbruchreaktion, Halogenalkane
Auf einen Blick – Alkane
Homologe Reihe
Alkane haben die allgemeine Formel CₙH₂ₙ₊₂. Jedes folgende Glied der homologen Reihe enthält eine CH₂-Gruppe mehr. Siedepunkt und Schmelzpunkt steigen mit der Kettenlänge.
Eigenschaften
Alkane sind unpolar und reagieren wegen der starken Einfachbindung normalerweise nicht. Zwischen den Molekülen wirken nur Van-der-Waals-Kräfte – daher niedrige Siedepunkte und schlechte Wasserlöslichkeit.
Radikalische Substitution
Alkane reagieren mit Halogenen durch radikalische Substitution (UV-Licht): Start (homolytische Spaltung) → Kettenreaktion (Radikal greift CH-Bindung an) → Abbruch (zwei Radikale verbinden sich).
Genfer Nomenklatur
Regeln: 1. Längste Kette bestimmen. 2. Substituenten von der nächstgelegenen Seite nummerieren. 3. Substituenten alphabetisch benennen. Beispiel: 3-Ethyl-2,2-dimethylhexan.
Häufige Fragen – Alkane
Was ist ein Alkan und was bedeutet „gesättigt"?
Alkane sind Kohlenwasserstoffe, die ausschließlich Einfachbindungen zwischen Kohlenstoffatomen besitzen. Die allgemeine Formel lautet CₙH₂ₙ₊₂. „Gesättigt" bedeutet, dass jedes C-Atom die maximale Anzahl an H-Atomen trägt – es gibt keine Doppel- oder Dreifachbindungen, an die weitere Atome addiert werden könnten. Beispiele: Methan CH₄, Ethan C₂H₆, Propan C₃H₈.
Warum steigt der Siedepunkt in der homologen Reihe der Alkane?
Mit zunehmender Kettenlänge steigt die Moleküloberfläche, über die Van-der-Waals-Kräfte wirken. Mehr Kontaktfläche bedeutet stärkere intermolekulare Anziehung – daher muss mehr Energie aufgewendet werden, um die Moleküle voneinander zu trennen, was sich in einem höheren Siedepunkt zeigt. → Homologe Reihe
Was sind die drei Schritte der radikalischen Substitution?
1. Startreaktion: UV-Licht spaltet Cl₂ homolytisch in zwei Chlorradikale (Cl•).
2. Kettenreaktion: Cl• greift CH₄ an → HCl + CH₃•; CH₃• reagiert mit Cl₂ → CH₃Cl + Cl• (Kette läuft weiter).
3. Abbruchreaktion: Zwei beliebige Radikale verbinden sich zu einem stabilen Molekül – die Kette bricht ab.
Das Verhältnis der Produkte (Mono-, Di-, Trichlormethan …) hängt von den Bedingungen ab.
→ Radikalische Substitution
Was ist der Unterschied zwischen Elektrophilen, Nucleophilen und Radikalen?
Elektrophile sind elektronenarme Teilchen, die Elektronenpaare suchen (Lewis-Säuren).
Nucleophile sind elektronenreiche Teilchen mit freien Elektronenpaaren (Lewis-Basen).
Radikale sind Teilchen mit einem ungepaarten Elektron; sie entstehen durch
homolytische Bindungsspaltung (z. B. durch UV-Licht) und sind besonders reaktiv.
→ Angriffsfreudige Teilchen
Wie benennt man verzweigte Alkane nach der Genfer Nomenklatur?
Schrittweise Vorgehensweise:
1. Längste durchgehende Kohlenstoffkette = Hauptkette → gibt den Stammnamen.
2. Nummerierung: von der Seite beginnen, die den ersten Substituenten mit der
kleinsten Zahl ergibt.
3. Substituenten: Alkylgruppen mit Lokant und Namen (z. B. 2-Methyl-).
Mehrere gleiche: di-, tri-, tetra-. Alphabetische Reihenfolge bei verschiedenen.
Beispiel: 3-Ethyl-2,2-dimethylhexan.
→ Genfer Nomenklatur
Lernkarten – Alkane
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist die allgemeine Summenformel der Alkane? Gib drei Beispiele an.
Allg. Formel: CₙH₂ₙ₊₂
Methan: CH₄ (n = 1)
Ethan: C₂H₆ (n = 2)
Propan: C₃H₈ (n = 3)
→ Gesättigte Kohlenwasserstoffe
Was sind Van-der-Waals-Kräfte und welche Auswirkung haben sie auf Alkane?
Schwache Dispersionskräfte zwischen unpolaren Molekülen.
→ Alkane: niedrige Siedepunkte
→ Schlecht löslich in Wasser
→ Siedepunkt steigt mit Kettenlänge (mehr Kontaktfläche)
Was versteht man unter Konstitutionsisomerie? Erkläre am Beispiel Butan.
Gleiche Summenformel, verschiedene Verknüpfung der Atome.
C₄H₁₀: n-Butan (gerade Kette)
und 2-Methylpropan / Isobutan (verzweigt)
→ unterschiedliche Siedepunkte!
Was entsteht bei der vollständigen Verbrennung von Alkanen?
Vollständige Verbrennung (Oxidation):
Alkan + O₂ → CO₂ + H₂O
Beispiel Methan:
CH₄ + 2 O₂ → CO₂ + 2 H₂O (ΔH < 0)
→ Exotherme Reaktion
Benenne: CH₃–CH(CH₃)–CH₂–CH₂–CH₃ nach Genfer Nomenklatur.
Längste Kette: 5 C → Pentan
Methylgruppe an C2 → 2-Methylpentan
Kontrolle: Nummerierung von links ergibt Lokant 2,
von rechts Lokant 4 → kleinste Zahl = 2 ✓
Weiter im Kapitel Organische Chemie
← Klasse 10 – Übersicht → 2 Alkene
🔁 Grundlagen (Kl. 9):
Atombindung ·
Lewis-Formeln
📚 Vertiefung Kursstufe:
Cycloalkane ·
Aromaten
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Methan (CH₄) ist das einfachste Alkan und gleichzeitig der Einstieg in die Organische Chemie. Du lernst, wie man über die qualitative Elementaranalyse auf die Summenformel schließt, wie die Strukturformel und der Bindungswinkel aussehen, und warum die Verbrennung von Methan eine Redoxreaktion ist.
Grundlagen aus der 9. Klasse
Lewis-Formeln, Atombindung und Oxidationszahlen hast du in der 9. Klasse kennengelernt: → Lewis-Formeln (Kl. 9) · → Oxidationszahlen (Kl. 9)
1.1.1 Vorkommen
Methan kommt vor in: Erdgas, Sumpfgas, Biogas, Grubengas.
1.1.2 Eigenschaften
- farb- und geruchloses Gas
- geringere Dichte als Luft
- brennbar
1.1.3 Ermittlung der Summenformel (Molekülformel) und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
Hierfür wird der zu untersuchende Stoff verbrannt und die Verbrennungsprodukte bestimmt.
Bildet sich Wasser, ist Wasserstoff als Element vorhanden.
Kohlenstoff lässt sich als Ruß (unvollständige Verbrennung)
oder als Kohlenstoffdioxid nachweisen.
Der CO₂-Nachweis erfolgt mit der Kalkwasserprobe:
Das entstandene Gas wird in Kalkwasser eingeleitet –
eine Trübung zeigt CO₂ an.
↑ Zum Vergrößern klicken
✕
- Nachweis von Wasserstoff → Bildung von Wasser → WaTesMo-Papier oder wasserfreies Kupfersulfat.
- Nachweis von C → Bildung von CO2 → Nachweis als CaCO3:
Ca(OH)2 (aq) + CO2 (g) → CaCO3 (s) + H2O (l)
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bestimmung der molaren Masse
Mit der Gaswägung lässt sich die molare Masse von Methan bestimmen:
M(Methan) = 16 g/mol · Molekülmasse 16 u.
c) Summenformel: CH4
d) Strukturformel
Man zeichnet Methan meist mit einem Winkel von 90°. Dieser Winkel entspricht nicht
dem tatsächlichen Bindungswinkel (vgl. unten). Man kann sich aber vorstellen, dass man
direkt auf das Molekül blickt.
↑ Zum Vergrößern klicken
✕ ✕
✕
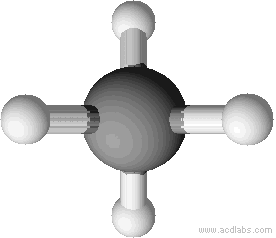
Tetraedrische Anordnung der Wasserstoffatome um das Kohlenstoffatom (Bindungswinkel 109,5°). Erklärung: größtmögliche Entfernung der Wasserstoffatome.
1.1.4 Vollständige Verbrennung
0 −IV +I +IV −II +I −II
2 O2 + CH4 → CO2 + 2 H2O ΔH = −888 kJ/mol
↑ Zum Vergrößern klicken
✕
Hinweis: Wenn die Ermittlung der Oxidationszahlen Schwierigkeiten macht, kann man es hier nochmals nachlesen.
1 l Methan benötigt zur vollständigen Verbrennung 10 Liter Luft (2 l Sauerstoff).
Auf einen Blick – Methan
Summenformel
Methan: CH₄ · molare Masse 16 g/mol · einfachstes Alkan · allg. Formel der Alkane: CₙH₂ₙ₊₂ (hier n = 1).
Tetraeder
Die vier H-Atome ordnen sich tetraedrisch um das C-Atom an. Bindungswinkel: 109,5° (größtmögliche Abstoßung der Bindungselektronenpaare).
Elementaranalyse
Verbrennung → H₂O (Wassernachweis: WaTesMo) + CO₂ (Kalkwasserprobe: Trübung durch CaCO₃) → Methan enthält C und H.
Verbrennung
CH₄ + 2 O₂ → CO₂ + 2 H₂O · ΔH = −888 kJ/mol (exotherm). C wird von −IV auf +IV oxidiert; O von 0 auf −II reduziert.
Häufige Fragen – Methan
Wie weist man experimentell nach, dass Methan Kohlenstoff und Wasserstoff enthält?
Methan wird vollständig verbrannt. Die entstehenden Gase und Dämpfe werden durch zwei Nachweisreagenzien geleitet: Wassernachweis mit wasserfreiem Kupfersulfat (wird blau) oder WaTesMo-Papier (Blaufärbung zeigt Wasser an) → Methan enthält Wasserstoff. CO₂-Nachweis mit Kalkwasser Ca(OH)₂: Trübung durch CaCO₃-Bildung → Methan enthält Kohlenstoff.
Warum ist der Bindungswinkel in Methan 109,5° und nicht 90°?
Die vier bindenden Elektronenpaare stoßen sich gemäß dem VSEPR-Modell (Valence Shell Electron Pair Repulsion) so weit wie möglich ab. Maximale Abstoßung ergibt eine tetraedrische Anordnung mit einem Bindungswinkel von 109,5°. In der vereinfachten Strukturformel zeichnet man 90°-Winkel, weil man so tut, als würde man von oben auf das Molekül blicken.
Warum ist die Verbrennung von Methan eine Redoxreaktion?
Bei der Verbrennung ändert sich die Oxidationszahl des Kohlenstoffs von −IV (in CH₄) auf +IV (in CO₂) → Oxidation. Der Sauerstoff wird von 0 (O₂) auf −II (in CO₂ und H₂O) reduziert → Reduktion. Es findet also ein Elektronenübergang statt: Methan ist das Reduktionsmittel, Sauerstoff das Oxidationsmittel. → Oxidationszahlen (Kl. 9)
Was bedeutet ΔH = −888 kJ/mol bei der Verbrennung?
Das negative Vorzeichen zeigt, dass Energie abgegeben wird – die Reaktion ist exotherm. Pro Mol verbranntem Methan (= 16 g) werden 888 kJ Wärmeenergie freigesetzt. Das erklärt, warum Methan (Erdgas) als Energieträger zum Heizen und Kochen eingesetzt wird. Mehr zur Reaktionsenthalpie: → Enthalpie (Kursstufe)
Wo kommt Methan natürlich vor und warum ist es klimarelevant?
Methan kommt natürlich in Erdgas (Hauptbestandteil), Sumpfgas (Zersetzung organischer Stoffe unter Wasser), Biogas (Gärung) und Grubengas (Steinkohlebergbau) vor. Als Treibhausgas ist CH₄ etwa 25-mal klimawirksamer als CO₂ (bezogen auf 100 Jahre), weil es Infrarotstrahlung besonders effektiv absorbiert.
Lernkarten – Methan
Klicke auf eine Karte, um die Antwort zu sehen.
Gib Summenformel, molare Masse und Bindungswinkel von Methan an.
Summenformel: CH₄
Molare Masse: 16 g/mol
Bindungswinkel: 109,5° (Tetraeder)
Struktur: 4 H-Atome tetraedrisch um C
Wie weist man bei der Elementaranalyse Kohlenstoff und Wasserstoff nach?
H-Nachweis:
WaTesMo-Papier oder CuSO₄ (wasserfrei) → Blaufärbung = H₂O vorhanden
C-Nachweis:
Kalkwasser Ca(OH)₂ → Trübung = CO₂ vorhanden
Stelle die vollständige Verbrennungsgleichung von Methan auf.
CH₄ + 2 O₂ → CO₂ + 2 H₂O
ΔH = −888 kJ/mol (exotherm)
Kontrolle: C: 1=1 ✓ · H: 4=4 ✓ · O: 4=4 ✓
Welche Oxidationszahlen hat Kohlenstoff in CH₄ und in CO₂? Was folgt daraus?
CH₄: C hat Oxidationszahl −IV
CO₂: C hat Oxidationszahl +IV
→ Oxidationszahl steigt → C wird oxidiert
→ Methan = Reduktionsmittel
Wieviel Liter Luft benötigt 1 l Methan zur vollständigen Verbrennung, und warum?
10 Liter Luft (≈ 2 l O₂, da Luft ≈ 21 % O₂)
CH₄ + 2 O₂ → … · Stöchiometrie: 1 Vol. CH₄ : 2 Vol. O₂
Luft enthält ~20 % O₂ → 2 l O₂ stecken in 10 l Luft
Weiter im Kapitel Alkane
← 1 Alkane – Übersicht → 1.4 Butan → 1.5 Homologe Reihe
🔁 Grundlagen (Kl. 9):
Lewis-Formeln ·
Oxidationszahlen
📚 Vertiefung Kursstufe:
Enthalpie ΔH
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Butan (C₄H₁₀) ist das erste Alkan, das in zwei verschiedenen Strukturen vorkommt. Du lernst den zentralen Begriff der Konstitutionsisomerie kennen, verstehst warum n-Butan und Isobutan verschiedene Siedepunkte haben, und übst die Halbstrukturformel als platzsparende Schreibweise.
Grundlagen aus 1.1 Methan
Summenformel, Strukturformel und Lewis-Formel hast du am Beispiel Methan kennengelernt: → 1.1 Methan · → Lewis-Formeln (Kl. 9)
Hinweis: 1.2 Ethan und 1.3 Propan werden nur bei ausreichend Zeit besprochen. Da sie ähnlich aufgebaut sind, wird auf einen eigenen Heftaufschrieb verzichtet (vgl. 1.5 Homologe Reihe).
1.4.1 Vorkommen
Im Erdgas; fällt an bei der Benzingewinnung.
1.4.2 Eigenschaften
Farbloses Gas · größere Dichte als Luft · brennbar (Verbrennungsprodukte bei vollständiger Verbrennung: CO2 und H2O) · unter Druck leicht verflüssigbar.
1.4.3 Ermittlung der Summenformel und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
↑ Zum Vergrößern klicken
✕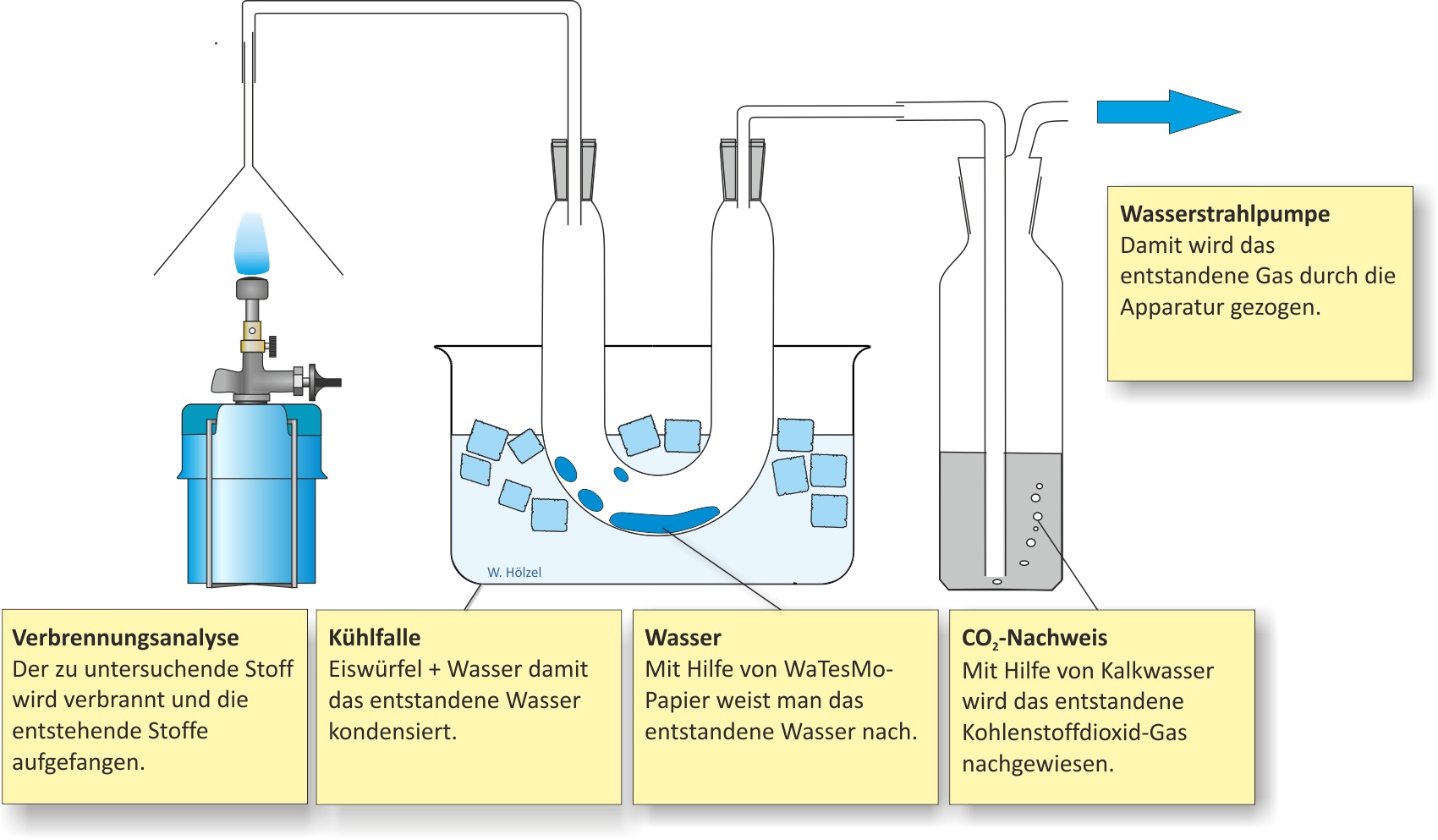
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Butan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bau und Formeln
1. Molare Masse = 58,12 g/mol · Molekülmasse = 58,12 u
2. Summenformel: C4H10
3. Strukturformel – zwei Möglichkeiten:
✕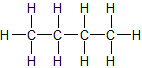 ✕
✕
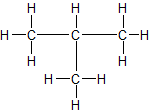
ZMK: nur Van-der-Waals-Kräfte. Bei n-Butan können sich die Moleküle dichter zusammenlagern → stärkere ZMK → etwas höhere Siedetemperatur als Isobutan.
Räumliche Strukturen im Kugelstabmodell (versuche, die Abbildungen n-Butan oder Isobutan zuzuordnen):
✕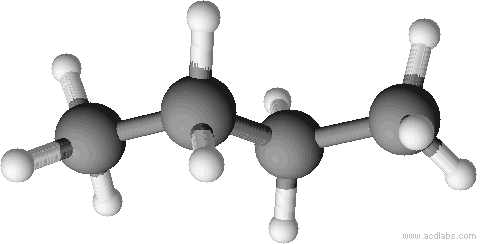 ✕
✕
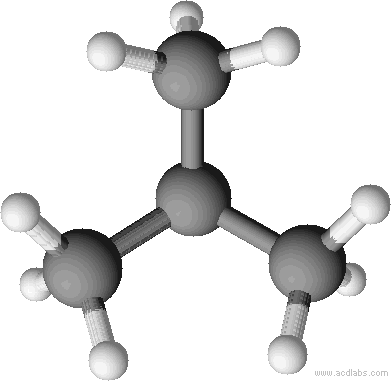
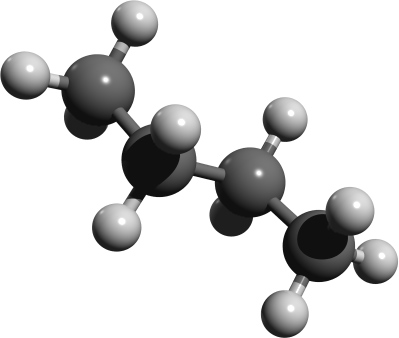
Renderbild n-Butan als Kugelstabmodell:
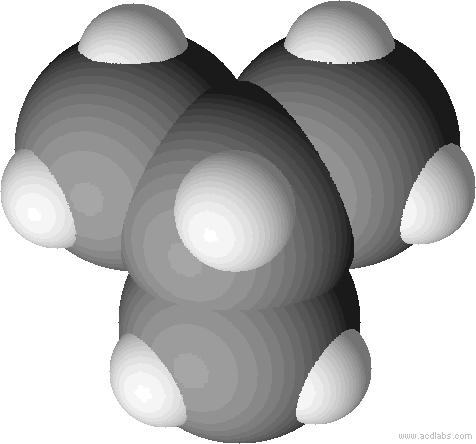
Kalottenmodell von 2-Methylpropan (= Isobutan) – bei Kalottenmodellen wird die Raumfüllung der Atome sichtbar:
Da Strukturformeln bei größeren Molekülen zu aufwendig sind, nutzt man die Halbstrukturformel: Die Wasserstoffatome werden als Summe direkt hinter das jeweilige C-Atom geschrieben. Man ermittelt zunächst, wie viele Bindungen ein C-Atom bereits hat, und ergänzt H-Atome bis zur Vierbindigkeit. Hier am Beispiel Isobutan:
↑ Zum Vergrößern klicken
✕
1.4.4 Verwendung
Heizgas („blaue Gaskartuschen") · Kältemittel (Ersatz für FCKW) · Treibgas in Sprays · Feuerzeuggas (häufig zusammen mit Propan).
1.4.5 Isomerie
(isos (griech.) = gleich; meros (griech.) = Teil)
Definition – Konstitutionsisomerie
Verbindungen, deren Moleküle bei gleicher Summenformel unterschiedliche Strukturformeln besitzen, bezeichnet man als Isomere. Isomere unterscheiden sich vor allem in ihren physikalischen Eigenschaften (Schmelz- und Siedepunkt) und wenig in ihren chemischen Reaktionen.
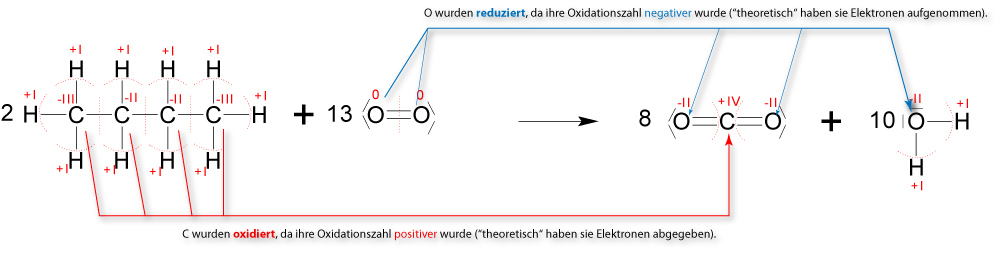
1.4.6 Vollständige Verbrennung (Oxidation)
Wenn Butan vollständig verbrannt wird, entstehen ausschließlich Kohlenstoffdioxid und Wasser:
↑ Zum Vergrößern klicken
✕
Auf einen Blick – Butan
Summenformel
C4H10 · molare Masse 58,12 g/mol · stimmt mit der allg. Formel CₙH₂ₙ₊₂ überein (n = 4 → 4·2+2 = 10 H).
Konstitutionsisomerie
n-Butan (Sdp. −0,5 °C) und Isobutan = 2-Methylpropan (Sdp. −12 °C) haben die gleiche Summenformel C₄H₁₀, aber verschiedene Strukturformeln.
ZMK und Siedepunkt
Nur Van-der-Waals-Kräfte. n-Butan lagert sich dichter zusammen → stärkere ZMK → höherer Siedepunkt als das verzweigte Isobutan.
Halbstrukturformel
H-Atome als Summe hinter das C schreiben. n-Butan: CH₃–CH₂–CH₂–CH₃ · Isobutan: CH₃–CH(CH₃)–CH₃ · Vierbindigkeit von C muss stets erfüllt sein.
Häufige Fragen – Butan
Was versteht man unter Konstitutionsisomerie?
Konstitutionsisomere sind Verbindungen mit gleicher Summenformel, aber unterschiedlicher Verknüpfung der Atome. Bei C₄H₁₀ gibt es zwei Isomere: n-Butan (unverzweigte Kette) und 2-Methylpropan (Isobutan) (verzweigte Kette). Sie unterscheiden sich in physikalischen Eigenschaften wie dem Siedepunkt, kaum aber in chemischen Reaktionen. Mit steigender C-Zahl nimmt die Zahl möglicher Isomere stark zu (C₅: 3, C₁₀: 75).
Warum hat n-Butan einen höheren Siedepunkt als Isobutan?
Beide Isomere sind unpolar und besitzen nur Van-der-Waals-Kräfte als Wechselwirkung zwischen den Molekülen. Die gestreckte Kette von n-Butan ermöglicht eine größere Kontaktfläche zwischen benachbarten Molekülen als die kompaktere, kugelförmigere Gestalt von Isobutan. Größere Kontaktfläche → stärkere Van-der-Waals-Kräfte → höherer Siedepunkt (n-Butan: −0,5 °C; Isobutan: −12 °C).
Was ist der Unterschied zwischen Strukturformel, Halbstrukturformel und Summenformel?
Die Summenformel gibt nur die Anzahl der Atome an (C₄H₁₀), nicht deren Anordnung. Die Strukturformel zeigt alle Bindungsstriche explizit – anschaulich, aber bei großen Molekülen aufwendig. Die Halbstrukturformel ist ein Kompromiss: Das C-Gerüst wird ausgeschrieben, H-Atome werden als Anzahl hinter das jeweilige C-Atom gesetzt. Isobutan: CH₃–CH(CH₃)–CH₃ · n-Butan: CH₃–CH₂–CH₂–CH₃.
Wofür wird Butan im Alltag verwendet?
Butan wird wegen seiner leichten Verflüssigbarkeit unter Druck vielfältig eingesetzt: als Heizgas in Gaskartuschen beim Camping, als Kältemittel (FCKW-Ersatz in Kühlschränken), als Treibgas in Sprühdosen und als Feuerzeuggas (oft zusammen mit Propan).
Wie lautet die ausgeglichene Verbrennungsgleichung für n-Butan?
Vollständige Verbrennung:
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle: C: 8 = 8 ✓ · H: 20 = 20 ✓ · O: 26 = 26 ✓
Die Reaktion ist stark exotherm – deshalb wird Butan als Brennstoff genutzt.
Lernkarten – Butan
Klicke auf eine Karte, um die Antwort zu sehen.
Gib Summenformel und molare Masse von Butan an. Prüfe die allg. Alkan-Formel.
Summenformel: C₄H₁₀
Molare Masse: 58,12 g/mol
Formel CₙH₂ₙ₊₂ mit n=4: 2·4+2 = 10 H ✓
Was sind Konstitutionsisomere? Nenne die beiden C₄H₁₀-Isomere mit Siedepunkten.
Gleiche Summenformel, verschiedene Struktur:
n-Butan: unverzweigt · Sdp. −0,5 °C
2-Methylpropan (Isobutan): verzweigt · Sdp. −12 °C
Schreibe n-Butan und Isobutan als Halbstrukturformel.
n-Butan:
CH₃–CH₂–CH₂–CH₃
Isobutan (2-Methylpropan):
CH₃–CH(CH₃)–CH₃
Warum hat n-Butan einen höheren Siedepunkt als Isobutan, obwohl beide C₄H₁₀ sind?
Nur Van-der-Waals-Kräfte vorhanden.
n-Butan: gestreckte Kette → größere Kontaktfläche
→ stärkere VdW-Kräfte → höherer Siedepunkt
Isobutan: kompaktere Form → weniger Kontakt
Stelle die ausgeglichene Verbrennungsgleichung für n-Butan auf.
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle:
C: 2·4 = 8 | 8·1 = 8 ✓
H: 2·10 = 20 | 10·2 = 20 ✓
O: 13·2 = 26 | 8·2+10 = 26 ✓
Weiter im Kapitel Alkane
← 1.1 Methan → 1.5 Homologe Reihe → 1.6 Nomenklatur
🔁 Grundlagen:
1.1 Methan ·
Lewis-Formeln (Kl. 9)
📚 Vertiefung:
Isomerie bei Alkenen ·
Isomerie (Kursstufe)
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Die homologe Reihe der Alkane ordnet alle gesättigten Kohlenwasserstoffe nach ihrer Kettenlänge. Du lernst die allgemeine Formel CₙH₂ₙ₊₂, siehst wie sich Strukturformel, Halbstrukturformel und Aggregatzustand systematisch ändern – und verstehst, warum der Siedepunkt mit steigender Kettenlänge zunimmt.
Grundlagen aus 1.1 und 1.4
Strukturformeln, Halbstrukturformeln und Konstitutionsisomerie hast du bereits an Methan und Butan kennengelernt: → 1.1 Methan · → 1.4 Butan & Isomerie
(homo = gleich, logos = Stoff)
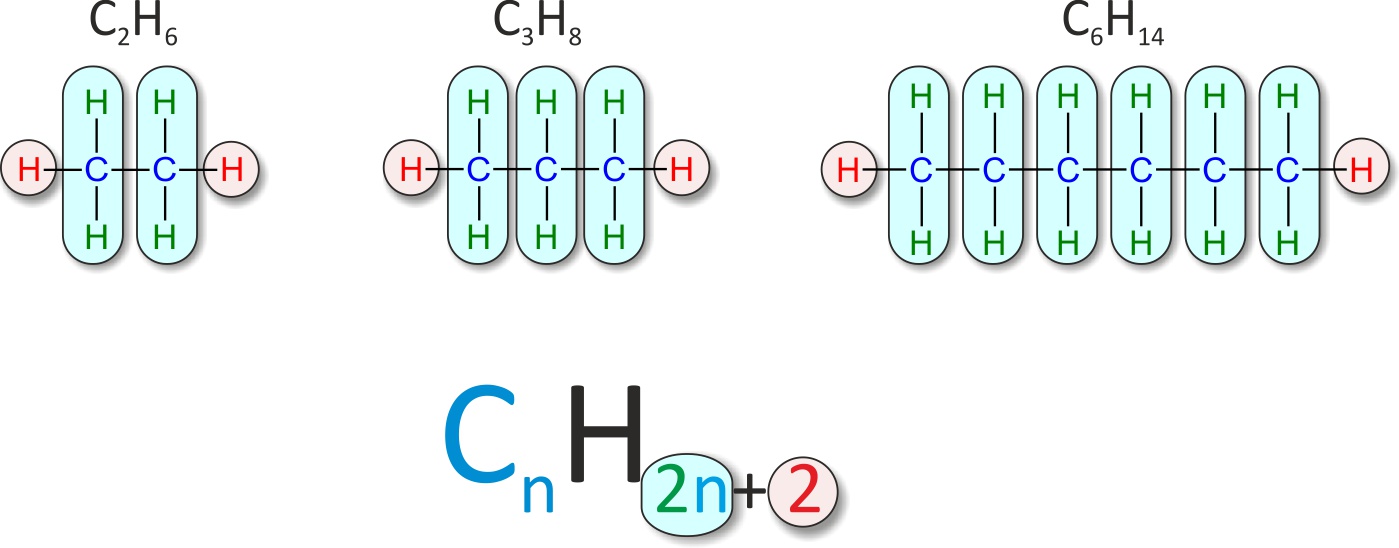
Allgemeine Summenformel der homologen Reihe:
↑ Zum Vergrößern klicken
✕
Definition – Homologe Reihe
Eine Reihe organischer Verbindungen, deren aufeinanderfolgende Glieder sich jeweils um eine bestimmte Atomgruppe – z. B. eine –CH₂– Gruppe – unterscheiden, nennt man homologe Reihe. Für Alkane gilt die allgemeine Summenformel CnH2n+2.
Wichtigste Eigenschaften aller Alkane:
- Brennbar (bei vollständiger Verbrennung entstehen CO2 und H2O)
- Dichte < 1 g/cm³ (leichter als Wasser)
- In Wasser unlöslich (nur Spuren); untereinander in jedem Verhältnis mischbar
Die homologe Reihe der Alkane (Übersicht)
| Name | Summenformel | Strukturformel | Halbstrukturformel | Aggregatzustand |
|---|---|---|---|---|
| Methan | CH4 |
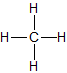 |
CH4 | gasförmig |
| Ethan | C2H6 |
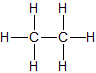 |
CH3–CH3 | gasförmig |
| Propan | C3H8 |
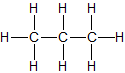 |
CH3–CH2–CH3 | gasförmig |
| n-Butan | C4H10 |
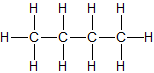 |
CH3–CH2–CH2–CH3 | gasförmig |
| n-Pentan | C5H12 |
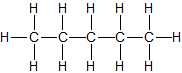 |
CH3–(CH2)3–CH3 | flüssig |
| n-Hexan | C6H14 |
|
CH3–(CH2)4–CH3 | flüssig |
| n-Heptan | C7H16 |
|
CH3–(CH2)5–CH3 | flüssig |
| n-Octan | C8H18 |
|
CH3–(CH2)6–CH3 | flüssig |
| n-Nonan | C9H20 |
|
CH3–(CH2)7–CH3 | flüssig |
| n-Decan | C10H22 |
|
CH3–(CH2)8–CH3 | flüssig |
| n-Undecan | C11H24 |
|
CH3–(CH2)9–CH3 | flüssig |
| n-Dodecan | C12H26 |
|
CH3–(CH2)10–CH3 | flüssig |
| … (C₁₃ bis C₁₆ flüssig) | ||||
| n-Heptadecan | C17H36 |
|
CH3–(CH2)15–CH3 | fest |
Auf einen Blick – Homologe Reihe der Alkane
Allgemeine Formel
CₙH₂ₙ₊₂ – jedes folgende Glied enthält eine –CH₂–-Gruppe mehr als das vorherige. Das verbindet alle Alkane zur homologen Reihe.
Aggregatzustände
C₁–C₄: gasförmig · C₅–C₁₆: flüssig · ab C₁₇: fest. Der Siedepunkt steigt mit wachsender Kettenlänge gleichmäßig an.
ZMK und Siedepunkt
Zwischen Alkanen wirken nur Van-der-Waals-Kräfte. Längere Kette = größere Moleküloberfläche = stärkere VdW-Kräfte = höherer Siedepunkt.
Eigenschaften
Alle Alkane sind brennbar, unpolar, in Wasser unlöslich und besitzen eine Dichte < 1 g/cm³. Chemisch reagieren sie wegen starker Einfachbindungen kaum.
Häufige Fragen – Homologe Reihe der Alkane
Was ist eine homologe Reihe und was verbindet die Glieder?
Eine homologe Reihe ist eine Gruppe organischer Verbindungen, deren aufeinanderfolgende Glieder sich jeweils um eine –CH₂–-Gruppe unterscheiden. Alle Glieder haben die gleiche allgemeine Summenformel (CₙH₂ₙ₊₂ für Alkane), ähnliche chemische Eigenschaften und kontinuierlich variierende physikalische Eigenschaften (Siedepunkt, Dichte etc.).
Warum wechselt der Aggregatzustand von gasförmig über flüssig zu fest?
Mit steigender Kettenlänge wächst die Moleküloberfläche. Über diese Fläche wirken Van-der-Waals-Kräfte – je größer die Fläche, desto stärker die Anziehung zwischen den Molekülen. Ab einer bestimmten Kettenlänge reicht die Wärmeenergie bei Raumtemperatur nicht mehr aus, die Moleküle voneinander zu trennen: C₁–C₄ gasförmig · C₅–C₁₆ flüssig · ab C₁₇ fest. → Eigenschaften der Alkane
Wie leitet man die Halbstrukturformel eines Alkans aus der Summenformel ab?
Man schreibt das Kohlenstoffgerüst in einer Kette und ergänzt H-Atome so, dass jedes C-Atom vierwertig ist: Die beiden Endgruppen sind immer CH₃–, jede mittlere Gruppe ist –CH₂–. Beispiel n-Hexan (C₆H₁₄): CH₃–(CH₂)₄–CH₃. Die Klammernotation (CH₂)ₙ spart Schreibarbeit bei langen Ketten.
Warum sind Alkane in Wasser unlöslich?
Alkane sind unpolare Moleküle – es gibt keine Partialladungen und keine Wasserstoffbrückenbindungen. Wasser dagegen ist polar und bildet starke Wasserstoffbrücken zwischen seinen Molekülen. Ein unpolares Alkan könnte diese Netzstruktur nicht ersetzen, daher ist das Einbringen energetisch ungünstig – „similia similibus solvuntur" (Gleiches löst Gleiches). In anderen unpolaren Lösungsmitteln (Benzin, Ether) lösen sich Alkane dagegen gut.
Wie berechnet man die Summenformel eines Alkans für beliebiges n?
Mit der allgemeinen Formel CₙH₂ₙ₊₂:
Einfach n einsetzen.
Beispiel n = 8 (Octan): C₈H₂·₈₊₂ = C₈H₁₈ ✓
Umgekehrt: Aus der Summenformel C₁₂H₂₆ folgt 2n+2 = 26 → n = 12 → Dodecan.
Kontrolle: Molare Masse = 12·12 + 26·1 = 170 g/mol.
Lernkarten – Homologe Reihe der Alkane
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist die allgemeine Summenformel der Alkane? Worum unterscheiden sich je zwei aufeinanderfolgende Glieder?
Allg. Formel: CₙH₂ₙ₊₂
Aufeinanderfolgende Glieder unterscheiden sich um eine –CH₂–-Gruppe.
→ Deshalb heißen sie homologe Reihe.
Ab welcher Kettenlänge sind Alkane bei Raumtemperatur flüssig? Ab wann fest?
C₁–C₄: gasförmig
C₅–C₁₆: flüssig
ab C₁₇: fest
Ursache: stärkere Van-der-Waals-Kräfte mit wachsender Kettenlänge
Gib Name, Summenformel und Halbstrukturformel für das Alkan mit n = 5 an.
n = 5 → n-Pentan
Summenformel: C₅H₁₂
(2·5+2 = 12 H ✓)
Halbstrukturformel:
CH₃–CH₂–CH₂–CH₂–CH₃
oder CH₃–(CH₂)₃–CH₃
Warum steigt der Siedepunkt in der homologen Reihe der Alkane mit zunehmender Kettenlänge?
Längere Kette → größere Moleküloberfläche
→ stärkere Van-der-Waals-Kräfte
→ mehr Energie nötig zur Trennung der Moleküle
→ höherer Siedepunkt
Ein Alkan hat die Summenformel C₁₀H₂₂. Wie heißt es? Wie lautet die Halbstrukturformel? Welchen Aggregatzustand hat es bei Raumtemperatur?
C₁₀H₂₂ → n = 10 → n-Decan
Halbstrukturformel:
CH₃–(CH₂)₈–CH₃
Aggregatzustand: flüssig
(C₅–C₁₆ sind bei RT flüssig)
Weiter im Kapitel Alkane
← 1.4 Butan → 1.6 Genfer Nomenklatur → 1.7 Eigenschaften
🔁 Grundlagen:
1.1 Methan ·
1.4 Butan & Isomerie
📚 Vertiefung:
2.1 Ethen – Homologe Reihe der Alkene ·
Siedepunkte und ZMK (Carbonsäuren)
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Mit der Genfer Nomenklatur (IUPAC-System) kannst du verzweigte Alkane eindeutig benennen und aus einem Namen die Strukturformel ableiten. Du lernst die sieben Nomenklaturregeln Schritt für Schritt kennen und wendest sie an konkreten Beispielmolekülen an.
Grundlagen aus dem Alkane-Kapitel
Die homologe Reihe der Alkane und den Begriff des Alkylrests hast du bereits im vorherigen Abschnitt kennengelernt: → 1.5 Homologe Reihe der Alkane
1.6 Nomenklatur (Benennung) der Alkane
1.6.1 Homologe Reihe der Alkane mit Alkylrest
Ein Alkylrest enthält jeweils ein Wasserstoff-Atom weniger als das entsprechende Alkanmolekül. Alkyle finden sich oft als „Seitengruppe" verzweigter Alkane.
| Name | Summenformel | Name des Alkyls | Summenformel |
| Methan | CH4 | Methylrest | –CH3 |
| Ethan | C2H6 | Ethylrest | –C2H5 |
| Propan | C3H8 | Propylrest | –C3H7 |
| allg. Alkane | CnH2n+2 | Alkylrest | –CnH2n+1 |
1.6.2 Nomenklaturregel für Alkane (Genfer Nomenklatur)
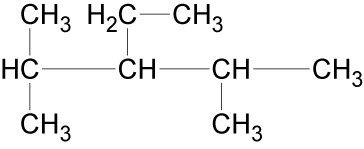
Als Beispiel soll folgendes Molekül systematisch benannt werden:
↑ Zum Vergrößern klicken
✕
-
Alkane haben die Endung -an.
-
Der Name des Alkans, das die Hauptkette bildet, liefert den Stammnamen des Stoffs.
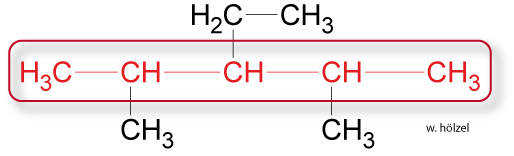
Längste Kette der Kohlenstoffkette suchen und „Glattbügeln".↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕
-
Alle Alkane mit 5 Kohlenstoff-Atomen in der längsten Kette heißen Pentan.
-
Die Namen der Seitenketten werden dem Stammnamen vorangestellt.
↑ Zum Vergrößern klicken
✕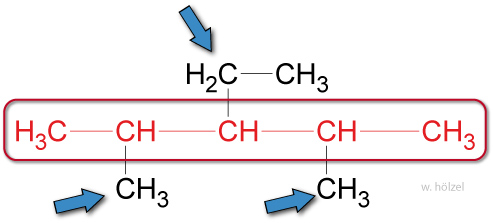
Beispiel: Methyl-Ethyl-Pentan.
-
Um anzuzeigen, an welchem Kohlenstoff-Atom die Seitenkette sitzt, wird die Hauptkette nummeriert. Die Verzweigungsstellen sollen dabei möglichst kleine Zahlen erhalten. Die Zahlen werden den Namen der Seitenketten vorangestellt.
↑ Zum Vergrößern klicken
✕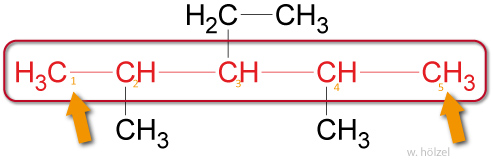
Beispiel: 2,4-Methyl-3-Ethyl-Pentan.
-
Treten gleiche Seitenketten mehrfach in einem Molekül auf, so wird das entsprechende Zahlwort (Di-, Tri-, Tetra-, Penta-) als Vorsilbe verwendet.
↑ Zum Vergrößern klicken
✕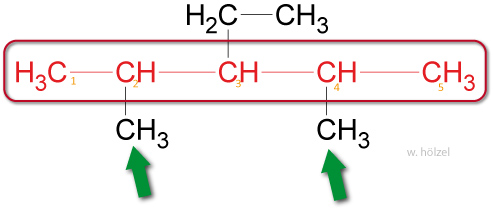
Beispiel: 2,4-Dimethyl-3-Ethyl-Pentan.
-
Unterschiedliche Seitenketten werden alphabetisch nach dem Namen der Alkylgruppe geordnet.
↑ Zum Vergrößern klicken
✕
Beispiel: 3-Ethyl-2,4-Dimethylpentan.
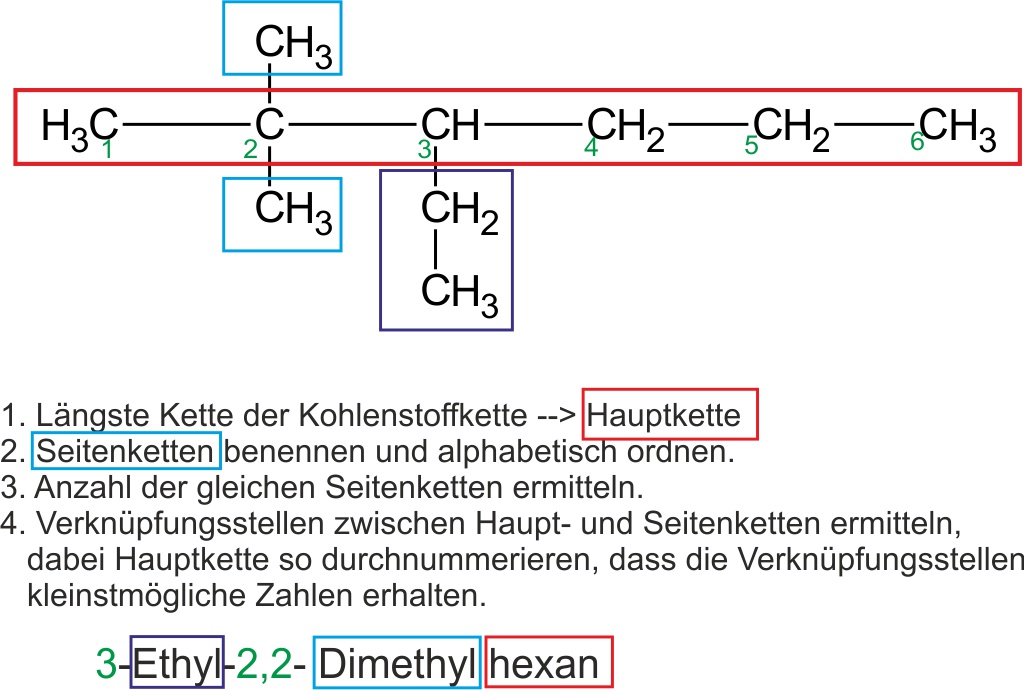
Folgende Abbildung zeigt ein weiteres Beispiel für die vollständige Anwendung aller Nomenklaturregeln:
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
HAUPTKETTE
Die längste zusammenhängende C-Kette bestimmt den Stammnamen (z. B. Pentan für 5 C-Atome).
LOKANTEN
Die Hauptkette wird so nummeriert, dass die Verzweigungsstellen möglichst kleine Zahlen erhalten.
VORSILBEN
Gleiche Seitenketten werden gezählt: Di- (2×), Tri- (3×), Tetra- (4×). Diese Vorsilben zählen nicht bei der alphabetischen Sortierung.
ALPHABETISCH
Verschiedene Seitenketten stehen im Namen in alphabetischer Reihenfolge – Ethyl (E) vor Methyl (M).
Häufige Fragen – Genfer Nomenklatur der Alkane
Was ist der Unterschied zwischen einem Alkan und einem Alkylrest?
Ein Alkan ist ein gesättigter Kohlenwasserstoff mit der allgemeinen Formel CnH2n+2. Ein Alkylrest entsteht, wenn man einem Alkan-Molekül ein Wasserstoff-Atom „entfernt"; seine allgemeine Formel lautet –CnH2n+1. Alkylreste treten als Seitenketten in verzweigten Alkanen auf – zum Beispiel der Methylrest (–CH3) oder der Ethylrest (–C2H5).
Wie bestimmt man die Hauptkette bei einem verzweigten Alkan?
Man sucht die längste zusammenhängende Kohlenstoffkette im Molekül. Es hilft, die Kette gedanklich „glatt zu bügeln". Der Name des entsprechenden unverzweigten Alkans (Methan, Ethan, Propan, Butan, Pentan, Hexan …) bildet den Stammnamen. Bei gleich langen Ketten wählt man diejenige, die die meisten Seitenketten trägt.
Warum sollen die Lokanten (Positionszahlen) möglichst klein sein?
Die Regel der niedrigsten Lokanten sorgt dafür, dass es für jede Verbindung nur einen eindeutigen IUPAC-Namen gibt. Die Hauptkette wird von dem Ende aus nummeriert, das dem ersten Verzweigungspunkt am nächsten liegt. So ergibt sich beispielsweise „2-Methylbutan" statt „3-Methylbutan" für dieselbe Verbindung.
Was bedeuten die Vorsilben Di-, Tri- und Tetra-?
Treten gleiche Seitenketten mehrfach auf, wird die Anzahl als Zahlwort vor den Seitenkettenname gesetzt: Di- (2×), Tri- (3×), Tetra- (4×), Penta- (5×). Alle zugehörigen Lokanten werden aufgelistet, z. B. „2,4-Dimethyl" für zwei Methylgruppen an C-Atom 2 und 4. Wichtig: Diese Zahlvorsilben werden bei der alphabetischen Sortierung der Seitenketten nicht berücksichtigt.
In welcher Reihenfolge werden unterschiedliche Seitenketten im Namen angegeben?
Verschiedene Seitenketten werden alphabetisch nach dem Namen der Alkylgruppe geordnet – dabei bleiben Zahlvorsilben wie Di- oder Tri- außer Acht. Ethyl (E) kommt daher vor Methyl (M), also z. B.: „3-Ethyl-2,4-dimethylpentan". Mehr zur Nomenklatur der nächsten Stoffklasse findest du auf der Seite → Nomenklatur der Alkene (Kl. 10).
Lernkarten – Genfer Nomenklatur
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist ein Alkylrest und wie lautet seine allgemeine Formel?
Ein Alkylrest ist ein Alkan, dem ein H-Atom fehlt. Formel: –CnH2n+1 (z. B. Methylrest –CH3, Ethylrest –C2H5).
Was bestimmt den Stammnamen eines verzweigten Alkans?
Die längste zusammenhängende Kohlenstoffkette (Hauptkette). 5 C-Atome → Pentan; 6 C-Atome → Hexan usw.
Wie wird die Hauptkette nummeriert?
Von dem Ende aus, das dem ersten Verzweigungspunkt am nächsten liegt → niedrigste Lokanten für alle Seitenketten.
Welche Reihenfolge gilt für verschiedene Seitenketten im IUPAC-Namen?
Alphabetisch nach dem Alkylgruppennamen (ohne Vorsilben Di-, Tri-). Ethyl (E) vor Methyl (M).
Wie heißt: 6 C-Kette, Ethylgruppe an C-3, zwei Methylgruppen an C-2 und C-2?
3-Ethyl-2,2-dimethylhexan
(Hexan = 6 C; 2,2-Dimethyl = zwei Methyl an C-2; 3-Ethyl an C-3; E vor M).
Weiter im Kapitel Alkane
← 1.5 Homologe Reihe der Alkane → 1.6 Übungen zur Nomenklatur
🔁 Weiter in der Organik: Nomenklatur der Alkene (Kl. 10)
- Details
- Geschrieben von: Wolfram Hölzel
