Was du in diesem Kapitel lernst
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung – noch reaktiver als die Alkene. Das wichtigste Alkin ist Ethin (Acetylen): du lernst seine Eigenschaften, seine technische Herstellung aus Calciumcarbid und die für Alkine typischen zweistufigen Additionsreaktionen kennen.
Grundlagen aus der 10. Klasse
Alkine bauen auf dem Wissen über ungesättigte Verbindungen auf – wiederhole bei Bedarf: → 2. Alkene – C=C-Doppelbindung, Bromwasserprobe, Additionsreaktion
Kapitelübersicht – 3. Alkine
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkine besitzen eine C≡C-Dreifachbindung (1 σ- + 2 π-Bindungen). Die Bindungslänge ist mit 120 pm kürzer als bei der Doppelbindung (134 pm). Allgemeine Formel: CnH2n−2.
Herstellung
Ethin entsteht aus Calciumcarbid und Wasser: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Diese Reaktion liefert das Gas auch in der Carbidlampe.
Reaktionstyp
Alkine reagieren durch elektrophile Addition. Die Reaktion läuft zweistufig ab: erst entsteht ein Alken-Zwischenprodukt, dann wird erneut addiert → schließlich ein Alkan oder Derivat.
Linearstruktur
Ethin ist linear: alle vier Atome liegen auf einer Geraden (Bindungswinkel 180°). Die Dreifachbindung besteht aus drei „Bananenbindungen" (sp-Hybridisierung).
Häufige Fragen – Alkine
Was sind Alkine, und was unterscheidet sie von Alkenen?
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung, bestehend aus einer σ-Bindung und zwei π-Bindungen. Die allgemeine Formel lautet CnH2n−2 (noch zwei H-Atome weniger als bei Alkenen: CnH2n). Alkine sind durch die Dreifachbindung noch reaktiver als Alkene. Das einfachste Alkin ist Ethin (C2H2), auch Acetylen genannt. Wie Alkene zeigen Alkine elektrophile Additionsreaktionen, jedoch oft zweistufig.
Wie wird Ethin (Acetylen) technisch hergestellt?
Ethin lässt sich aus Calciumcarbid (CaC2) und Wasser herstellen. Reaktionsgleichung: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Calciumcarbid wird in der Carbidlampe (Grubenlampe) genutzt: Das entstehende Ethin verbrennt mit einer hellen, stark leuchtenden Flamme. Industriell wird Ethin heute hauptsächlich durch Cracken von Erdgas gewonnen. → 3.1.3 Herstellung
Was ist die Besonderheit der linearen Struktur von Ethin?
Beim Ethin sind alle vier Atome linear angeordnet (Bindungswinkel 180°, sp-Hybridisierung). Die C≡C-Dreifachbindung besteht nach dem Bananenbindungsmodell aus drei gebogenen Bindungen (σ + 2 π). Die Bindungslänge beträgt nur 120 pm (zum Vergleich: C=C 134 pm, C–C 154 pm). Diese kompakte Struktur erklärt die hohe Reaktivität und die ausgeprägte elektrophile Addition. → 3.1 Ethin
Wie verläuft die Bromierung von Ethin – und warum ist sie zweistufig?
Ethin reagiert mit Brom in einer elektrophilen Addition, die zweistufig abläuft: In der ersten Stufe addiert Br2 an die Dreifachbindung → es entsteht das Zwischenprodukt trans-1,2-Dibromethen (noch eine Doppelbindung vorhanden). In der zweiten Stufe reagiert dieses mit weiterem Br2 → 1,1,2,2-Tetrabromethan (gesättigtes Endprodukt). Wird Br2 im Unterschuss eingesetzt, kann man die Reaktion auf der Dibromstufe stoppen. → 3.2 Reaktionstyp
Welche Verwendungen hat Ethin in Industrie und Technik?
Ethin (Acetylen) wird vielfältig genutzt: (1) Autogenschweißen und Schneiden: Die Verbrennung mit Sauerstoff erzeugt eine Flamme von über 3000 °C. (2) Ausgangsstoff in der Chemie: Aus Ethin werden wichtige Kunststoffe und Lösungsmittel hergestellt (z. B. PVC über Vinylchlorid). (3) Carbidlampen: Historisch als tragbare Lichtquelle in Bergbau und Feuerwehr. (4) Bei Pflanzen spielt das analoge Ethylen (= Ethen) als Phytohormon eine Rolle – Ethin kann diese Wirkung verstärken.
Lernkarten – Alkine
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist die funktionelle Gruppe der Alkine, und woraus besteht sie?
Die C≡C-Dreifachbindung. Sie besteht aus einer σ-Bindung + zwei π-Bindungen. Bindungslänge: 120 pm. Hybridisierung: sp. Alle vier Atome in Ethin sind linear angeordnet (180°).
Wie lautet die allgemeine Formel der Alkine? Nenne Ethin und Propin mit Formel.
CnH2n−2 (n ≥ 2)
Ethin: C2H2 (HC≡CH)
Propin: C3H4 (CH3–C≡CH)
Wie wird Ethin aus Calciumcarbid hergestellt? Nenne die Reaktionsgleichung.
CaC2 + 2 H2O
→ C2H2 + Ca(OH)2
Calciumcarbid reagiert mit Wasser zu Ethin und Calciumhydroxid.
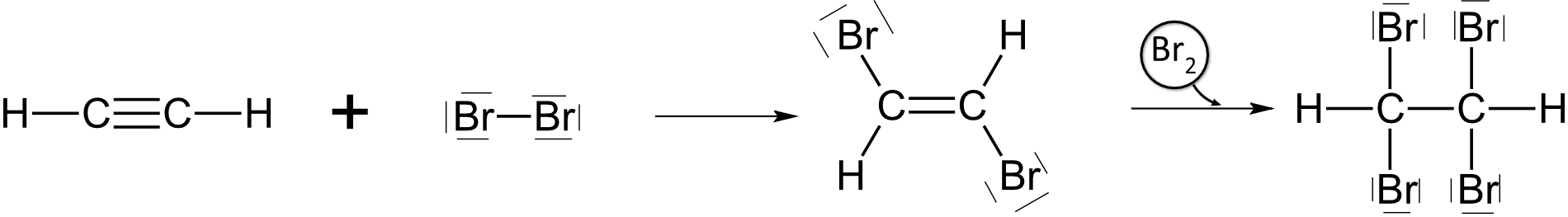
Wie verläuft die Bromierung von Ethin – welche zwei Stufen gibt es?
Stufe 1: C2H2 + Br2 → C2H2Br2 (trans-1,2-Dibromethen, noch C=C)
Stufe 2: + Br2 → C2H2Br4 (1,1,2,2-Tetrabromethan)
Berechne: Wie viel g Br2 werden benötigt, um 26 g Ethin vollständig zu tetrabromieren?
C2H2 + 2 Br2 → C2H2Br4
M(C2H2) = 26 g/mol → n = 1 mol
n(Br2) = 2 mol → m = 2 · 160 g/mol = 320 g Br2
Weiter im Fach Chemie / 10. Klasse
← 2. Alkene → 5. Alkohole ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Cycloalkane · Aromaten – Benzol und seine Derivate
- Details
- Geschrieben von: Wolfram Hölzel
3.1 Ethin (Acetylen)
3.1.1 Eigenschaften
a) physikalische Eigenschaften
- farbloses Gas (geruchslos)
- leichter als Luft
- Smp.: -80,8°C
- Sdp.: - 84°C (Sublimation)
b) chemische
- brennt mit stark leuchtender und rußender Flamme
- entfärbt Bromwasser
- bildet mit Luft ein explosives Gemisch
- zerfällt unter Druck explosionsartig (⇨ nicht in Druckflaschen)
3.1.2 Formelermittlung
Verbrennungsprodukte: H₂O, CO₂ (und bei unvollständiger Verbrennung C)
Molare Masse: M(Ethin) = 26 g/mol
Ermittel aus der molaren Masse die Summen- und die Strukturformel:
{slider title="Lösung" open="false" class="icon"}
Summenformel: C₂H₂
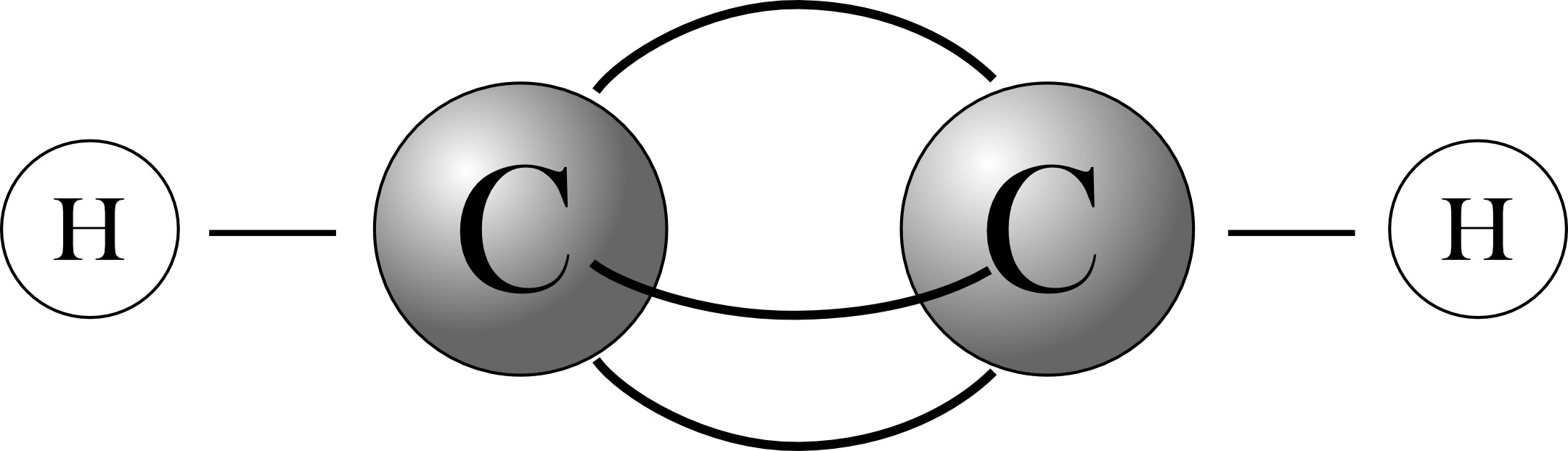
Strukturformel:
(linear; Bindungswinkel 180°)Bindungslänge noch geringer als bei der Doppelbindung (C=C: 134 pm; C=-C: 120 pm)
Ballmodell:
3 „Bananenbindungen“, alle 4 Atome sind linear angeordnet.
{/sliders}
- Details
- Geschrieben von: Wolfram Hölzel
3.1.3 Herstellung
- Wasser wird auf Calciumcarbid (CaC₂) getropft (vgl unten)
- Cracken von Erdöl
3.1.4 Funktionsweise von Carbidlampen
Gewinnung von Calciumcarbid aus Kohle und Kalkstein;Technisch wird Calciumcarbid im Lichtbogenofen bei 2500 °C aus Calciumoxid (Branntkalk) und Koks gewonnen, so dass die Herstellung durch den hohen Stromverbrauch sehr kostenintensiv ist.
a) Bildung von Calciumcarbid:
Im Lichtbogenofen (2500 °C) aus Calciumoxid und Koks (C) gewonnen. Dabei entsteht CO.
Aufgabe: Formulierte die Reaktionsgleichung für die Bildung:
{slider title="Lösung" open="false" class="icon"}
CaO + 3 C → CaC₂ + CO
{/sliders}
b) Bildung von Ethin (Auftropfen auf Calciumcarbid):
Calciumcarbid + Wasser → Ethin + Calciumhydroxid ΔH < 0
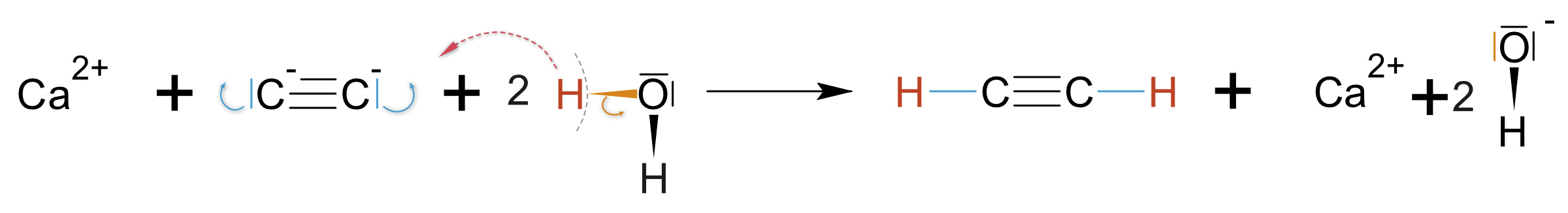
CaC₂ ist eine Ionenverbindung: Ca²⁺ + C₂²⁻
Formuliert hier die Reaktionsgleichung mit bindenden und nichtbindenden Elektronenpaare (Lewis/Strukturformel):
{slider title="Lösung" open="false" class="icon"}
{/sliders}
c) Verbrennung von Ethin
Stark Exotherm (Temp. Über 3000 °C ⇨ Eisen und Stahl schmilzt).
Aufgabe: Eine vollständige Verbrennungsreaktion müsste jetzt keine Schwierigkeiten mehr bereiten. Formuliere die vollständige Verbrennung in Strukturformelschreibweise und ergänze diese mit Oxidationszahlen.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
3.1.5 Verwendung
- Autogenes Schweißen (vgl. Verbrennungsreaktionsgleichung)
- Wichtiger Grundstoff für Synthesen
- Details
- Geschrieben von: Wolfram Hölzel
3.2 Reaktionstyp bei Alkinen
Wie bei Doppelbindungen ⇨ Additionsreaktionen
a) Addition von Halogene
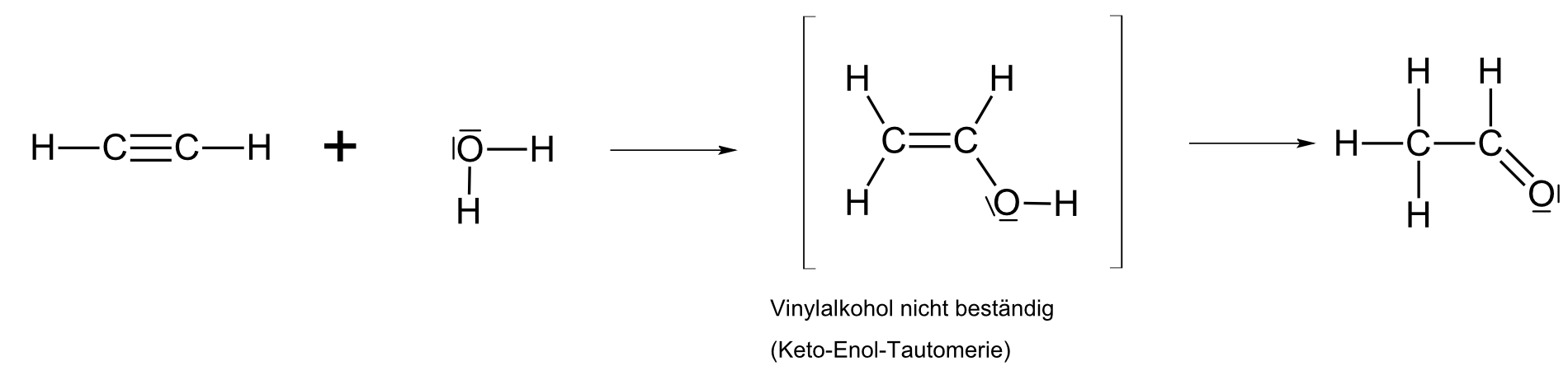
b) mit Wasser
Es gibt viele weitere Reaktionen, die technisch genutzt werden.
Überungsaufgaben
1. Gib alle möglichen Strukturformeln von Propin und Butin an (nur eine Mehrfachbindung).
{slider title="Lösung" open="false" class="icon"}
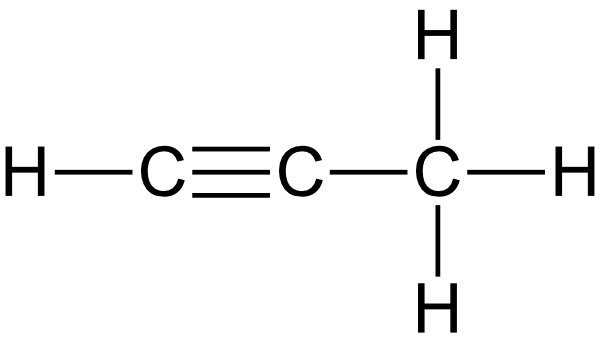
Propin:
Butin:
2-Butin oder But-2-in
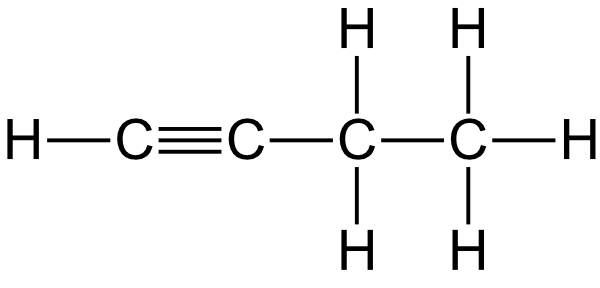
1-Butin oder But-1-in
{/sliders}
2. Formuliere die Reaktionsgleichungen für
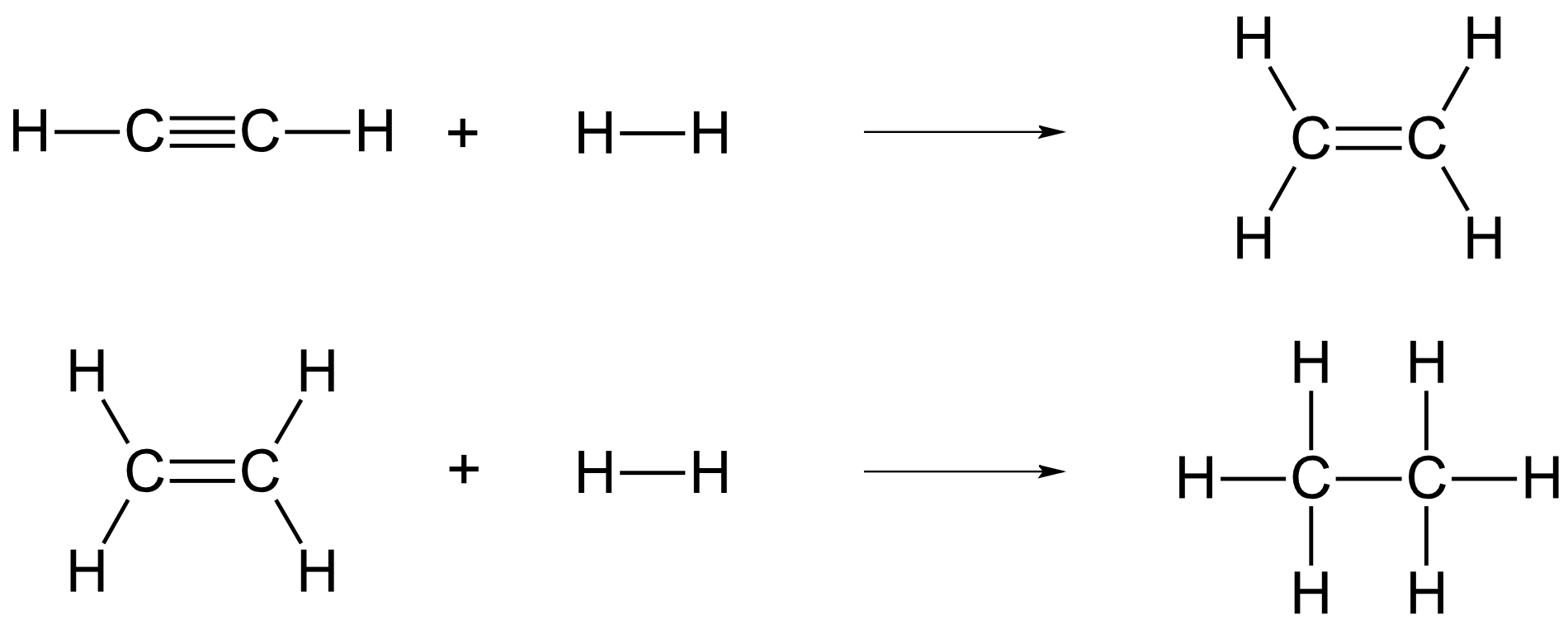
a) die Reaktion von Ethin zu Ethen und dann zu Ethan;
{slider title="Lösung" open="false" class="icon"}
{/sliders}
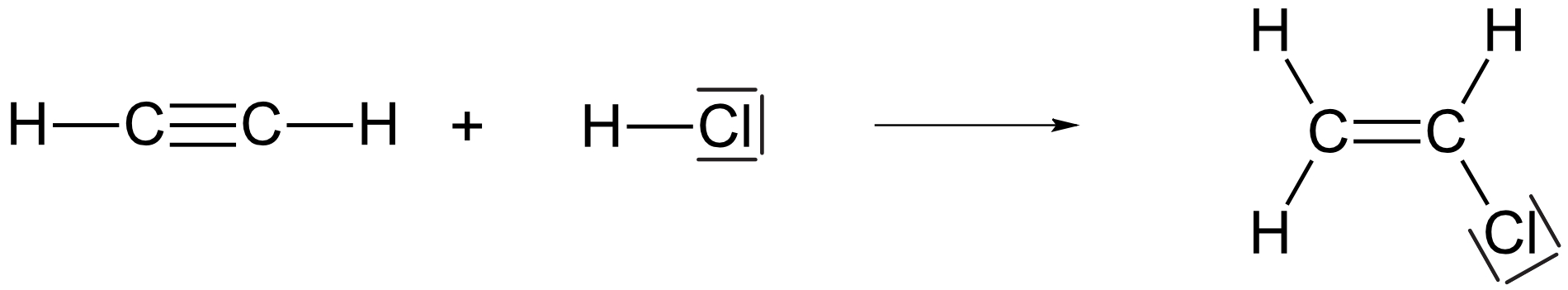
b) die Herstellung von Chlorethen aus Ethin.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
3. Bei Alkenen findet man die cis-trans-Isomerie. Gibt es das auch bei Alkinen?
{slider title="Lösung" open="false" class="icon"}
Nein, da an den beiden C-Atomen der C-C-Dreifachbindung sich nur je ein Atom/Atomgruppe befindet und der Bindungswinkel 180° beträgt. Es gibt somit keine "gegenüberliegende" Seite.
{/sliders}
4. Ethin wird heute vorwiegend durch unvollständige Verbrennung von Methan hergestellt. Formuliere die Reaktionsgleichung als Summenformel.
{slider title="Lösung" open="false" class="icon"}
4 CH₄ (g) + 3 O₂ (g) → 2 C₂H₂ (g) + 6 H₂O (g)
{/sliders}
- Details
- Geschrieben von: Wolfram Hölzel